Презентация на тему: Элементы металлы

Презентация открытого урока химии в 8 классе на тему: «Простые вещества – неметаллы. Аллотропия» учителя химии и биологии МАОУ «Средняя общеобразовательная школа №1» Тихоновой Натальи Сергеевны. 900igr.net

Тема урока: «Простые вещества – неметаллы. Аллотропия»

Цели урока: Получить представление о простых веществах – неметаллах; Познакомиться с общими физическими свойствами неметаллов и явлением аллотропии; Научиться определять принадлежность веществ к неметаллам;

Проверка домашнего задания. 1. Где в периодической системе находятся элементы, соответствующие простым веществам металлам?

2. Каковы общие физические свойства металлов?

3. По каким физическим свойствам различаются металлы?

4. Какое из веществ названных в приведённом ниже стихотворении, не относится к металлам? Семь металлов создал Свет По числу семи планет: Медь, железо, серебро… Дал нам Космос на добро. Злато, олово, свинец… Сын мой, сера - их отец. А ещё ты должен знать: Всем им ртуть – родная мать.

Изучение новой темы. «Простые вещества – неметаллы. Аллотропия»

Неметаллы - это химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.

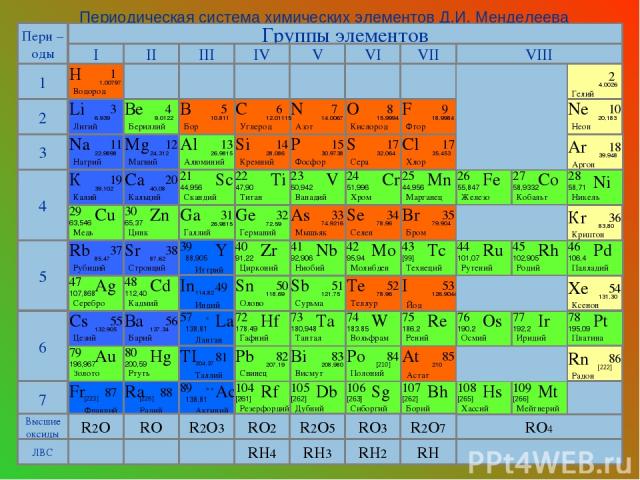
Периодическая система химических элементов Д.И. Менделеева

Газообразные вещества неметаллы: О2 - N2 - H2 - Cl2 - F2 -

N2 Cl2 F2 В начало

благородные газы: He - Ne - Ar - Kr - Xe - Rn - Инертные газы Каждая молекула инертного газа состоит из одного атома. Покажите как распределяются электроны в атомах гелия и неона.

Строение внешнего электронного слоя атомов гелия и неона +2 He ) 2 +10 Ne ) ) 2 8

Применение гелия, неона и аргона.

Единственное жидкое вещество - Br2.

Твердые вещества: S – P – I2 – C – Si -

Аллотропия – способность атомов одного химического элемента образовывать несколько простых веществ. Причины аллотропии: Различное число атомов в молекуле; Образование различных кристаллических форм.

Аллотропия кислорода. Кислород и озон

Модификации кислорода. О2- кислород; бесцветный газ; не имеет запаха; плохо растворим в воде; температура кипения-182,9 С; устойчивая молекула. О3 – озон; газ голубого цвета; имеет резкий запах; растворяется в 10 раз лучше, чем кислород; температура кипения -111,9 С; не устойчивая молекула.

Аллотропия фосфора. Красный и белый фосфор Р (красный фосфор) (белый фосфор) Р4
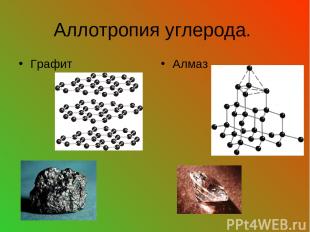
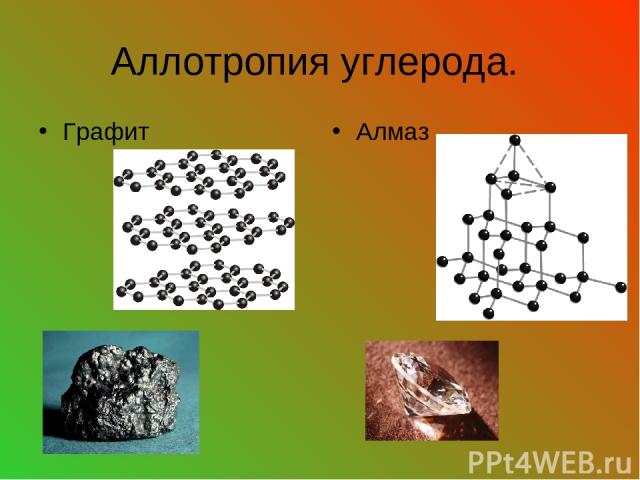
Аллотропия углерода. Графит Алмаз

Аллотропия серы. Кристаллическая, пластическая и моноклинная

Пограничное положение между металлами и неметаллами. Белое олово металл Серое олово неметалл

Почему химически неверно поэтическое выражение: «В воздухе пахло грозой»?

Экспедиция полярного исследователя Р. Скотта к Южному полюсу в 1912 году погибла из-за того, что потеряла весь запас горючего: оно находилось в запаянных оловом баках. Какой химический процесс лежал в основе этого?

Какой тип химической связи должен быть в металлическом водороде?

Выполните задание. 1 вариант О2 – кислород, газ; Р4 – I2 – Si – бетта Sn – He – H2 – F2 - 2 вариант О3 –озон, газ; P – C – альфа Sn – Ne – N2 – Cl2 – Br2 –

Проверь ответы. 1 вариант О2 – кислород, газ; Р4 – белый фосфор,твёрдый; I2 – йод, твердый Si – кремний, твердый бетта Sn – белое олово, металл, твёрдое; He – гелий, благородный газ; H2 – водород, газ; F2 – фтор, газ. 2 вариант О3 –озон, газ; P – красный фосфор, твёрдый; C – углерод, твёрдый; альфа Sn – серое олово, неметалл, порошок; Ne – неон,благородный газ; N2 – азот, газ; Cl2 – хлор, газ; Br2 – бром, жидкость.

Критерии оценок 8 правильных ответов – «5»; 7,6 првильных ответов – «4»; 5,4 правильных ответов – «3»; Менее 4 правильных ответов – «2»;

Спасибо за внимание!