Презентация на тему: Электролитическая диссоциация

ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ 8 КЛАСС 5klass.net

Цели урока Обобщить сведения об ионах Закрепить умение записывать процесс диссоциации при помощи химических знаков и формул Сформулировать основные положения теории электролитической диссоциации

ПРОВЕРЬ СВОИ ЗНАНИЯ Вещества, растворы которых проводят электрический ток, называют ……… Процесс распада электролита на ионы называют …….. Вещества, растворы которых не проводят электрический ток, называют ………. Отношение числа частиц, распавшихся на ионы, к общему числу растворенных частиц называют …………
ПРОВЕРЬ СВОИ ЗНАНИЯ (дополните схему) ЭЛЕКТРОЛИТЫ (по степени электролитической диссоциации )
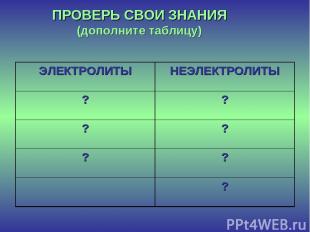
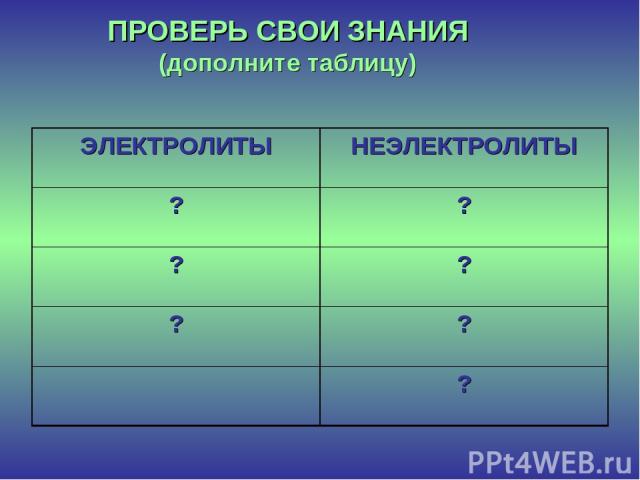
ПРОВЕРЬ СВОИ ЗНАНИЯ (дополните таблицу) ЭЛЕКТРОЛИТЫ НЕЭЛЕКТРОЛИТЫ ? ? ? ? ? ? ?
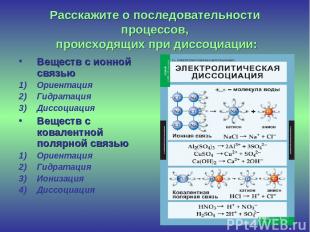
Расскажите о последовательности процессов, происходящих при диссоциации: Веществ с ионной связью Ориентация Гидратация Диссоциация Веществ с ковалентной полярной связью Ориентация Гидратация Ионизация Диссоциация

История открытия теории электролитической диссоциации В 1887 году шведский химик Сванте Аррениус сформулировал основные положения теории электролитической диссоциации

Основные положения ТЭД При растворении в воде электролиты диссоциируют (распадаются) на положительные и отрицательные ионы. NaCl = Na+ + Cl- Ионы – это одна из форм существования химического элемента
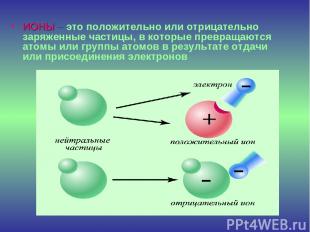
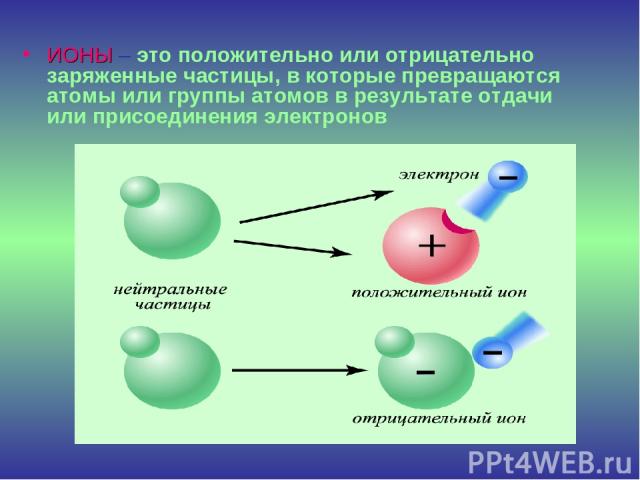
ИОНЫ – это положительно или отрицательно заряженные частицы, в которые превращаются атомы или группы атомов в результате отдачи или присоединения электронов

ЭЛЕКТРОННЫЕ ФОРМУЛЫ +11Na0 2ē 8ē 1ē +11Na+ 2ē 8ē атом ион +17Cl0 2ē 8ē 7ē +17Cl0 2ē 8ē 8ē атом ион

ИОНЫ (по составу) ПРОСТЫЕ Например: Cl- K+ СЛОЖНЫЕ Например: NO3- SO42-

Основные положения ТЭД 2. Причиной диссоциации электролита в водном растворе является его гидратация, т.е. взаимодействие электролита с молекулами воды и разрыв химической связи в нем.

ИОНЫ (по наличию водной оболочки) ГИДРАТИРОВАННЫЕ Например: В растворах и кристаллогидратах CuSO4 * 5H2O Na2SO4* 10H2O НЕГИДРАТИРОВАННЫЕ Например: В безводных солях Cu2+SO42- Na+NO3-

Основные положения ТЭД 3. Под действием электрического тока положительно заряженные ионы движутся к отрицательному полюсу источника тока – катоду, поэтому их называют катионами, а отрицательно заряженные ионы движутся к положительному полюсу источника тока – аноду, поэтому их называют анионами.

ИОНЫ (по знаку заряда) КАТИОНЫ положительно заряженные частицы АНИОН отрицательно заряженные частицы

Основные положения ТЭД 4. Электролитическая диссоциация – процесс обратимый для слабых электролитов. Наряду с процессом диссоциации протекает и обратный процесс – ассоциация (соединение ионов) HNO2 H+ + NO2-

Основные положения ТЭД 5. Не все электролиты в одинаковой мере диссоциируют на ионы.
ЭЛЕКТРОЛИТЫ (по степени диссоциации) СЛАБЫЕ СИЛЬНЫЕ

Основные положения ТЭД 6. Химические свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.

ЭЛЕКТРОЛИТЫ (по характеру образующихся ионов) КИСЛОТЫ ОСНОВАНИЯ СОЛИ

ЗАДАНИЕ Составьте возможные уравнения электролитической диссоциации веществ в водных растворах. 1) HCl 2) HNO3 3) Н2SiO3

ДОПИШИТЕ ОПРЕДЕЛЕНИЕ Кислоты – это электролиты, которые диссоциируют на катионы и анионы

КИСЛОТЫ электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. HCl = H+ + Cl- HNO3 = H+ + NO3-

Многоосновные кислоты диссоциируют ступенчато H3PO4 (фосфорная кислота) 1) Образование дигидрофосфат-ионов H3PO4 ↔ H+ + H2PO4- 2) Образование гидрофосфат-ионов H2PO4- ↔ H+ + HPO42- 3) Образование фосфат-ионов HPO42- ↔ H+ + PO43-

ЗАДАНИЕ Составьте возможные уравнения электролитической диссоциации веществ в водных растворах. 1) NaOH 2) KOH 3) Fe(OH)2

ДОПИШИТЕ ОПРЕДЕЛЕНИЕ Основания – это электролиты, которые диссоциируют на катионы и анионы

ОСНОВАНИЯ электролиты, которые при диссоциации образуют катионы металла и гидроксид-анионы. NaOH = Na+ + OH- KOH = K+ + OH-

Многокислотные основания диссоциируют ступенчато Ba(OH)2 (гидроксид бария) 1) Образование гидроксо-ионов бария Ba(OH)2 ↔ OH- + BaOH+ 2) Образование ионов бария BaOH+ ↔ Ba2+ + OH-

ЗАДАНИЕ Составьте возможные уравнения электролитической диссоциации веществ в водных растворах. 1) NaCl 2) KNO3 3) BaSO4

ДОПИШИТЕ ОПРЕДЕЛЕНИЕ Cоли – это электролиты, которые диссоциируют на катионы и анионы

СОЛИ электролиты, которые при диссоциации образуют катионы металла (или аммония NH4) и анионы кислотных остатков. K3PO4 = 3K+ + PO43- NH4Cl = NH4+ + Cl-

ПРОВЕРЬ СВОИ ЗНАНИЯ Пользуясь таблицей растворимости, приведите примеры трех веществ, которые в растворах образуют сульфат-ионы. Запишите уравнения электролитической диссоциации этих веществ. 1) H2SO4 ↔ H+ + HSO4- 2) HSO4- ↔ H+ + SO42-

Разложение хлорида меди электрическим током

ОЦЕНКИ ЗА УРОК

ДОМАШНЕЕ ЗАДАНИЕ § 36, положения ТЭД записать в тетрадь, выучить наизусть Определения кислот, оснований, солей выучить наизусть Задание №5, страница 203 (письменно)