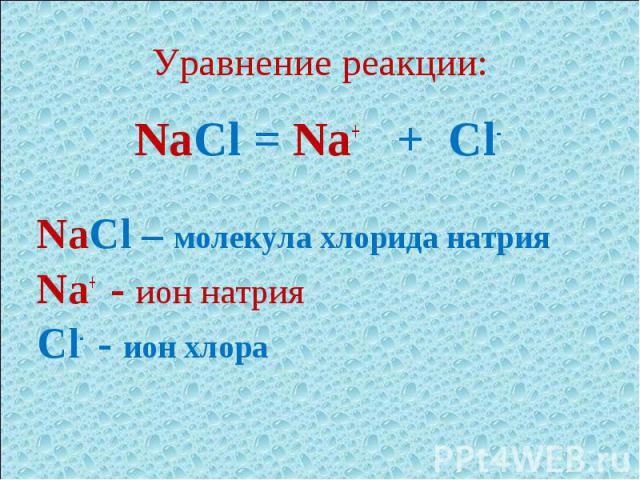Презентация на тему: Электролитическая диссоциация 9 класс

Электролитическая диссоциация Выполнила учитель химии и экологии МОУ «СОШ с.Усть-Курдюм» Филимонова Ирина Вячеславовна

Вещества ЭЛЕКТРОЛИТЫ НЕЭЛЕКТРОЛИТЫЭлектролиты – вещества, растворы и расплавы которых проводят электрический ток Неэлектролиты – вещества, растворы и расплавы которых не проводят электрический ток.

Почему растворы электролитов проводят электрический ток? Сванте Аррениус(1859-1927) Создал теорию электролитической диссоциации. За исследования в области электролитов был удостоен Нобелевской премии в 1903 г.

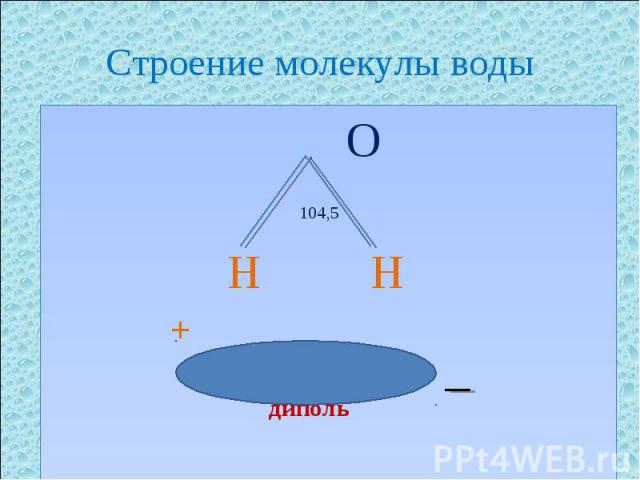
Строение молекулы воды

Электролитическая диссоциация – процесс распада электролита на ионы при растворении его в воде или расплавлении.

Легче всего диссоциируют вещества с ионной и ковалентной полярной связью:Кислоты : HCl, H2SO4, HF, HNO3Основания: NaOH, Ba(OH)2, KOHСоли : NaCl, CuSO4, KNO3

Последовательность процессов, происходящих при электролитической диссоциации: Ориентация молекул – диполей воды около ионов;Гидратация (взаимодействие) молекул воды с противоположно заряженными ионами поверхностного слоя кристалла;Диссоциация (распад) кристалла электролита на гидратированные ионы
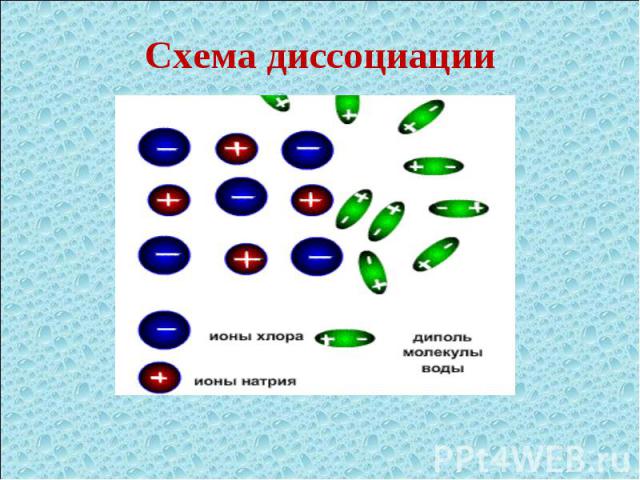
Схема диссоциации
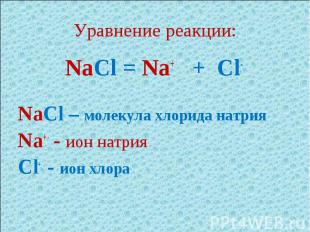
Уравнение реакции: NaCl = Na+ + Cl-NaCl – молекула хлорида натрияNa+ - ион натрияCl- - ион хлора

Степень диссоциации – это отношение числа частиц, распавшихся на ионы (Nд), к общему числу растворенных частиц (Nр) ά – степень диссоциацииNд - число частиц, распавшихся на ионыNр - общее число растворенных частиц

Степень диссоциации выражают в долях или процентах. При ά = 0 диссоциация отсутствует При ά = 1 или 100% электролит полностью распадается на ионыПо степени электролитической диссоциации электролиты делят сильные слабые

Электролиты Сильныевсе растворимые соли;сильные кислотыH2SO4, HCl, HNO3все щелочиNaOH, KOHСлабыеслабые кислотыH2S, H2CO3, HNO2водный раствор аммиакаNH3*H2Oорганические вещества

Домашнее задание § 35, упр. 1-5