Презентация на тему: Электролитическая диссоциация 8 класс

Электролитическая диссоциацияУчебная презентация для 8 класса

Теория электролитической диссоциации была создана шведским ученым С. Аррениусом в 1883 году Механизм электролитической диссоциации был подробно изучен русским ученым И. А. Каблуковым
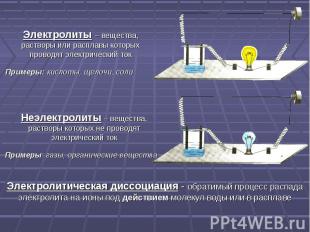
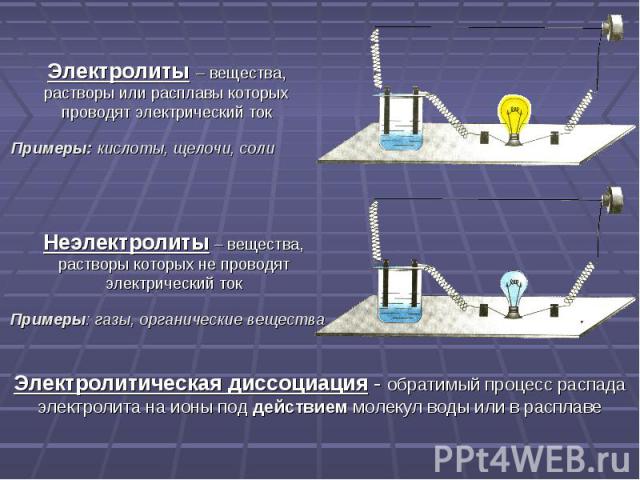
Электролиты – вещества, растворы или расплавы которых проводят электрический ток Примеры: кислоты, щелочи, соли Неэлектролиты – вещества, растворы которых не проводят электрический ток Электролитическая диссоциация - обратимый процесс распада электролита на ионы под действием молекул воды или в расплаве

строение молекулы воды Молекулы воды представляют собой диполи, так как атомы водорода расположены под углом 104,5 градуса, благодаря чему молекула имеет угловую форму
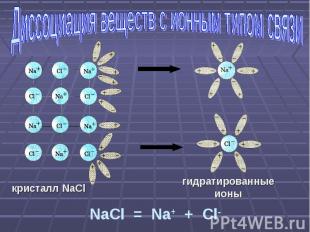
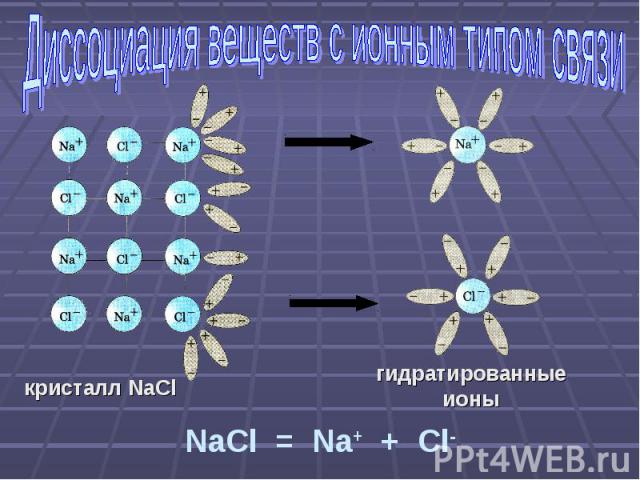
Диссоциация веществ с ионным типом связи кристалл NaCl NaCl = Na+ + Cl-

Механизм электролитической диссоциации веществ с ионным типом связи Ориентация молекул – диполей воды около ионов кристалла Взаимодействие молекул воды с противоположно заряженными ионами поверхностного слоя кристалла (гидратация) Распад кристалла электролита на гидратированные ионы (диссоциация)
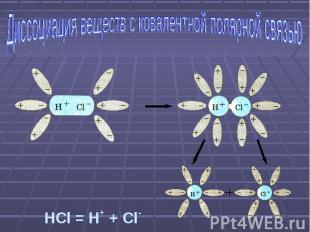
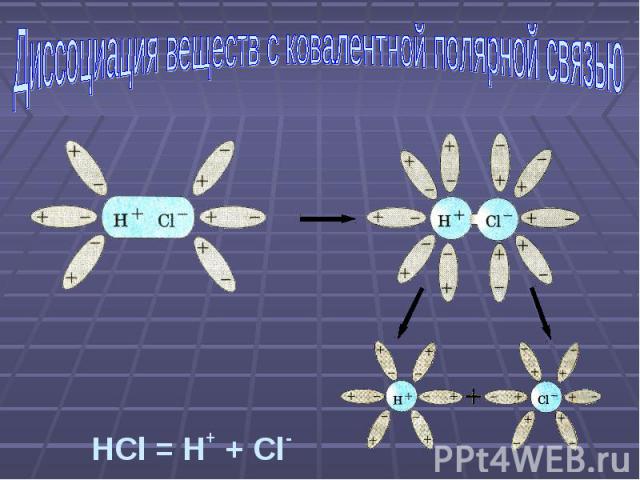
Диссоциация веществ с ковалентной полярной связью HCl = H+ + Cl-

Механизм электролитической диссоциации веществ с ковалентной полярной связью Ориентация молекул воды вокруг полюсов молекулы электролитаВзаимодействие молекул воды с противоположно заряженными ионами поверхностного слоя кристалла (гидратация) Превращение ковалентной полярной связи в ионную (ионизация молекул электролита) Распад молекул электролита на гидратированные ионы (диссоциация)

Степень электролитической диссоциации – отношение числа частиц, распавшихся на ионы, к общему числу растворенных частиц > 30 %сильные 2 − 30 %средней силы < 2 %слабые Соли, щелочи, кислоты H2SO4, HNO3, HCl, HBr, HI H2O, NH4OH, Me(OH)n , H2CO3, H2SiO3, H2S, CH3COOHСтепень электролитическойдиссоциации зависит от

Основные положения теории электролитической диссоциации При растворении в воде электролиты диссоциируют на положительные и отрицательные ионыПричиной диссоциации электролита в водном растворе является его гидратация, то есть взаимодействие электролита с молекулами воды и разрыв химической связи в немПод действием электрического тока положительно заряженные ионы движутся к отрицательному полюсу источника тока – катоду, их называют катионами; а отрицательно заряженные ионы движутся к положительному полюсу источника тока – аноду, их называют анионамиЭлектролитическая диссоциация – процесс обратимый для слабых электролитовХимические свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации

Кислоты – электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка HCl H+ + Cl- HNO3 H+ + NO3− H2SO4 2H+ + SO42− Слабые многоосновные кислоты диссоциируют ступенчато: H2SO3 H+ + HSO3− HSO3− H+ + SO32− Общие характерные свойства кислот обусловлены присутствием катионов водорода

Основания – электролиты, которые при диссоциации образуют катионы металла и анионы гидроксогрупп ОН- NaOH = Na+ + OH- КОН = К+ + ОН- Са(ОН)2 = Са2+ + 2ОН- Слабые многокислотные основания диссоциируют ступенчато. Fe(OH)2 FeOH+ + OH- FeOH+ Fe2+ + OH- Общие свойства оснований обусловлены присутствием гидроксид-ионов ОН-

Средние соли – сильные электролиты, которые при диссоциации образуют катионы металла (или аммония NH4+) и анионы кислотных остатков Кислые соли – электролиты, диссоциирующие на катион металла и сложный анион, в состав которого входят атомы водорода и кислотный остаток Основные соли – электролиты, которые при диссоциации образуют анионы кислотного остатка и сложные катионы, состоящие из атомов металла и гидроксогрупп ОН−

Проверьте свои знания Вещества, растворы которых проводят электрический ток.Процесс распада электролита на ионы.Положительно заряженные ионы. Отрицательно заряженные ионыЭлектролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка.Электролиты, которые при диссоциации образуют катионы металла и анионы гидроксогрупп ОН−. Электролиты, которые при диссоциации образуют катионы металла и анионы кислотных остатков.Количественная характеристика электролитической диссоциацииМолекулы, имеющие два электрических заряда, равных по величине, но противоположных по знаку, и расположенных на некотором расстоянии друг от другаАвтор теории электролитической диссоциации.

Ответы 1. Электролиты2. Электролитическая диссоциация3. Катионы 4. Анионы 5. Кислоты 6. Основания7. Соли8. Степень электролитической диссоциации9. Диполи 10. С. Аррениус

http://www.catalogmineralov.ru – сайт содержит каталог минералов, большую коллекцию фотографий и описание минералов.http://www.elementy.ru – сайт « Элементы большой науки», содержит каталоги и статьи научно-популярных журналов «Химия и жизнь», « Наука и жизнь», «Природа» и др.http://www.ovitanah.com - сайт посвящен витаминам и микроэлементам, содержит интересную информацию.http://www.alhimik.ru – сайт «Алхимик» содержит самую разнообразную информацию по химии.