Презентация на тему: Технология подготовки учащихся "ЕГЭ по химии"

ЕГЭ по химии Технология подготовки учащихся
www.fipi.ru
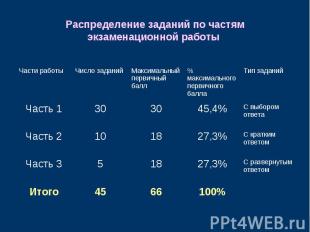
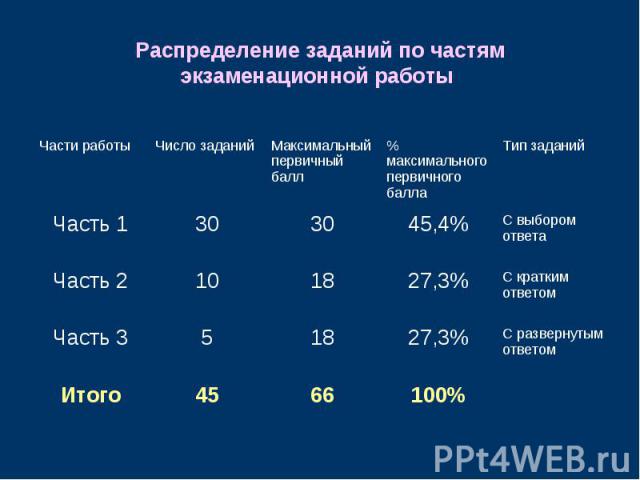
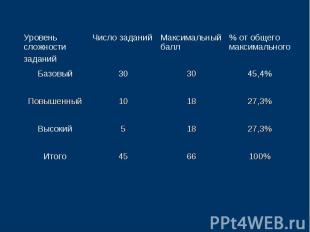
Распределение заданий по частям экзаменационной работы

Структура КИМ ЕГЭA1Строение атомаA2Периодический закон и ПСХЭA3 Металлы главных и побочных подгруппA4 Неметаллы, общая характеристикаA5 Химическая связь

A6 Электроотрицательность. Степени окисленияA7 Кристаллические решеткиA8 Классификация веществ, номенклатураA9 - A12 Химические свойства простых веществ и классов неорганических соединенийA13Генетическая связь между классами неорганических веществ

A14 Изомеры и гомологи - и -Связи. Типы гибридизацииA15-A17 Химические свойства классов органических веществ A18 -20Способы получения органических веществ, генетическая связь между углеводородами и кислородсодержащими

A21 Классификация химических реакцийА22 Скорость химических реакцийA23 Обратимые и необратимые реакцииA24 Электролитическая диссоциацияA25 Реакции ионного обменаA26 Гидролиз солей

A27 ОВРA28 Вещества в нашей жизни. Применение веществ. Распознавание веществA29 Химия в промышленности и в экологииA30 Термохимический расчет или расчет объемных отношений

Часть BB1 Классификация и номенклатура веществB2 Степени окисления. ОВРB3 ЭлектролизB4 ГидролизB5 Химические свойства классов неорганических веществ

Часть BB6 УглеводородыB7 Кислородсодержащие орг.веществаB8 Азотсодержащие орг.веществаB9 ЗадачаB10 Задача

Используя метод электронного баланса, составьте уравнение реакции:Si + HNO3 + HF = = H2SiF6 + NO + … Определите окислитель и восстановитель.

Даны вещества:серасероводородазотная кислота (конц.) серная кислота (конц.)Приведите уравнения четырех возможных реакций между этими веществами.

Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:

Какой объем хлора (н.у.) выделится, если к 200 мл 35%-ной соляной кислоты (плотность 1,17 г/мл) добавить при нагревании 26,1 г оксида марганца(IV)?Какая масса гидроксида натрия в холодном растворе прореагирует с таким количеством хлора?

При взаимодействии одного и того же количества алкена с различными галогеноводородами образуется соответственно 7,85 г хлорпроизводного или 12,3 г бромпроизводного. Определите молекулярную формулу алкена.

Спасибо за внимание!