Презентация на тему: Биотрансформация чужеродных соединений в организме

ЛЕКЦИЯ № 5. Биотрансформация чужеродных соединений в организме. Этапы и основные пути биотрансформации. Факторы, влияющие на метаболизм чужеродных соединений. Метаболиты и токсичность. Представление о вторичном метаболизме. Экскреция чужеродных соединений и их метаболитов. Биотрансформация — метаболическое превращение эндогенных и экзогенных химических веществ в более полярные (гидрофильные) соединения. Фазы биотрансформации Реакции 1-й фазы Реакции 2-й фазы (реакции синтеза) гидролиз, восстановление, окисление. -глюкуронирование, -сульфатирование, -ацетилирование, -метилирование, конъюгация (соединение) с: а) глутатионом (синтез меркаптуровой кислоты) б) аминокислотами (глицином, таурином и глутаминовой кислотой).

Основные пути биотрансформации чужеродных соединений. 1. Окисление: а) микросомальное – алифатичекое или ароматическое гидроксилирование, – эпоксидирование, – N-гидроксилирование, – N, S-окисление, – дезалкилирование, – дезаминирование, – десульфирование; б) немикросомальное – окислительное дезаминирование, – окисление спиртов, альдегидов, – ароматизация алициклических соединений. 2. Восстановление: а) восстановление нитросоединений, азотсоединений микросомальными ферментами; б) микросомальное восстановительное галогенирование; в) немикросоальное восстановление. 3. Гидролиз с участием микросомальных и немикросомальных ферментов. 4. Синтез (реакции коньюгирования): а) образование коньюгатов с глюкуроновой кислотой; б) образование сложных эфиров с серной и фосфорной кислотами; в) метилирование; г) ацетилирование; д) пептидная коньюгация.
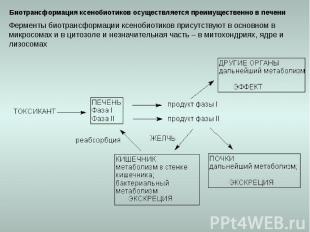
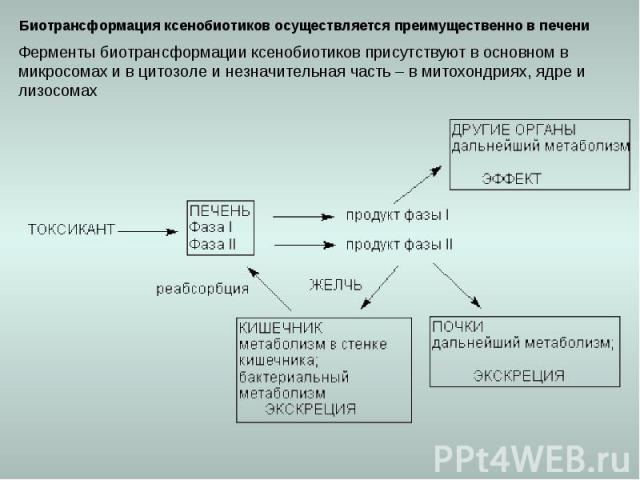
Биотрансформация ксенобиотиков осуществляется преимущественно в печени Ферменты биотрансформации ксенобиотиков присутствуют в основном в микросомах и в цитозоле и незначительная часть – в митохондриях, ядре и лизосомах

Ферментативные реакции 1-й фазы биотрансформации ксенобиотиков карбоксилэстераза, ацетилхолинэстераза псевдохолинэстераза эпоксидная гидролаза 1. Гидролиз при биотрансформации X = OR‘, SR‘, Cl, NR‘2 параоксаназа амидная связь между аминокислотами в пептидах, рекомбинантных пептидных гормонах, факторах роста, цитокинах, растворимых рецепторов и моноклональных антител. эфиры карбоновых кислот, амидов и тиоэфиров эфиры фосфорной кислоты пептидазы присоединение воды к эпоксидам алкенов и оксидам аренов l фаза метаболизма - этап биотрансформации, в ходе которого к молекуле соединения либо присоединяются полярные функциональные группы, либо осуществляется экспрессия таких групп, находящихся в субстрате в скрытой форме

2. Восстановление при биотрансформации Некоторые металлы альдегиды, кетоны, дисульфиды, сульфоксиды, хиноны, алкены, азо- и нитросоединеня Коферменты — никотинамидадениндинуклеотид (НАД+/НАДН, НАДФ+/НАДФН) флавинадениндинуклеотид (ФАД/ФАДН2). Восстановление азо- и нитросоединений - цитохром Р450 НАДФН-хинон оксидоредуктазы реакция ингибируются кислородом
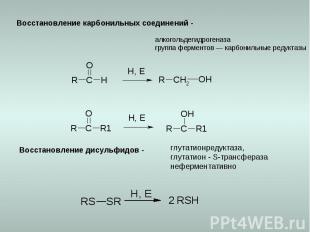
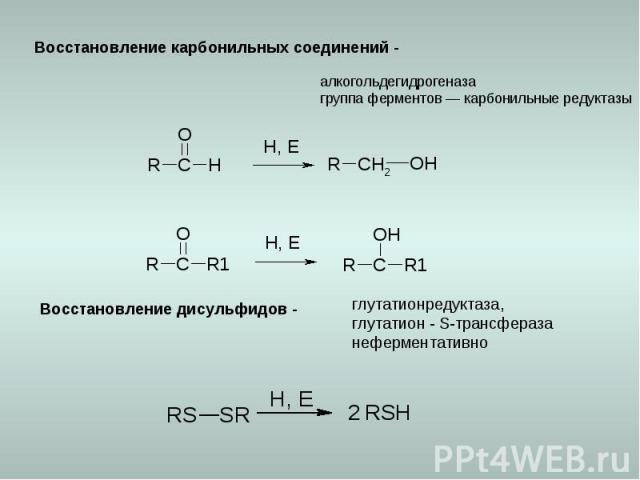
Восстановление карбонильных соединений - алкогольдегидрогеназа группа ферментов — карбонильные редуктазы Восстановление дисульфидов - глутатионредуктаза, глутатион - S-трансфераза неферментативно
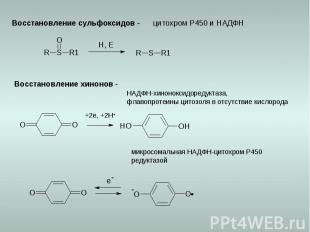
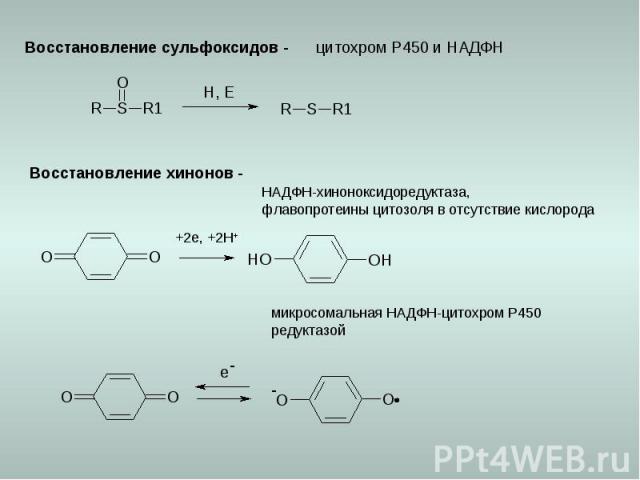
Восстановление сульфоксидов - цитохром Р450 и НАДФН Восстановление хинонов - +2e, +2H+ НАДФН-хиноноксидоредуктаза, флавопротеины цитозоля в отсутствие кислорода микросомальная НАДФН-цитохром Р450 редуктазой
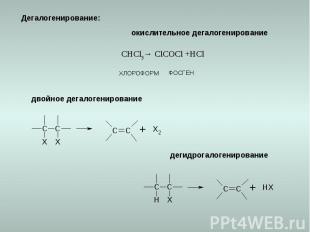
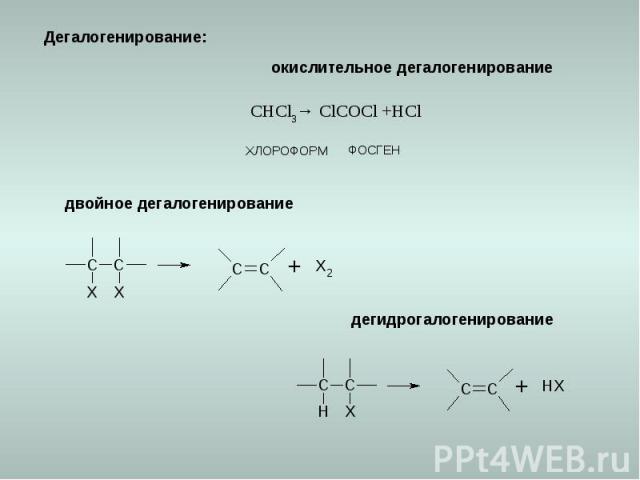
Дегалогенирование: окислительное дегалогенирование двойное дегалогенирование дегидрогалогенирование ХЛОРОФОРМ ФОСГЕН CHCl3→ ClCOCl +HCl
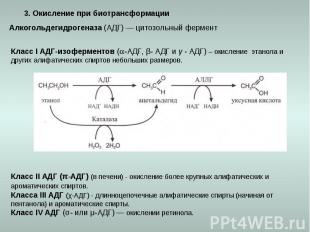
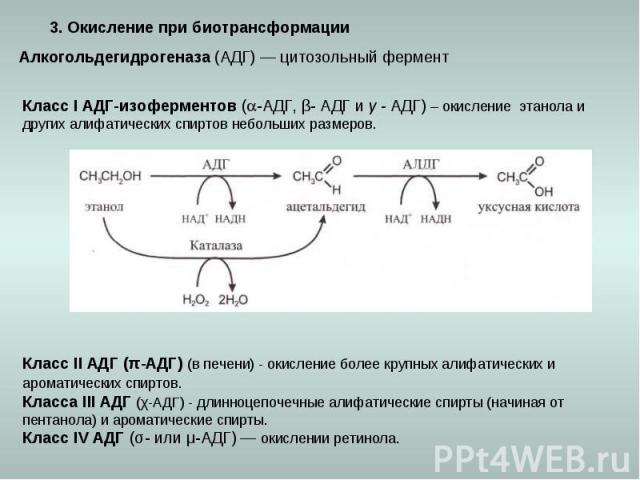
3. Окисление при биотрансформации Алкогольдегидрогеназа (АДГ) — цитозольный фермент Класс I АДГ-изоферментов (-АДГ, β- АДГ и γ - АДГ) – окисление этанола и других алифатических спиртов небольших размеров. Класс II АДГ (π-АДГ) (в печени) - окисление более крупных алифатических и ароматических спиртов. Класса III АДГ (χ-АДГ) - длинноцепочечные алифатические спирты (начиная от пентанола) и ароматические спирты. Класс IV АДГ (σ- или μ-АДГ) — окислении ретинола.

Альдегид-дегидрогеназа (АЛДГ) - окислении альдегидов до карбоновых кислот (кофактор НАД+). Дигидродиолдегидрогеназа - окисление полициклических ароматических углеводородов. Молибденовые гидроксилазы – альдегидоксидаза и ксантиндегидрогеназа / ксантиноксидаза, сульфитоксидаза - окисляет токсичный сульфит до относительно безопасного сульфата. Ксантиндегидрогеназа (XD) и ксантиноксидаза (ХО) — участвуют в процессах, связанных с оксидативным стрессом, пероксидном окислении липидов. Альдегидоксидаза - пероксидное окисление липидов, катаболизм биогенных аминов и катехоламинов.

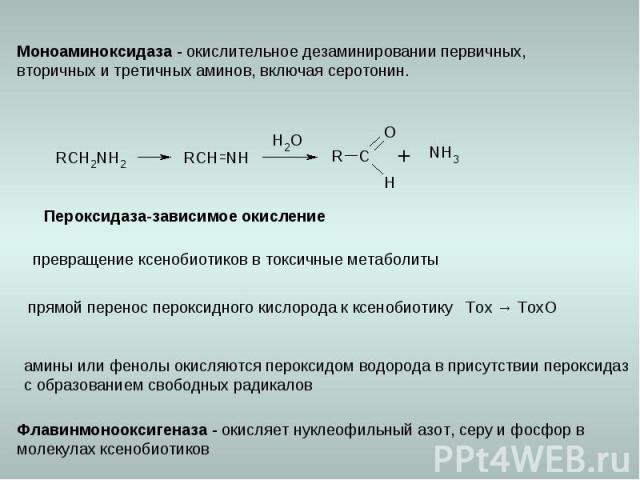
Пероксидаза-зависимое окисление превращение ксенобиотиков в токсичные метаболиты прямой перенос пероксидного кислорода к ксенобиотику Тох → ТохО амины или фенолы окисляются пероксидом водорода в присутствии пероксидаз с образованием свободных радикалов Флавинмонооксигеназа - окисляет нуклеофильный азот, серу и фосфор в молекулах ксенобиотиков Моноаминоксидаза - окислительное дезаминировании первичных, вторичных и третичных аминов, включая серотонин.

Цитохром Р450 катализирует реакции окисления: -гидроксилирование алифатических и ароматических углеводородов; эпоксидирование двойной связи; окисление гетероатомов (О-, S-, N-, Si-) N-гидроксилирование; деалкилирование гетероатомов (О-, S-, N-, Si-), окислительный перенос группы; разрыв сложноэфирной связи; дегидрирование. НАДФН НАДФ
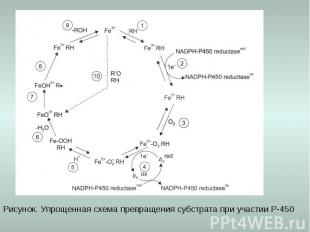
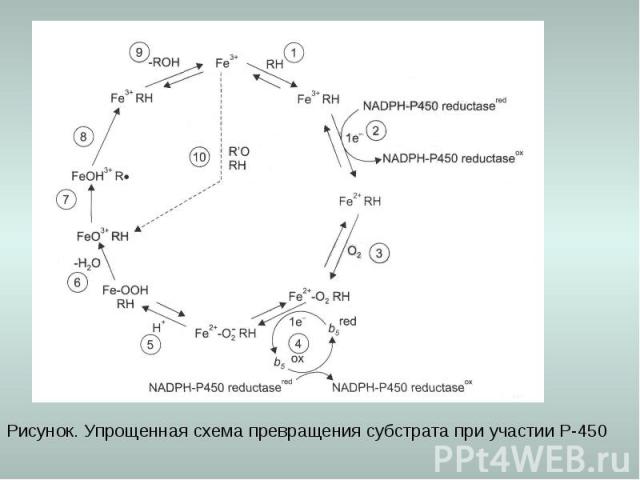
Рисунок. Упрощенная схема превращения субстрата при участии Р-450
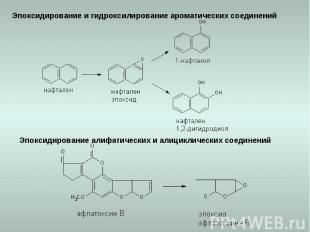
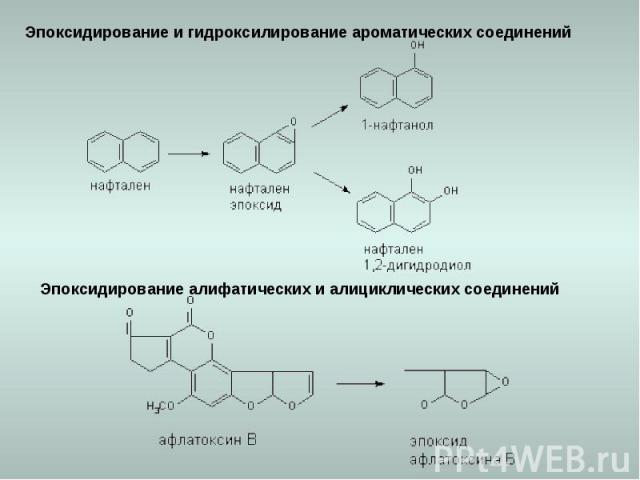
Эпоксидирование и гидроксилирование ароматических соединений Эпоксидирование алифатических и алициклических соединений
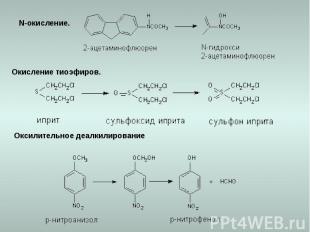
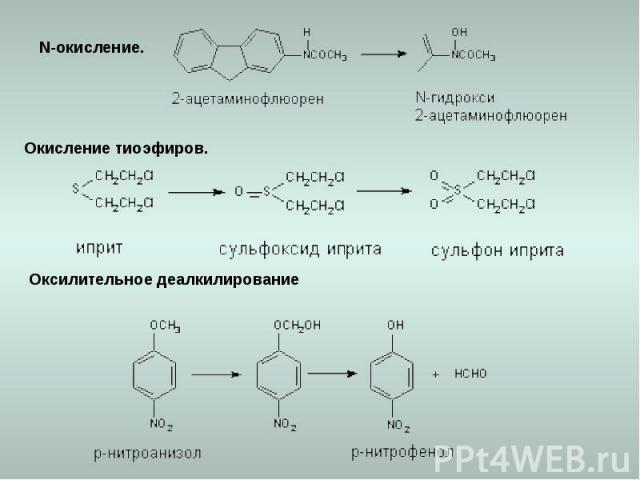
N-окисление. Оксилительное деалкилирование Окисление тиоэфиров.
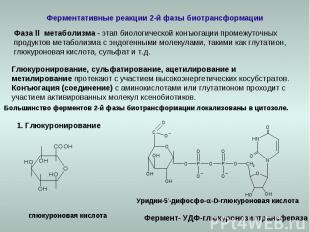
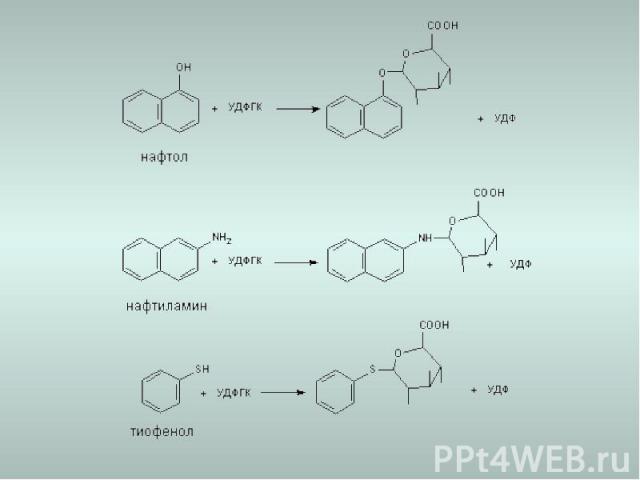
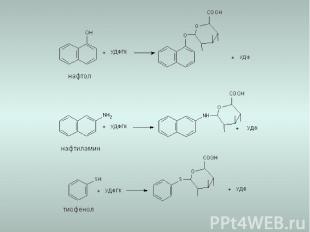
Ферментативные реакции 2-й фазы биотрансформации Фаза ll метаболизма - этап биологической конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, такими как глутатион, глюкуроновая кислота, сульфат и т.д. Глюкуронирование, сульфатирование, ацетилирование и метилирование протекают с участием высокоэнергетических косубстратов. Конъюгация (соединение) с аминокислотами или глутатионом проходит с участием активированных молекул ксенобиотиков. Большинство ферментов 2-й фазы биотрансформации локализованы в цитозоле. 1. Глюкуронирование Уридин-5‘-дифосфо--D-глюкуроновая кислота глюкуроновая кислота Фермент- УДФ-глюкуронозилтрансфераза
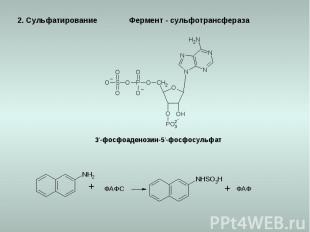
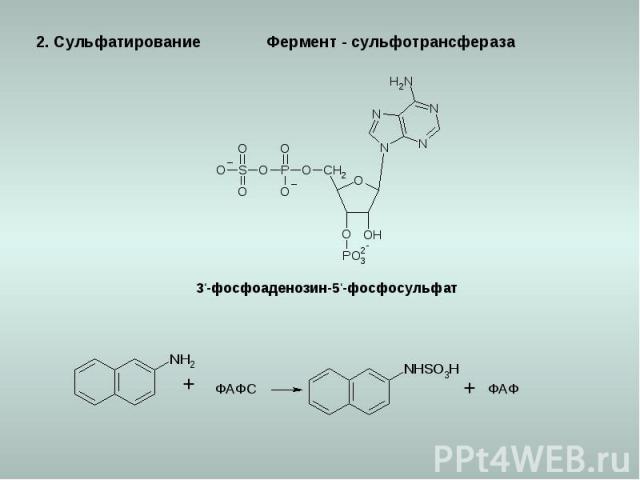
2. Сульфатирование 3‘-фосфоаденозин-5‘-фосфосульфат ФАФС ФАФ Фермент - сульфотрансфераза
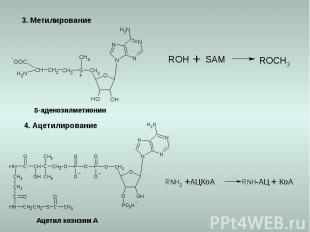
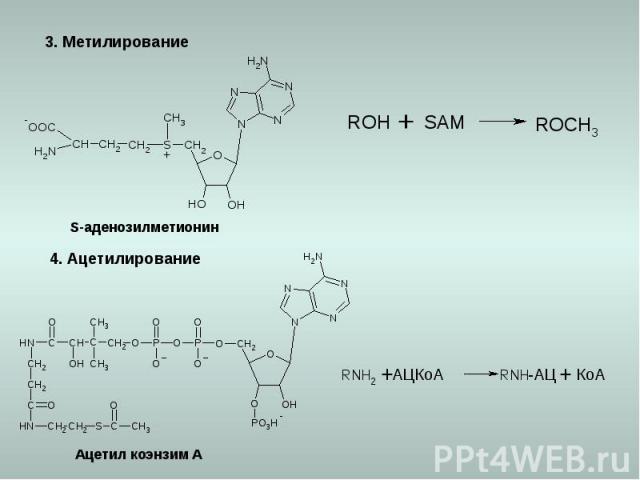
3. Метилирование 4. Ацетилирование S-аденозилметионин Ацетил коэнзим А КоА АЦКоА -АЦ
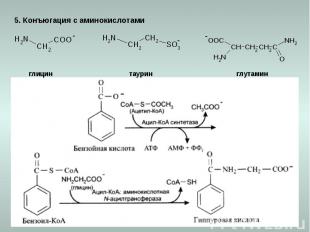
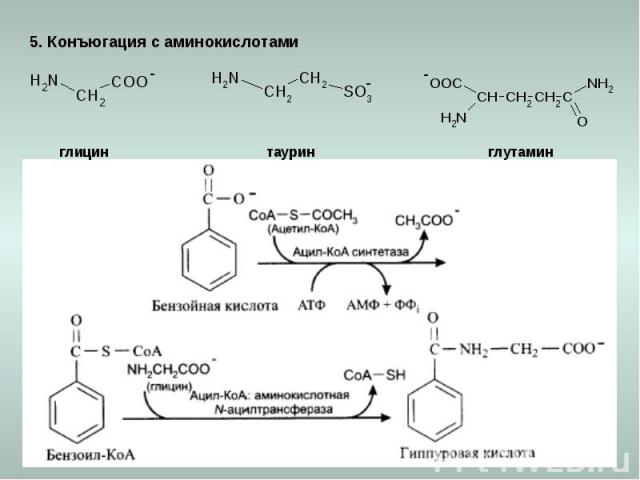
5. Конъюгация с аминокислотами глицин таурин глутамин
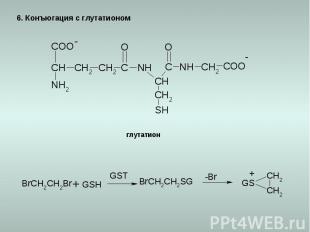
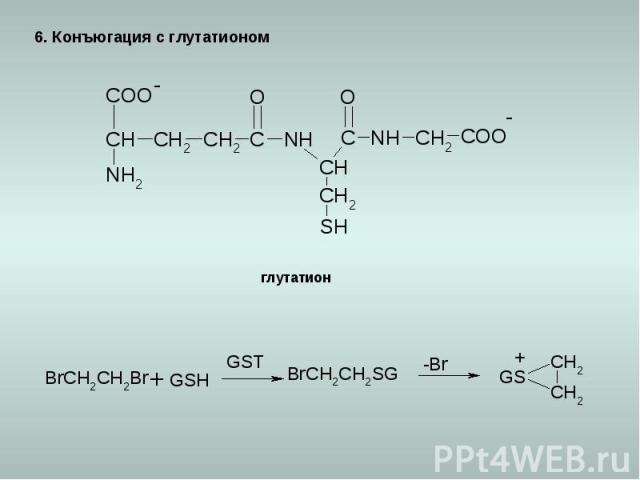
6. Конъюгация с глутатионом глутатион
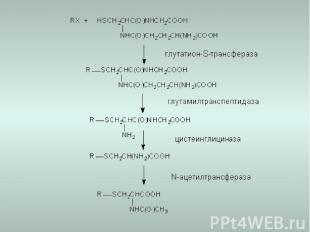

Факторы, влияющие на метаболизм чужеродных соединений. Генетические факторы и внутривидовые различия (возможны генетические дефекты ферментов, их изучением занимается фармакогенетика). 2. Физиологические: -возраст и развитие ферментных систем; -половые различия; -гормональный фон; -беременность; -питание; -патологические состояния, заболевания; -длительное применение лекарств. 3. Факторы окружающей среды: -стресс; -ионизирующая радиация; -стимулирование метаболизма чужеродными соединениями; -ингибирование метаболизма чужеродными соединениями. Вторичный метаболизм - посмертные метаболические процессы