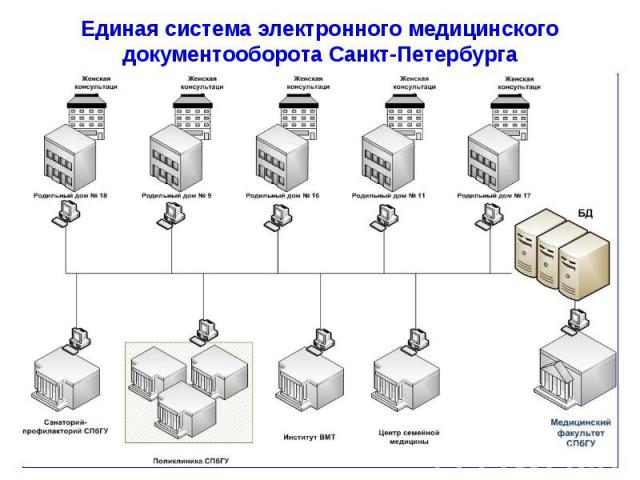
Презентация на тему: Лаборатория клинической фармакологии медицинского лечебно-профилактического учебно-научный центра Санкт-Петербургского государственного университета. Планируемая деятельность и перспективы развития

Лаборатория клинической фармакологии медицинского лечебно-профилактического учебно-научный центра Санкт-Петербургского государственного университета. Планируемая деятельность и перспективы развития.

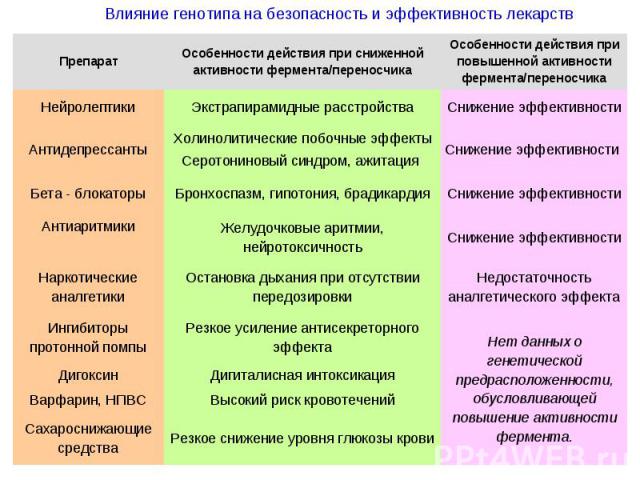
ПРЕДПОСЫЛКИ ДЛЯ ОРГАНИЗАЦИИ ЛАБОРАТОРИИ C помощью клинической фармакологии, возможно, оптимизировать использование лекарств на основе анализа качества, клинической эффективности, безопасности и экономической целесообразности (“четыре барьера”) Необходимость адаптации в регионе федеральных клинико-экономических стандартов оказания медицинской помощи Проблема био- и терапевтической эквивалентности воспроизведенных лекарств Сложности, возникающие у практикующего доктора при систематизации информационного потока по лекарственным средствам

Проведение подобных исследований должно осуществляться группами подготовленных специалистов экспертов в области клинической-фармакологии, которые должны быть аккумулированы в едином научно-методическом центре Такого центра в Санкт-Петербурге и Северо-Западном регионе нет


Общее положение Лаборатория клинической фармакологии является учебно-научно-исследовательским подразделением, входящим в состав медицинского факультета СПбГУ Генеральный партнер - СПбГМА им. И.И.Мечникова

1. развитие научно-практического сотрудничества с органами практического здравоохранения; научными учреждениями и производственными организациями 2. расширение международного научного сотрудничества с целью вхождения в международную систему клинико-фармакологических исследований и образования совместной исследовательской работы
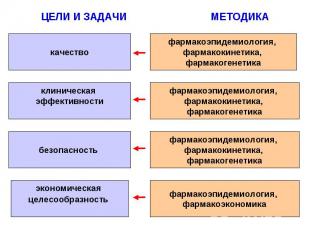
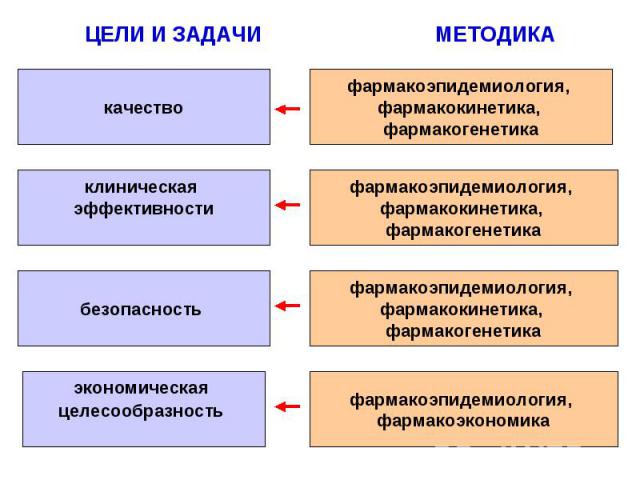
ЦЕЛИ И ЗАДАЧИ МЕТОДИКА

ВИДЫ НАУЧНО-ПРАКТИЧЕСКОЙ ДЕЯТЕЛЬНОСТИ Фармакоэпидемиологические и клинико-экономические исследования; Фармакогенетические исследования; Фармакокинетические исследования; Диагностика и регистрация нежелательных явлений лекарств; Информационный центр по клинической фармакологии.

Эксперты по основным направлениям работы лаборатории А.С. Колбин, Андреев Б.В., Бурбелло А.Т., Бабак С.В., Горячкина К.А., Климко Н.Н., Мазуров В.И., Симаненков В.И., Курылев А.А., Виленская Е.Г.

Сотрудничество Комитет по Здравоохранению Правительства Санкт-Петербурга Федеральный центр мониторинга безопасности лекарственных средств (Фармконадзор) Общество клинических фармакологов Санкт-Петербурга Городской онкодиспансер ЗАО “Империя – Фарма Холдинг”

Планируемое сотрудничество Санкт-Петербургская медицинская академия последипломного образования Санкт-Петербургская государственная педиатрическая медицинская академия Санкт-Петербургский государственный медицинский университет им. акад.И.П.Павлова Военно-медицинская академия им. С.М.Кирова

Планируемое международное сотрудничество Каролинский институт Отделение клинической фармакологии Каролинского университетского госпиталя

Потребители работ Практикующие врачи Административные органы здравоохранения регионального или федерального уровня Лечебно-профилактические учреждения Разработчики и производители лекарственных средств Дистрибьюторы фармацевтической продукции

ЦЕНТРАЛИЗОВАННАЯ ЗАЯВКА НА ЛЕКАРСТВЕННЫЕ СРЕДСТВА В САНКТ-ПЕТЕРБУРГЕ: ФАРМАКОЭПИДЕМИОЛОГИЧЕСКИЙ АНАЛИЗ

“Доказательная медицина” в крупном мегаполисе 80 ЛПУ 6 высших медицинских учреждений более 10 НИИ в каждом ЛПУ от 10 до 20 клинических баз кафедр научные группы, реализующие свои взгляды через учебники, методические рекомендации, статьи, собственный клинический опыт гипертрофированная роль экспертов (на первом месте не данные клинических исследований, а а авторитарное мнение эксперта)


1. Разработать систему сбора данных об использовании лекарств в стационарах 2. Провести качественную и количественную оценку лекарственных средств и лекарственных препаратов используемых в стационара Санкт-Петербурга
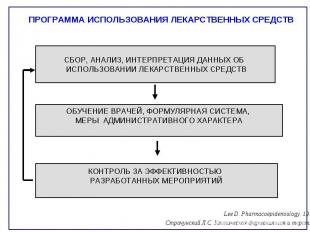
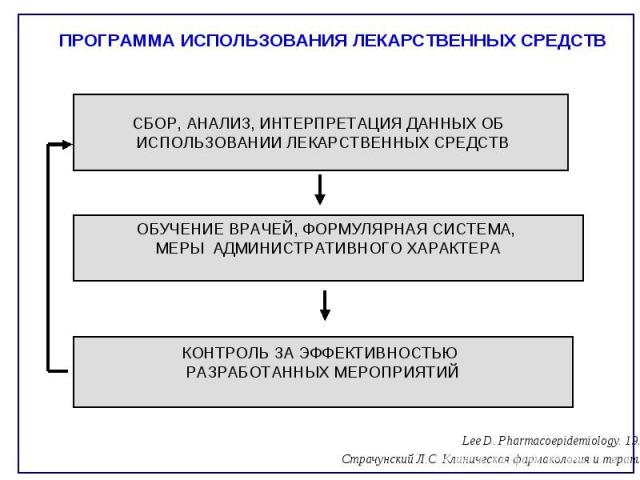
ПРОГРАММА ИСПОЛЬЗОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ

I. Первый этап – на основании таблицы “валидности” все ЛС в заявки были оценены по 15-ти фармакоэпидемиологическим показателям, с присвоением баллов II. Второй этап - заключение экспертов по каждому ЛС на основании суммы баллов III. Третий этап - модифицированная техника Дельфи, с целью достижения согласия между экспертами IV. Четвертый этап - АВС анализ V. Совмещение фармакоэпидемиологических данных и АВС-анализа VI. Окончательное заключение с рекомендациями

на основании данных 3 и 4 квартала централизованной заявки на основании данных 3 и 4 квартала централизованной заявки

Результаты создана база данных c критериями оценки 747 ЛС (МНН и НН) 2146 ЛП (торговые названия) 80 ЛПУ Санкт-Петербурга

Результаты На основании анализа базы централизованной заявки по 15-ти показателям предложены методы выбора лекарственных средств и лекарственных препаратов с позиций “качество – безопасность – терапевтическая эффективность – стоимость”.

Нет данных по терапевтической эквивалентности Крайне ограничены данные по биоэквивалентности Отсутствие данных о соответствии GMP, прежде всего у российских производителей Нет данных по ДДД - анализу Ограничены данные по заболеваемости

Впервые Впервые был проведен количественный и качественный анализ централизованной заявки на ЛС стационаров Санкт-Петербурга.

Утверждены Комитетом по Здравоохранению Методические рекомендации для формирования заявки на лекарственные средства лечебно-профилактических учреждений Санкт-Петербурга подведомственных Комитету по Здравоохранению (для организаторов здравоохранения, клинических фармакологов, провизоров и врачей)

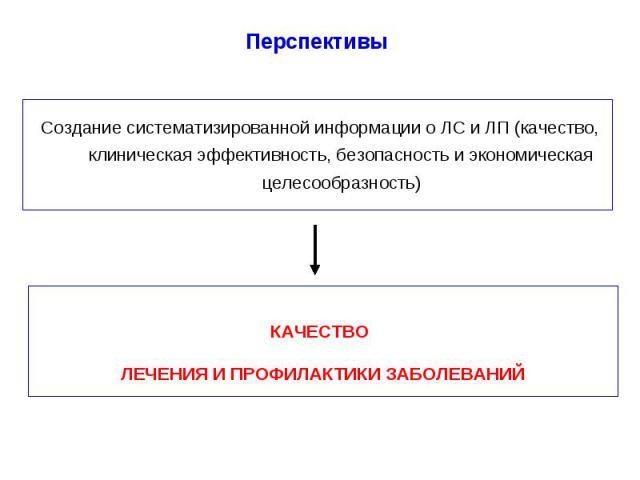
Перспективы Создание систематизированной информации о ЛС и ЛП (качество, клиническая эффективность, безопасность и экономическая целесообразность)

Перспективы Создание систематизированной информации о ЛС и ЛП (качество, клиническая эффективность, безопасность и экономическая целесообразность) Позволит Проводить фармакоэкономические исследования Оценить заболеваемость в стационарах с проведением ДДД - анализа Составить списки ЛС, к которым привержены врачи и / или пациенты Создать информационный поток для формирования городского формуляра

Перспективы Создание систематизированной информации о ЛС и ЛП (качество, клиническая эффективность, безопасность и экономическая целесообразность) Экономия денежных средств на основе выявления наиболее затратных и наименее клинически целесообразных технологий использования лекарств

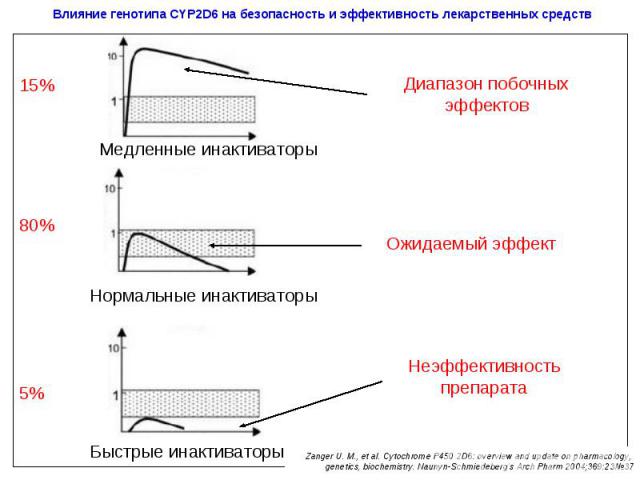
Фармакогенетические исследования выявление причин, по которым пациенты неадекватно реагируют на лекарственную терапию прогноз риска развития нежелательных явлений индивидуальный подбор фармакотерапии качество фармакотерапии создание базы данных
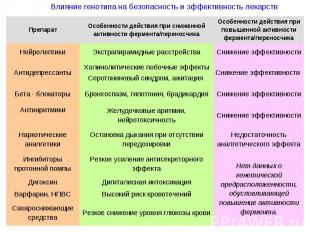
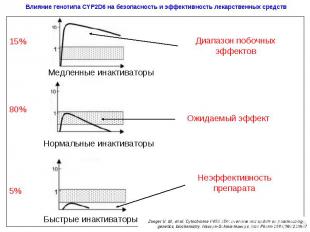

Фармакогенетические исследования

Фармакогенетические исследования амплификатор в реальном времени Stratagene Mx3000 планируемое начало работ – сентябрь 2008 года.

Фармакокинетические исследования необходимость контроля и полноценного обеспечения эффективности и безопасности фармакотерапии необходимость независимых исследований на биоэквивалентность ЛС

Фармакокинетические исследования Анализ концентраций ЛС в биологических образцах при использовании лекарств с узким терапевтическим интервалом Анализ концентраций ЛС при подозрении на токсическое воздействие или неэффективность терапии Экспертная оценка полученных результатов, клинические рекомендации Планирование и проведение клинических исследований по изучению фармакокинетики новых или воспроизведенных ЛС

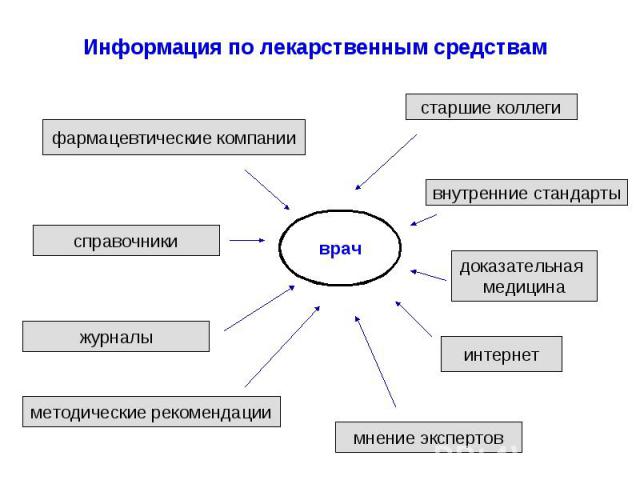
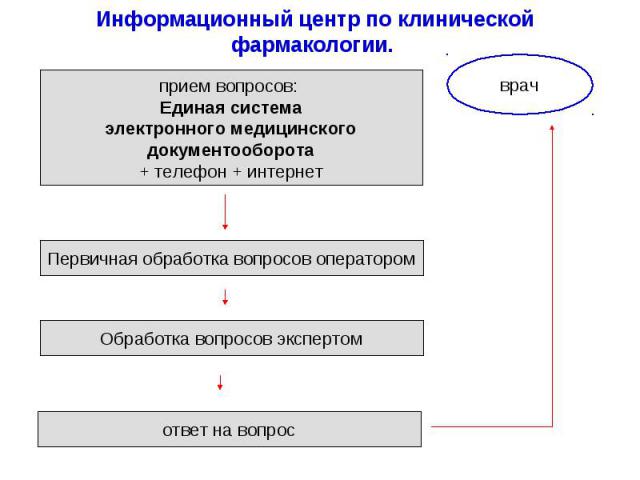
Информационный центр по клинической фармакологии. врачи повсеместно нуждаются в информации об особенностях применения ЛС международный опыт работы подобных центров показал, что предоставляемая ими информация пользуется возрастающим спросом среди врачей
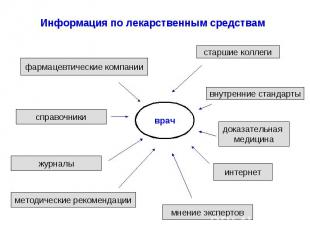
Информация по лекарственным средствам
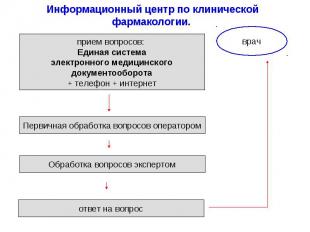
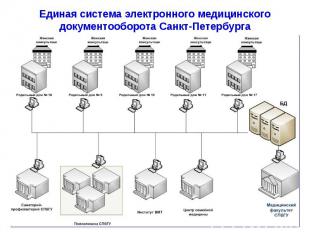

Информационный центр по клинической фармакологии. Создание базы данных наиболее часто задаваемых вопросов Ситуационная оценка Разработка методических рекомендаций и ситуационных задач по данным проблемам Разработка методических рекомендаций и ситуационных задач по данным проблемам для студентов