Презентация на тему: Инновационные подходы к комплексной терапии больных туберкулезом. Регуляторы системы внутренней защиты организма

Научно-практическая конференция Мониторинг туберкулеза и сопутствующие заболевания Г.С. Баласанянц ИННОВАЦИОННЫЕ ПОДХОДЫ К КОМПЛЕКСНОЙ ТЕРАПИИ БОЛЬНЫХ ТУБЕРКУЛЕЗОМ. НОВАЯ ГРУППА ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ – РЕГУЛЯТОРЫ СИСТЕМ ВНУТРЕННЕЙ ЗАЩИТЫ ОРГАНИЗМА Иркутск 2011

«…не вмешивайтесь в иммунологию. Не надо – она сама вмешается!» М.А. В.

« …. При рациональных комбинациях отдельных химиопрепаратов возможно потенцирование их туберкулостатического действия на микробную популяцию…» (А.Г. Хоменко/ Туберкулез органов дыхания. – 1988г.) « … Одним из основных принципов химиотерапии туберкулеза является применение комбинации препаратов. При приеме двух и более препаратов возникает суммарный бактериостатический эффект как за счет воздействия их на разные клеточные структуры микроорганизма, так и за счет повышения бактериостатической крови, и, соответственно, тканей организма больного…» (М.И. Перельман и др./Туберкулез (учебник). – 1990г.)
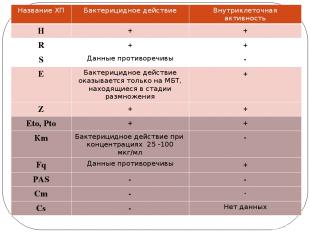
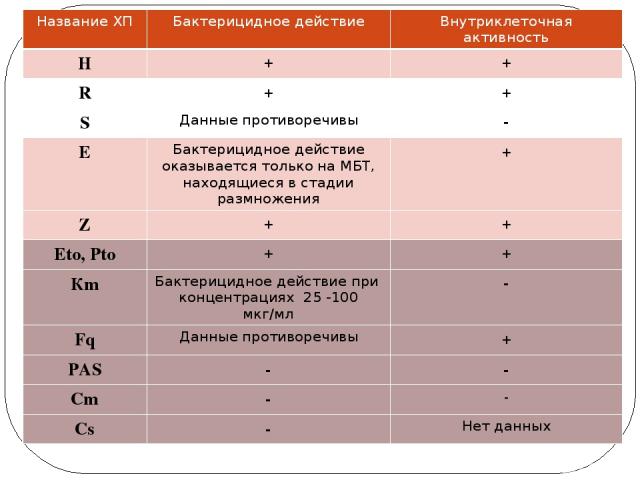
Название ХП Бактерицидное действие Внутриклеточная активность H + + R + + S Данные противоречивы - E Бактерицидное действие оказывается только на МБТ, находящиеся в стадии размножения + Z + + Eto,Pto + + Кm Бактерицидное действие при концентрациях 25 -100 мкг/мл - Fq Данные противоречивы + PAS - - Cm - - Cs - Нет данных

Проблема усугубляется невыгодной позицией на «поле боя» МБТ эволюционно приспособились сохранять жизнедеятельность внутриклеточно, фагоциты являются фармакологическим убежищем для МБТ Трансформированные фагоциты – источник биологически активных молекул, привносящих дисбаланс в реакции иммунной системы и ее взаимодействие с другими системами Изменения в макрофагах обусловлены как повреждающим действием микобактерий туберкулеза, так и действием ферментов, попадающих в ткани при разрушении фагоцитов. Комбинированная химиотерапия и, неизбежные в этих условиях, дополнительные изменения в тканевом метаболизме, также влияют на функциональную активность клеток Неполноценность фагоцитарной реакции благоприятствует хроническому течению специфического воспаления с развитием грубых морфологических изменений. Изменения тканевого метаболизма и реактивности организма существенно влияют на динамику и исход туберкулезного воспаления в процессе лечения.

Требования к средствам новой стратегии лечения туберкулеза Обеспечение модуляции иммунного ответа макроорганизма с целью эффективной элиминации МБТ Обеспечение возможности проведения курсовой ПХТ в полном объеме Подавление активности механизмов, обеспечивающих лекарственную устойчивость МБТ Обеспечение реализации терапевтического эффекта других лекарственных средств Уменьшение повреждающего воздействия МБТ на ткани



На сегодняшний день в США, Канаде, Европе, Китае реализуются подходы лечения хронических инфекционных и пролиферативно-воспалительных заболеваний, в которых используется противомикробный, антивирусный, противоопухолевый, иммуномодулирующий эффекты дефензинов. Дефензины – это катионные амфипатические пептиды длиной примерно в 30 аминокислот и трехнитевой β-пластинчатой структурой, содержащей три дисульфидные связи. На основании способа дисульфидного связывания дефензины разделяют на семейства – α-, β- и реже встречающиеся Θ-дефензины. У человека α-дефензины производятся в гранулах нейтрофилов как часть их противомикробного арсенала и в клетках крипт кишечника, а также в других лейкоцитах и эпителиоцитах. β-дефензины производятся в эпителии слизистых, коже и в некоторых лейкоцитах. Θ-дефензины – это циклические пептиды с высокой анти-ВИЧ активностью, которые не производятся у человека и пока были выявлены только у обезьян.
Высокое разнообразие по последовательностям и многофункциональная природа БИС дает большие возможности для конструирования искусственных пептидов и их производных с терапевтическими целями Терапевтический потенциал пептидов с прямым противомикробным действием уже хорошо изучен и некоторые из таких пептидов уже находятся на этапе клинических исследований Иммуномодулирующий пептид, который уже применяется как противоинфекционный препарат, - это препарат «Глутоксим» (NOV-002), хотя этот пептид и отличается от других синтетических катионных РЕИ. Единственным зарегистрированным препаратом, фармакологическая активность которого опосредована способностью восстанавливать ситуационно обусловленный уровень образования дефензинов, является ГЛУТОКСИМ.
Создание новых и производство современных лекарств в России неимоверно отстало. 75% назначаемых врачами препаратов – импортные, а многие «отечественные» производятся из импортного сырья. Полностью отечественных препаратов только 2% (Ю.Н. Штейнгардт, Здравоохранение РФ, 2011, №3)

Схема применения ГЛУТОКСИМ применяется внутримышечно ежедневно по 60 мг (3% 2 мл) в течение 10 дней Последующие 20 дней ГЛУТОКСИМ вводится в той же дозе (60 мг) через день По показаниям целесообразно продление курса для закрепления эффекта на протяжении всей интенсивной фазы терапии, в дозе 60 мг через день
ГЛУТОКСИМ - синтетический аналог природного гексапептида - окисленного глутатиона (GSSG) относят к метаболическим иммунокорректорам ввиду содержащихся в нем аминокислот (бис-γ-L-глутамил-L-цистенил-бис-глицин), которые транспортируются в пораженные клетки. ГЛУТОКСИМ оказывает комплексное воздействие на клеточный метаболизм, активирует функцию нормальных клеток и инициирует процесс элиминации из организма генетически дефектных клеток. Этот вариант иммунокоррекции осуществляет не «исправление», а поддержку адаптивных перестроек внутриклеточного обмена иммунных клеток. Под его воздействием повышается эффективность макрофагально-фагоцитарной реакции и устойчивость клеток к различным токсическим факторам .
Микобактерии паразитируют в альвеолярных макрофагах, нарушая созревание фагосом. Метаболическая активность микобактерий в фагосомах макрофагов индуцирует механизмы, подавляющие чувствительность рецепторного аппарата макрофагов к действию регуляторов.
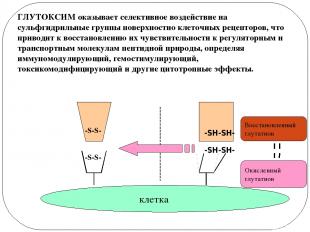
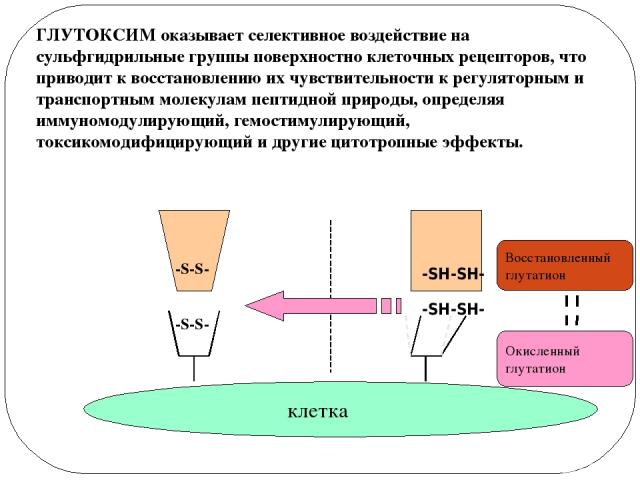
клетка -S-S- -S-S- -SH-SH- -SH-SH- Восстановленный глутатион Окисленный глутатион Окисленный глутатион ГЛУТОКСИМ оказывает селективное воздействие на сульфгидрильные группы поверхностно клеточных рецепторов, что приводит к восстановлению их чувствительности к регуляторным и транспортным молекулам пептидной природы, определяя иммуномодулирующий, гемостимулирующий, токсикомодифицирующий и другие цитотропные эффекты.

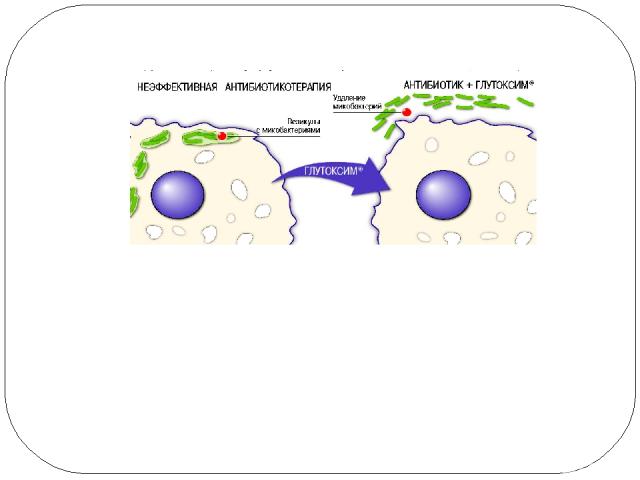
Глутоксим восстанавливает и, тем самым, стимулирует функционально-метаболическую активность макрофагов, что сопровождается либо секрецией (экзоцитозом) фагосом, либо их нормальным развитием с последующим перевариванием микобактерий. В дополнение к способности инициировать реакции удаления микобактерий туберкулеза из убежища в макрофагах, Глутоксим ограничивает активность механизма их проникновения в макрофаги.
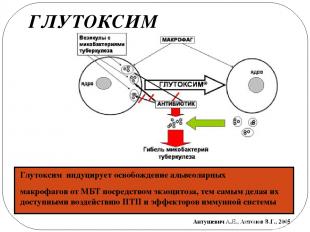
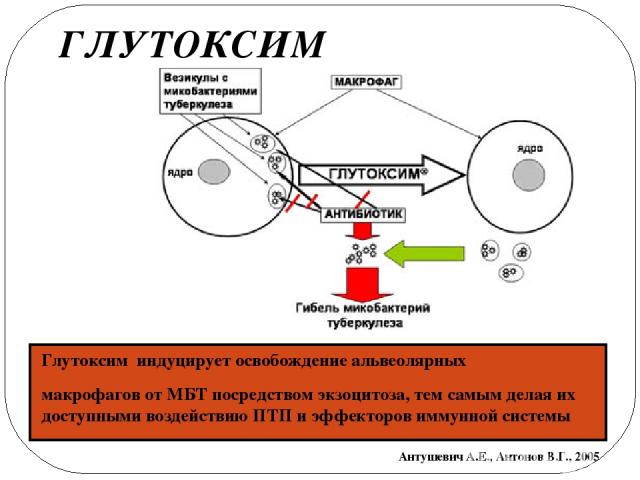
Глутоксим индуцирует освобождение альвеолярных макрофагов от МБТ посредством экзоцитоза, тем самым делая их доступными воздействию ПТП и эффекторов иммунной системы Антушевич А.Е., Антонов В.Г., 2005 ГЛУТОКСИМ
Действие Глутоксима приводит к нормализации соотношения иммунокомпетентных лимфоцитов – Т-хелперов (Th1 и Th2), устраняя преобладание Th2, одно из ведущих условий хронизации туберкулезного процесса с аллергическими проявлениями. Препарат также способствует усилению индуцированной ФГА продукции IL-2. Глутоксим активирует макрофаги и моноциты влияя на : - активность лизосомальных ферментов; - образование активных форм кислорода; - поглощение и киллинг микобактерий; - синтез цитокинов: интерлейкина-1, фактора некроза опухоли, колонистимулирующего фактора.
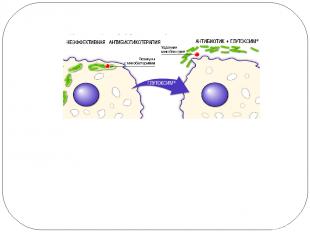
Способность МБТ использовать макрофаги в качестве убежища от эффекторов иммунной системы, средств фармакотерапии определяется рядом условий, включая депрессию процессов обмена кальция в макрофагах, низкую активность реакций опсонизации МБТ. Рецептор-опосредованное воздействие препарата ГЛУТОКСИМ на макрофаги, восстанавливающее физиологически необходимую интенсивность кальциевого обмена и активность Са2+зависимых путей индукции созревания фагосом, что обуславливает формирование качественного специфического иммунного ответа
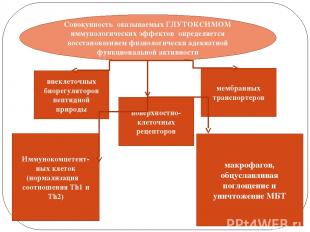
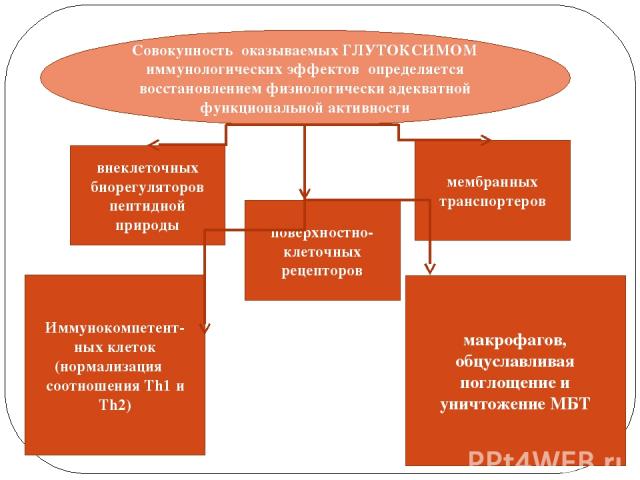
Совокупность оказываемых ГЛУТОКСИМОМ иммунологических эффектов определяется восстановлением физиологически адекватной функциональной активности внеклеточных биорегуляторов пептидной природы мембранных транспортеров поверхностно-клеточных рецепторов Иммунокомпетент-ных клеток (нормализация соотношения Th1 и Th2) макрофагов, обцуславливая поглощение и уничтожение МБТ

Глутоксим, изменяя активность мембранных транспортеров лекарственной устойчивости, «преодолевает» ее и способствует повышению эффективности средств противотуберкулезной химиотерапии Глутоксим способен ограничивать развитие и функционирование механизмов лекарственной устойчивости Micobacterium tuberculosis, так как препарат является фактором негативной регуляции процессов индуцированного мутагенеза, предопределяя, тем самым, снижение способности образования и отбора лекарственно устойчивых штаммов МБТ при проведении противотуберкулезной терапии.

Сочетание Глутоксима с основными противотуберкулезными препаратами повышает антимикробный эффект изониазида и рифампицина. В культуре легочной ткани, инфицированной устойчивыми к изониазиду, рифампицину и стрептомицину МБТ, при добавлении Глутоксима антимикробный эффект комбинации циклосерин+рифабутин увеличивается в 3 раза, а комбинации циклосерин+протионамид в 5 раз.

Гепатопротективное и детоксицирующее действие ГЛУТОКСИМА В результате восстанавливается вся цепочка - захват, переработка и элиминация гепатоцитом токсинов, как эндогенных, так и экзогенных
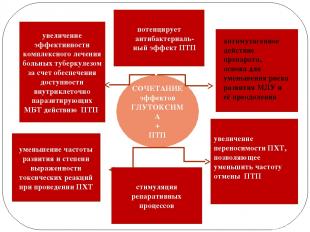
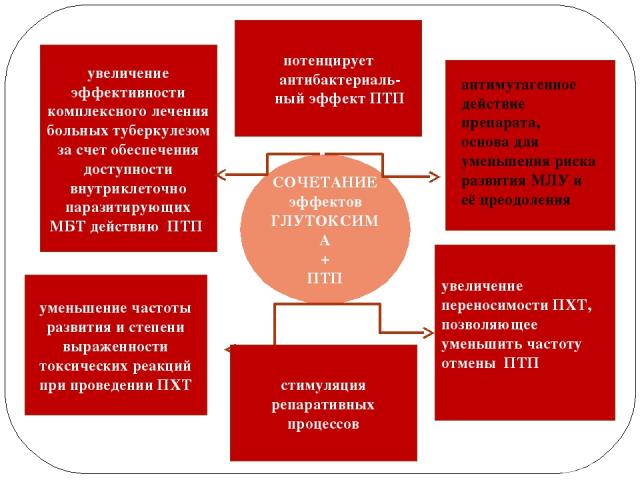
СОЧЕТАНИЕ эффектов ГЛУТОКСИМА + ПТП увеличение эффективности комплексного лечения больных туберкулезом за счет обеспечения доступности внутриклеточно паразитирующих МБТ действию ПТП уменьшение частоты развития и степени выраженности токсических реакций при проведении ПХТ увеличение переносимости ПХТ, позволяющее уменьшить частоту отмены ПТП антимутагенное действие препарата, основа для уменьшения риска развития МЛУ и её преодоления потенцирует антибактериаль-ный эффект ПТП стимуляция репаративных процессов

Повышение эффективности комплексного лечения больных туберкулезом легких Профилактика послеоперационных осложнений Улучшение переносимости химиотерапии Снижение частоты отмены ПТП Уменьшение риска развития МЛУ Улучшение эпидемиологических показателей Уменьшение затрат на лечение больных Сокращение пребывания в стационаре Уменьшение затрат на гепатопротекторы Снижение потребления препаратов резерва Результаты применения

Эффективные пути клинического излечения Нарушение закономерностей жизненного цикла МБТ, включая внутриклеточное паразитирование Подавление механизмов развития МЛУ Повышение устойчивости защитных систем организма