Презентация на тему: СТРОЕНИЕ И СВОЙСТВА АЛКАНОВ



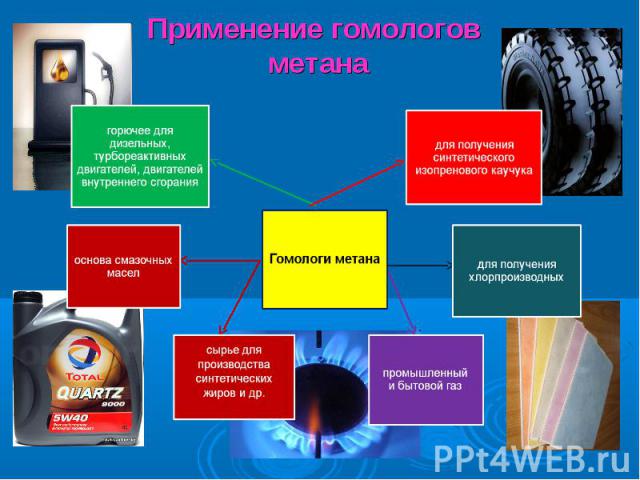
Где геологу найти алканы? Где геологу найти алканы? Что общего найдет математик и физик между молекулой метана и пакетом молока? Что делать химику с алканами? Экологи и технологи спорят: алканы – зло или благо?

Вот что мы узнали!!! Вот что мы узнали!!!




Проблемный вопрос: Почему Проблемный вопрос: Почему алканы называются «предельными углеводородами»?

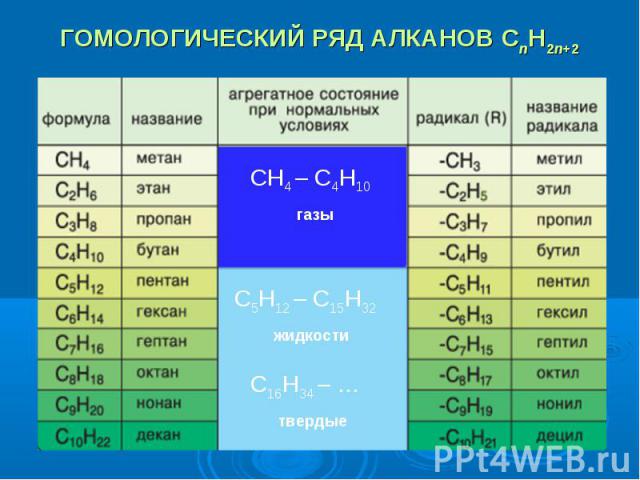
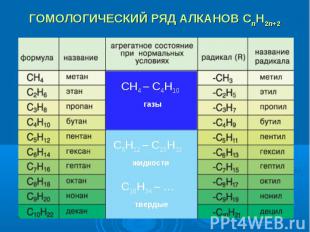
Вспомните, какие вещества мы называем гомологами? Вспомните, какие вещества мы называем гомологами?

выяснить, что общего между молекулой метана и пакетом молока? выяснить, что общего между молекулой метана и пакетом молока?
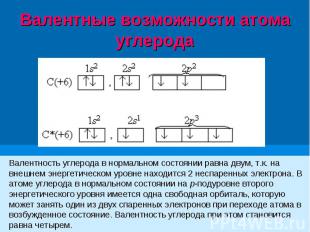
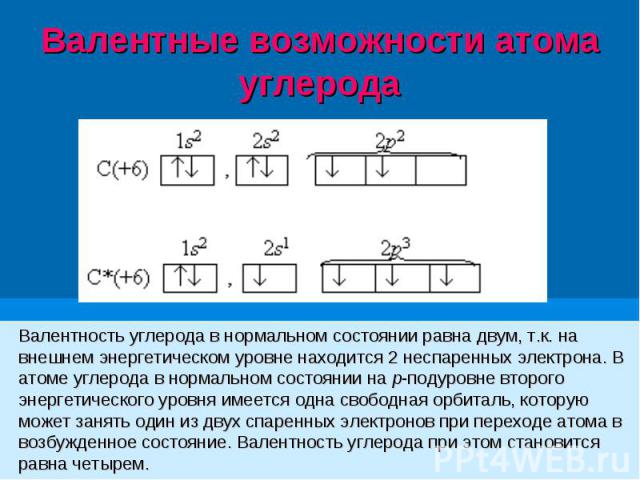
Валентность углерода в нормальном состоянии равна двум, т.к. на внешнем энергетическом уровне находится 2 неспаренных электрона. В атоме углерода в нормальном состоянии на р-подуровне второго энергетического уровня имеется одна свободная орбиталь, которую может занять один из двух спаренных электронов при переходе атома в возбужденное состояние. Валентность углерода при этом становится равна четырем. Валентность углерода в нормальном состоянии равна двум, т.к. на внешнем энергетическом уровне находится 2 неспаренных электрона. В атоме углерода в нормальном состоянии на р-подуровне второго энергетического уровня имеется одна свободная орбиталь, которую может занять один из двух спаренных электронов при переходе атома в возбужденное состояние. Валентность углерода при этом становится равна четырем.

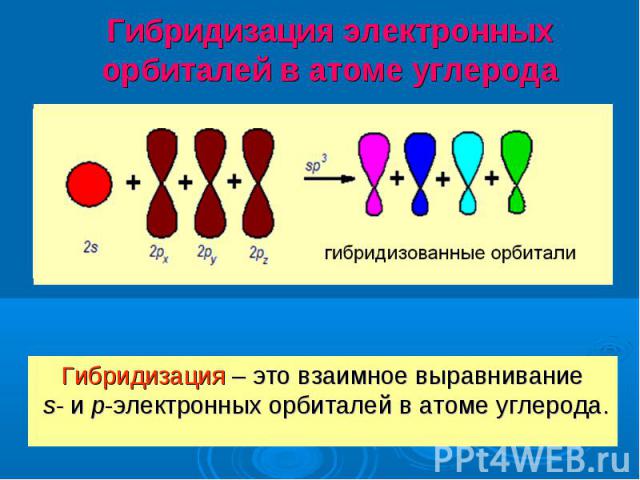
Гибридизация – это взаимное выравнивание s- и р-электронных орбиталей в атоме углерода. Гибридизация – это взаимное выравнивание s- и р-электронных орбиталей в атоме углерода.

В алканах все четыре неспаренных электрона у углеродных атомов участвуют в процессе гибридизации. Такой тип называется В алканах все четыре неспаренных электрона у углеродных атомов участвуют в процессе гибридизации. Такой тип называется sp3 – гибридизация
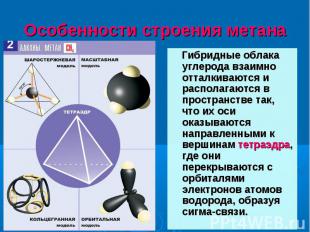
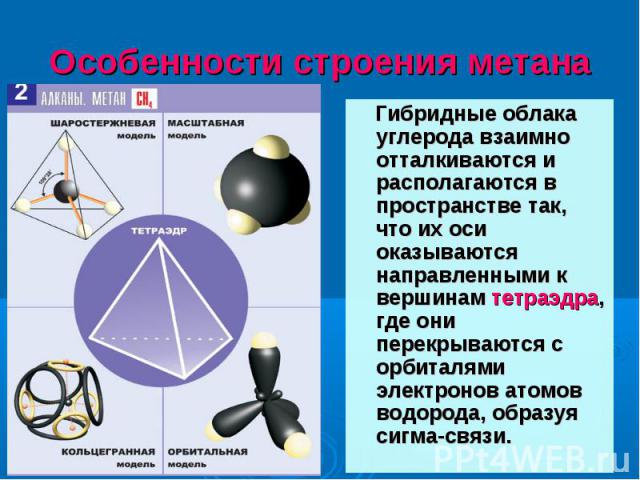
Гибридные облака углерода взаимно отталкиваются и располагаются в пространстве так, что их оси оказываются направленными к вершинам тетраэдра, где они перекрываются с орбиталями электронов атомов водорода, образуя сигма-связи. Гибридные облака углерода взаимно отталкиваются и располагаются в пространстве так, что их оси оказываются направленными к вершинам тетраэдра, где они перекрываются с орбиталями электронов атомов водорода, образуя сигма-связи.
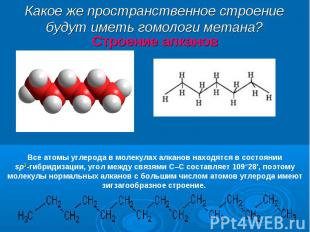

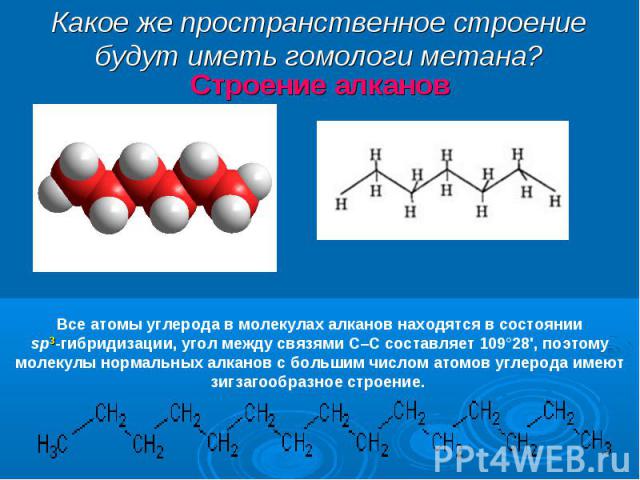
Тип гибридизации атома углерода в алканах определяет направление гибридных электронных облаков в пространстве к вершинам тетраэдра . Такое же пространственное строение имеет и пакет молока. Тип гибридизации атома углерода в алканах определяет направление гибридных электронных облаков в пространстве к вершинам тетраэдра . Такое же пространственное строение имеет и пакет молока.

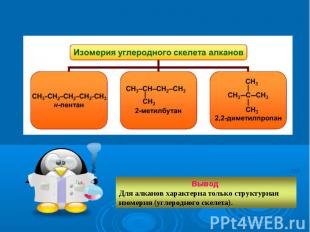

t кипения и t плавления увеличиваются t кипения и t плавления увеличиваются

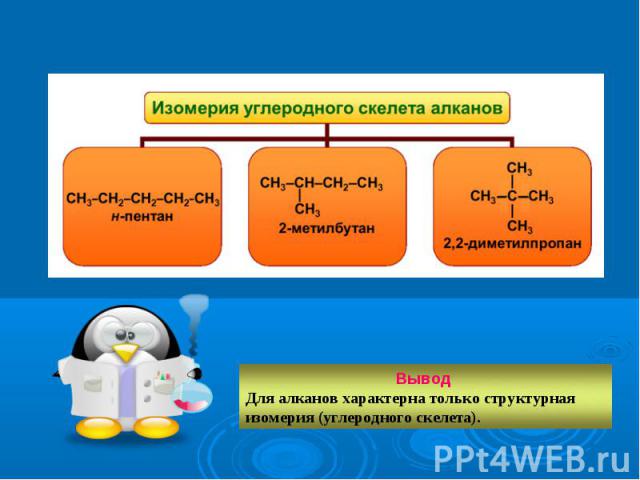
1. Выбирают наиболее длинную (главную) цепь и нумеруют ее, начиная с того конца, к которому ближе радикал (заместитель, обозначен желтым цветом). 1. Выбирают наиболее длинную (главную) цепь и нумеруют ее, начиная с того конца, к которому ближе радикал (заместитель, обозначен желтым цветом). 2. Название строится в следующей последовательности: префикс + корень + суффикс. а) Префикс состоит из цифры, указывающей на номер углеродного атома, возле которого стоит радикал, и названия самого радикала. Например: 3-метил… Если молекула содержит несколько одинаковых радикалов, то после перечисления всех цифр, указывающих их местоположение, к названию радикала добавляют числовую приставку (ди – два, три – три, тетра – четыре). Например: 2,3-диметил…, или 3,4,5-триэтил… б) Корень – название неразветвлённого алкана с таким же количеством атомов углерода, как в выбранной нами главной цепи. в) Суффикс – у алканов суффикс «ан».

Проблемный вопрос: Почему алканы считают малоактивными веществами? Проблемный вопрос: Почему алканы считают малоактивными веществами?


1) Горение алканов: 1) Горение алканов: CnH2n+2 + O2 CO2 + H2O.

2) Каталитическое окисление алканов. 2) Каталитическое окисление алканов.

При сильном нагревании без доступа воздуха происходит полное разложение алканов на простые вещества. При сильном нагревании без доступа воздуха происходит полное разложение алканов на простые вещества. CH4 C + 2H2.


Запомни! Запомни!

В промышленности: В промышленности: а) из природного газа; б) синтез из оксида углерода (II) и водорода (из синтез-газа): CO + 3H2 CH4↑ + H20. В лаборатории: а) гидролиз карбида алюминия: Al4C3 + 12H2O 3CH4↑ + 4Al(OH)3; б) сплавление солей уксусной кислоты (ацетатов) со щелочами: CH3COOH (тв.) + NaOH (тв.) CH4↑+ Na2CO3.
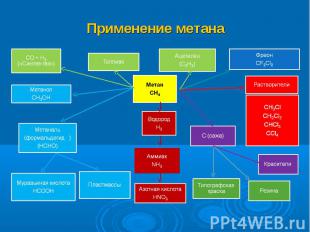


Как алканы влияют на климат? Метан считается одним из парниковых газов и остается предметом активных обсуждений и исследований в связи с проблемами глобального изменения климата.












а) C4H10 + O2 = б) этан + Cl2 = в) C5 H12 →
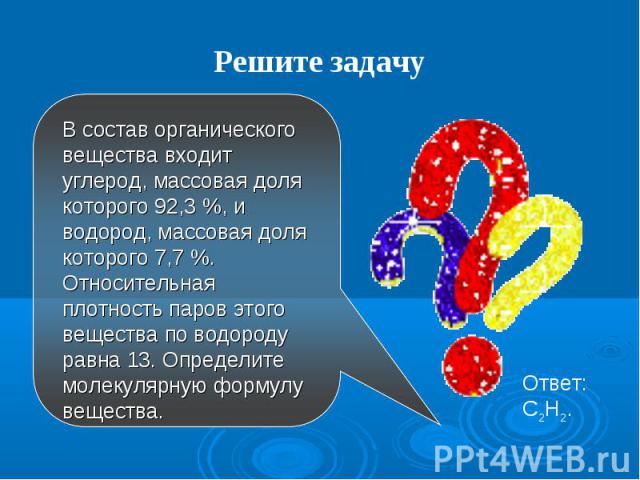
В состав органического вещества входит углерод, массовая доля которого 92,3 %, и водород, массовая доля которого 7,7 %. Относительная плотность паров этого вещества по водороду равна 13. Определите молекулярную формулу вещества. В состав органического вещества входит углерод, массовая доля которого 92,3 %, и водород, массовая доля которого 7,7 %. Относительная плотность паров этого вещества по водороду равна 13. Определите молекулярную формулу вещества.