Презентация на тему: Презентация Химические свойства и применение алканов


Образовательная: изучение химических свойств алканов, опираясь на их строение. Образовательная: изучение химических свойств алканов, опираясь на их строение. Развивающая: продолжить формирование умения составлять уравнения химических реакций, умений анализировать, сравнивать делать собственные выводы. Воспитательная: воспитание патриотизма на примерах значительных вкладов в химическую науку русских и советских ученых, показать использование алканов и их производных в мирных целях

Изучить важнейшие химические свойства алканов и показать их зависимость от особенностей строения предельных углеводородов. Изучить важнейшие химические свойства алканов и показать их зависимость от особенностей строения предельных углеводородов. Совершенствование составления структурных формул гомологов, изомеров, уравнений химических реакций. Раскрыть важнейшие области практического применения алканов

Горение Горение При поджигании на воздухе алканы горят, превращаясь в двуокись углерода и воду и выделяя большое количество тепла. CH4 + 2O2 ––пламя> CO2 + 2H2O C5H12 + 8O2 ––пламя> 5CO2 + 6H2O

Реакции замещения - это Реакции замещения - это реакции алканов, идущих с разрывом С_Н связей.

СН4 + Cl2hv CH3Cl + HCl Хлорметан, или Хлористый метил СН3 Cl – газ, легко сжижается и при последующем испарении поглощает большое количество теплоты. Применяется в холодильных установках

СН3Cl + Cl2 hv CH2Cl2 + HCl СН3Cl + Cl2 hv CH2Cl2 + HCl Дихлорметан, или хлористый метилен СН2 Cl2 – применяется как растворитель, для склеивания пластиков

СН2Cl2 + Cl2 hv CHCl3 + HCl СН2Cl2 + Cl2 hv CHCl3 + HCl Трихлорметан или хлороформ СН Cl3 – хлороформ, бесцветная летучая жидкость с эфирным запахом и сладким вкусом используется: при производстве фреонового хладагента; в качестве растворителя в фармакологической промышленности; для производства красителей и пестицидов

СНCl3 + Cl2 hv CCl4 + HCl СНCl3 + Cl2 hv CCl4 + HCl Тетрахлорметан, (четыреххлористый углерод) С Cl4 - применяется как растворитель (жиров, смол, каучука); для получения фреонов, в медицине. Являлся стандартным наполнителем переносных огнетушителей для советской бронетехники

При нагревании алканов до 140°С с разбавленной (10%-ной) азотной кислотой под давлением осуществляется реакция нитрования – замещение атома водорода нитрогруппой (реакция М.И.Коновалова). СН4 + HO-NO2 = CH3-NO2 + H2O

Под влиянием катализаторов при нагревании углеводороды нормального строения подвергаются изомеризации - перестройке углеродного скелета с образованием алканов разветвленного строения. Под влиянием катализаторов при нагревании углеводороды нормального строения подвергаются изомеризации - перестройке углеродного скелета с образованием алканов разветвленного строения. CH3-CH2-CH2-CH3 AlCl3 CH3-CH-CH3 CH3 n-бутан 2-метил пропан

При нагревании до температуры выше 500° в молекулах алканов происходит разрыв связей между атомами углерода. При нагревании до температуры выше 500° в молекулах алканов происходит разрыв связей между атомами углерода. C 10H22 C5H12+C5H10 C10H22 C4H10+C6H12 Этот процесс называется термическим крекингом (от англ. tocrack– «колоть, расщеплять»).


При увеличении температуры можно достичь такой степени протекания реакции, при которой органические вещества – углеводороды – полностью разлагаются на углерод и водород. Такой процесс называется пиролизом. При увеличении температуры можно достичь такой степени протекания реакции, при которой органические вещества – углеводороды – полностью разлагаются на углерод и водород. Такой процесс называется пиролизом. СН4 С+2Н2

При пропускании нагретого алкана над платиновым или никелевым катализатором может отщепиться водород. Этот процесс называется дегидрированием При пропускании нагретого алкана над платиновым или никелевым катализатором может отщепиться водород. Этот процесс называется дегидрированием C3H8 C3H6 + H2

СН4+Н2O CO+3H2 СН4+Н2O CO+3H2 Так называют взаимодействия алканов, из которых чаще всего используют природный газ с парами воды. При высокой температуре около 1000 образуется смесь оксида углерода – угарного газа и водорода. Эту смесь называют синтез- газ. Часто ее не разделяют, а используют для получения разных органических веществ.

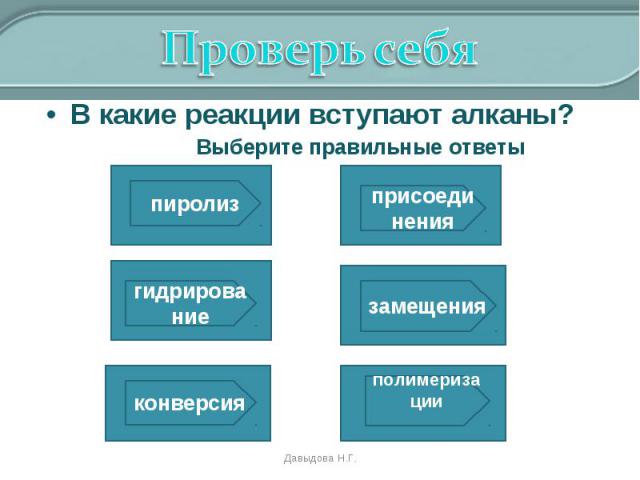
В какие реакции вступают алканы? В какие реакции вступают алканы? Выберите правильные ответы
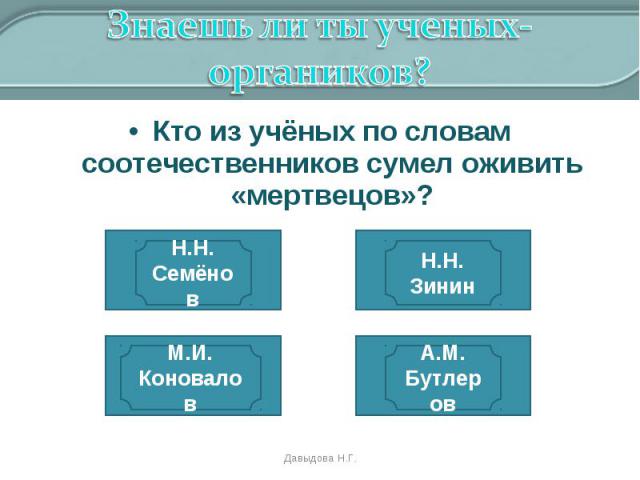
Кто из учёных по словам соотечественников сумел оживить «мертвецов»? Кто из учёных по словам соотечественников сумел оживить «мертвецов»?

По желанию можно выполнить одно из двух заданий: По желанию можно выполнить одно из двух заданий: 1. Составить генетическую цепь, используя полученные знания по химическим свойствам (3-4 звена). 2. Какой из галогензамещённых алканов применяли как анестезирующее средство? (используя справочную литературу подготовить сообщение)

http://school-collection.edu.ru/catalog/res/76f609e3-5da6-7559-4264-68d3548bb069/view/ http://school-collection.edu.ru/catalog/res/76f609e3-5da6-7559-4264-68d3548bb069/view/ http://files.school-collection.edu.ru/dlrstore/8d7caa13-f7f5-c3db-3f7d-a504e7456d96/00119627250504103.htm http://files.school-collection.edu.ru/dlrstore/5838e73f-fd71-188f-d53c-b3903cc3a965/00119627348768537.htm http://school-collection.edu.ru/catalog/res/5e8f612a-b762-9f6b-de63-c5dc1d3e64c5/view/ http://school-collection.edu.ru/catalog/res/47cbac0d-2c6b-46bc-d57f-4b250cfa0e07/view/ htthttp://school-collection.edu.ru/catalog/res/47cbac0d-2c6b-46bc-d57f-4b250cfa0e07/view/ p://www.youtube.com/watch?v=CnJnT9tXzaQ http://www.youtube.com/watch?v=CnJnT9tXzaQ