Презентация на тему: Степень окисления

ХимияСтепень окисления

ОглавлениеГлава1 – понятие о степени окисления.Глава2 – определение степени окисления.Глава3 – степень окисления в ионе.Глава4 - составление формул по степеням окисления.Глава5 – правило креста.Глава6 – тренировочные задания.Глава7 – правильные ответы.Глава8 – проверочная работа, ответы.Глава9 – степень окисления углерода.

Степень окисленияСтепень окисления – это условный заряд атома химического элемента в соединении, вычисленный на основе предположения, что все соединения (и ионные, и ковалентные полярные) состоят только из ионов .

Определение степени окисленияСтепень окисления простых веществ равна нулю Например: S0, H02, Cl02, O02, Na0.Максимальная (высшая) степень окисления равна + номер группы (элемент на первом месте) Например: P2+5O5 , S+6F6. Если степень окисления переменная – будет указано в скобках.Минимальная степень окисления равна – ( 8 – номер группы) (элемент на втором месте) Например: SCl2-1 , Li3P-3.Постоянные степени окисления:H +1 (кроме гидридов активных металлов, например:Na+1H-1)O-2 (кроме O+2F2, H2O2-1,пероксидов металлов)F-1металлы первой группы (кроме Cu, Au) –степень окисленияметаллы второй группы (кроме Hg) – степень окисления B и металлы третьей группы – степень окисления

Алгебраическая сумма степеней окисления в веществе равна нулю

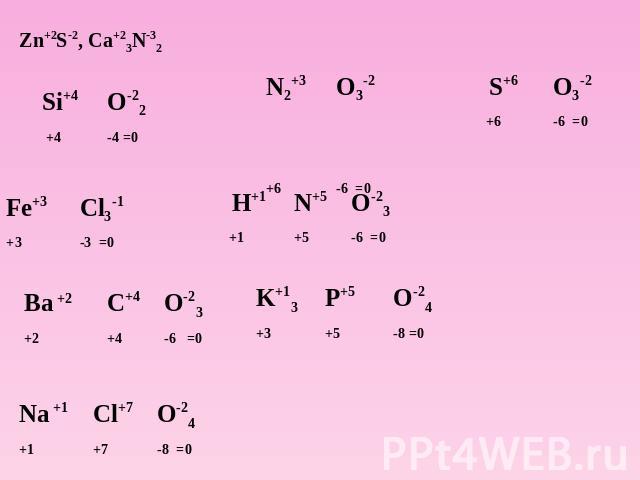
Определение степени окисления +6 -2SO3 +7 -2Mn2O7 +5 -2P2O5 +1 -2Li2O +3 -2B2O3 +1 -3H3N +2 -1BaCl2 +6 -1SF6 +2 -1MgH2 +2 -2CaS

Алгебраическая сумма степеней окисления в ионе Правило: алгебраическая сумма степеней окисления в сложном ионе равна суммарному заряду этого иона.Рассмотрим пример:Обозначим степень окисления кислорода-2 .Три иона кислорода будут иметь общий отрицательный заряд(-2).3=-6. Тогда общий заряд двух ионов серы будет равен+4, а одного иона (+4):2=+2 (S22+O3-2)2-

Zn+2S-2, Ca+23N-32

Правило креста Правило креста: для составления химических формул по названию вещества надо записать соответствующие знаки химических элементов и указать степени окисления каждого из них.Например, оксид алюминия - Al+3O-2. Затем по «правилу креста» степень окисления кислорода равна индексу у атома Al, а степень окисления алюминия-индексу у атома O. Al+3 O-2 Al2O3

Составление формул по степени окисления Оксид натрия -Хлорид железа (III) -Нитрид магния -Оксид серы (IV) -Сульфид алюминия - Гидрид магния -Na+1O-2 Fe+3Cl-1Mg+2N-3 S+4O-2 сокращается на два - SO2Al+3S-2Mg+2H-1

Тренировочные задания (подготовка к с/р) Расставьте степени окисления в соединениях и в ионах:MgO ZnKNO3HMnO4CaSo3Na3PO4(CrO4)-2(IO4)-Составьте формулы следующих соединений:Хлорид железа(III) Оксид серы(VI) Гидрид калияНитрид барияНазовите вещества, представленные формулами:P2O5 AgBr CuS NaH

Правильные ответы Mg+2O-2 , Zn0

Хлорид железа(III) – Fe+3Cl3 -1 Оксид серы(VI) – S+6O3-2 Гидрид калия – K+1H-1 Нитрид бария – Ba3+2N2 -1P2O5 – оксид фосфора(V) AgBr – бромид серебра CuS – сульфид меди(II) NaH – гидрид натрия

Проверочная работа I вариант H2SO3 H4P2O7 ZnF2 BaCO3 O2 Na2SO4(PO4)3-, (MnO4)-II вариант CaBr2 KClO4 S8 Na2Cr2O7 Li2SO4 MgSiO3 (ClO2)- ,(NO3)- Составьте формулы следующих соединений:

Ответы к проверочной работе I вариант1H2+1S+4O3-2 H4+1P2+5O7-2Zn+2F2-1 Ba+2C+4O3-2 O20 Na2+1S+6O4-2(P+5O4-2)3-(Mn+7O4-2)-II вариант 1Ca+2Br2-1 K+1CL+7O4-2 S80 Na2+1Cr2+6O7-2 Li2+1S+6O4-2 Mg+2Si+4O3-2 (Cl+3O2-2)-(N+5O3-2)-

2.Хлорид магния- MgCl2, Сульфид железа (III)- Fe2S3Оксид бора - B2O3Нитрид кальция - Ca3N2Оксид азота(II) - NO 3.Гидрид лития - LiHОксил меди(II) - CuOХлорид железа(III) - FeCl3Сульфид серебра - Ag2S2.Фторид алюминия - AlF3Гидрид бария - BaH2Оксид серы(IV) - SO2Сульфид магния - MgSНитрид лития - Li3N3.Хлорид железа(II) - FeCl2Гидрид кальция - CaH2Оксид углерода(IV) - CO2Сульфид алюминия - Al2S3
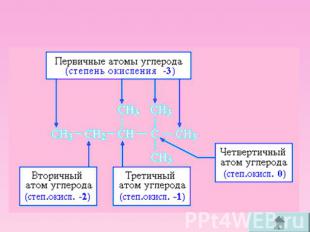
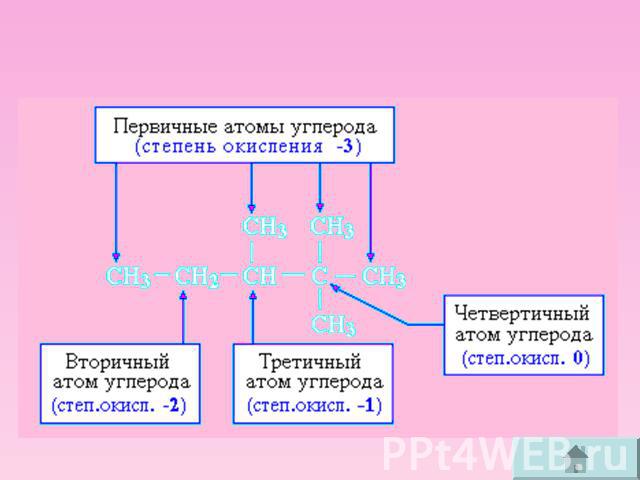
Степень окисления атома углерода