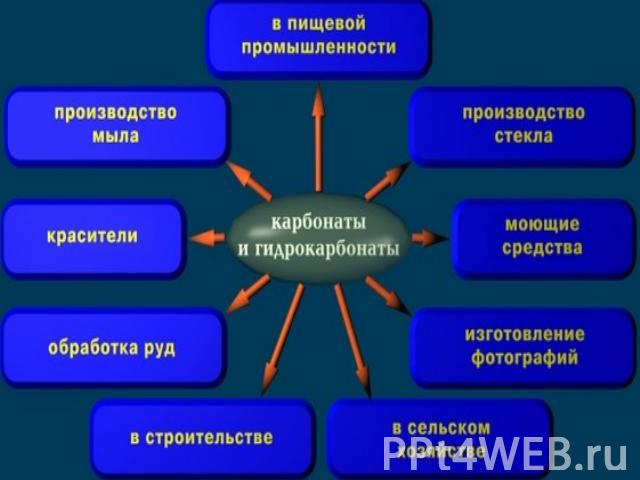
Презентация на тему: Путешествие по стране карбонатов

Путешествие по стране карбонатов

Кроссворд
Маршрутный лист

СТАНЦИЯИНФОРМАЦИОННАЯ
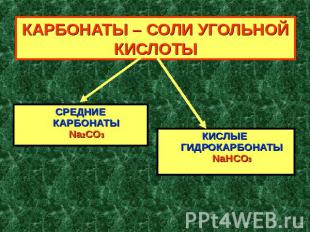
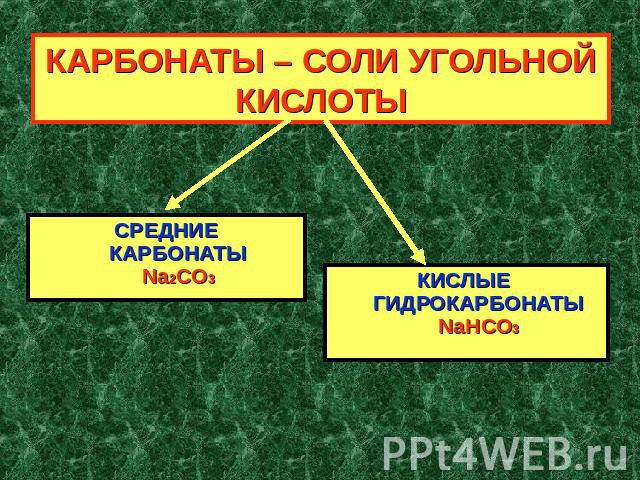
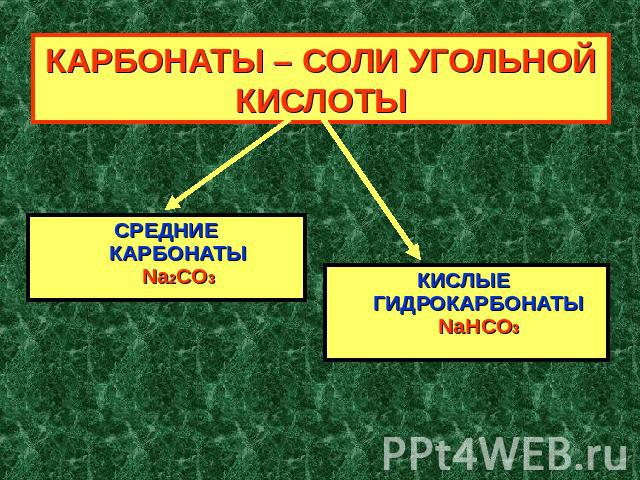
КАРБОНАТЫ – СОЛИ УГОЛЬНОЙ КИСЛОТЫ СРЕДНИЕКАРБОНАТЫNa2CO3КИСЛЫЕ ГИДРОКАРБОНАТЫNaHCO3
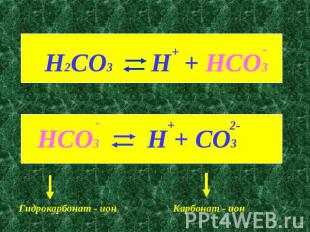
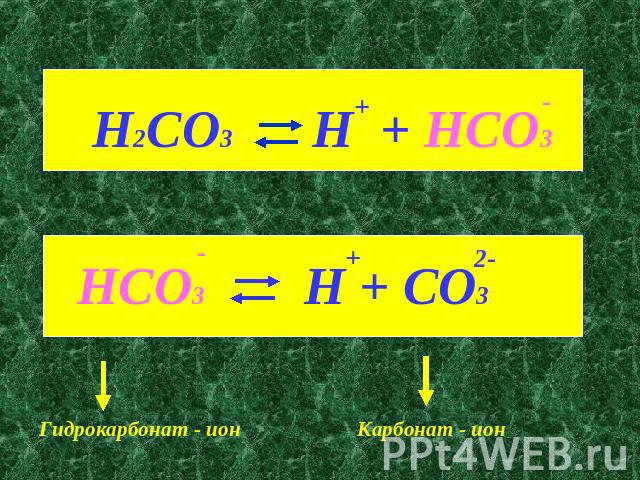
H2CO3 H + HCO3HCO3 H + CO3
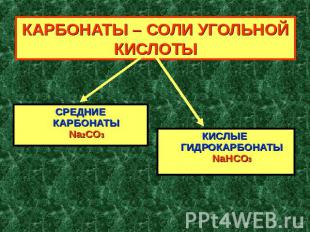
КАРБОНАТЫ – СОЛИ УГОЛЬНОЙ КИСЛОТЫ СРЕДНИЕКАРБОНАТЫNa2CO3КИСЛЫЕ ГИДРОКАРБОНАТЫNaHCO3
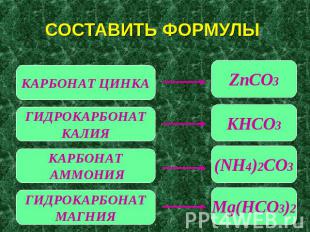
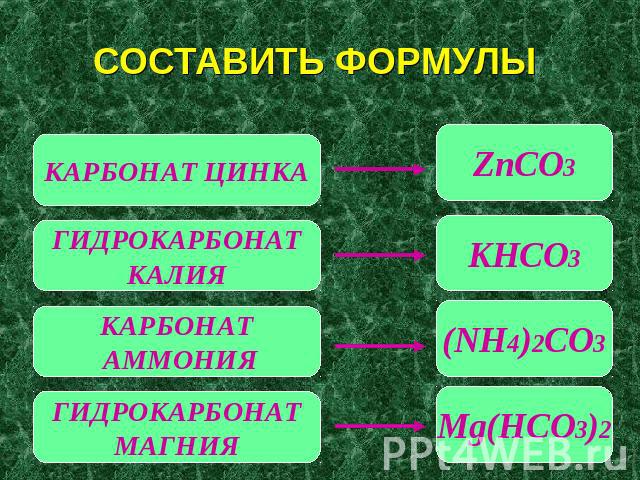
СОСТАВИТЬ ФОРМУЛЫ

СТАНЦИЯЭКСПЕРИМЕНТАЛЬНАЯ

Взаимодействие с сильными кислотамиCaCO3+2HCl = CaCl2 +H2O+CO2Качественные реакции
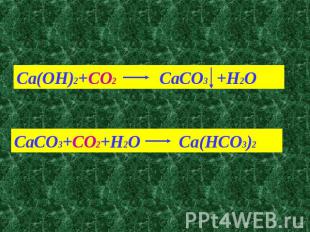
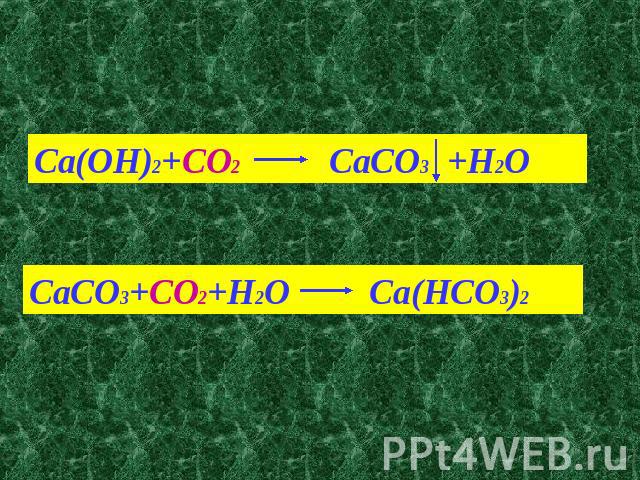
Ca(OH)2+CO2 CaCO3 +H2O CaCO3+CO2+H2O Ca(HCO3)2

Превращение гидрокарбонатов в карбонатыа) при нагревании2NaHCO3 Na2CO3 + H2O+CO2 б) при действии щёлочиNaHCO3 + NaOH Na2CO3 + H2O

Взаимодействие с растворами солейNa2 CO3+BaCl2 BaCO3 +2NaCl Разложение карбонатовРазложение карбонатов

ОСУЩЕСТВИТЕ ПРЕВРАЩЕНИЕ I. Ca(OH)2 CaCO3 Ca(HCO3)2II. NaOH Na2CO3 NaHCO3III. Na2CO3 BaCO3 CO2

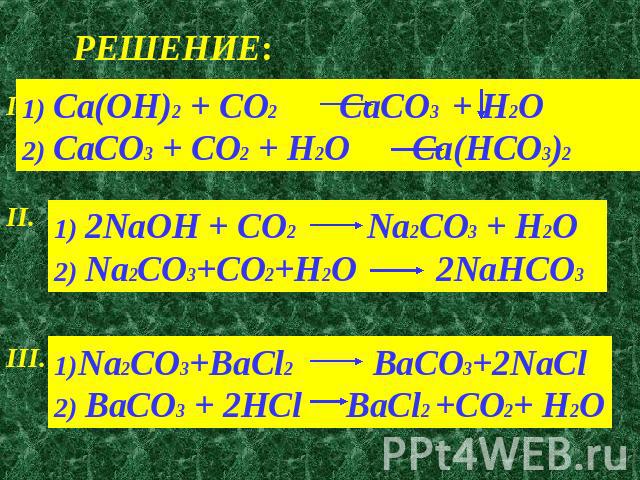
РЕШЕНИЕ: 1) Ca(OH)2 + CO2 CaCO3 + H2O2) CaCO3 + CO2 + H2O Ca(HCO3)21) 2NaOH + CO2 Na2CO3 + H2O 2) Na2CO3+CO2+H2O 2NaHCO31)Na2CO3+BaCl2 BaCO3+2NaCl 2) BaCO3 + 2HCl BaCl2 +CO2+ H2O
СТАНЦИЯ БИОЛОГО - ГЕОГРАФИЧЕСКАЯ

КОРАЛЛОВЫЕ ПОЛИПЫ – CaCO3
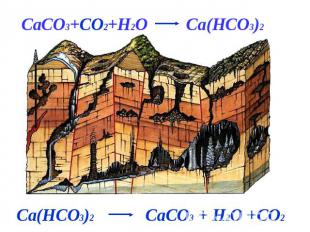
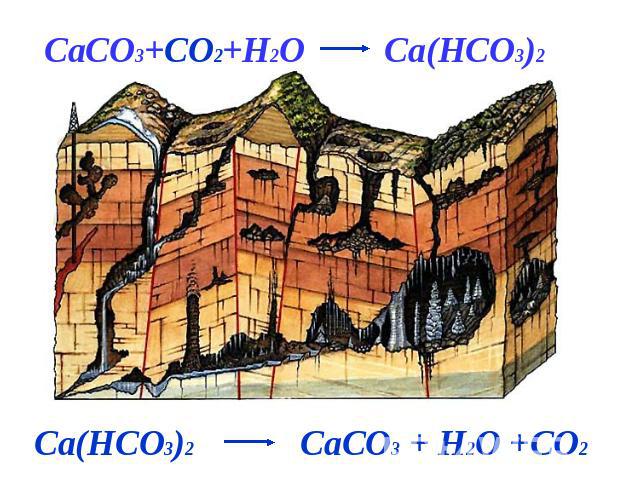
CaCO3+CO2+H2O Ca(HCO3)2Ca(HCO3)2 CaCO3 + H2O +CO2
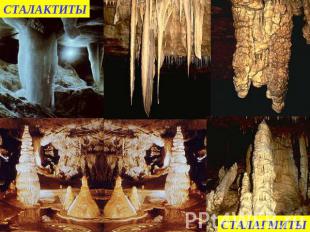
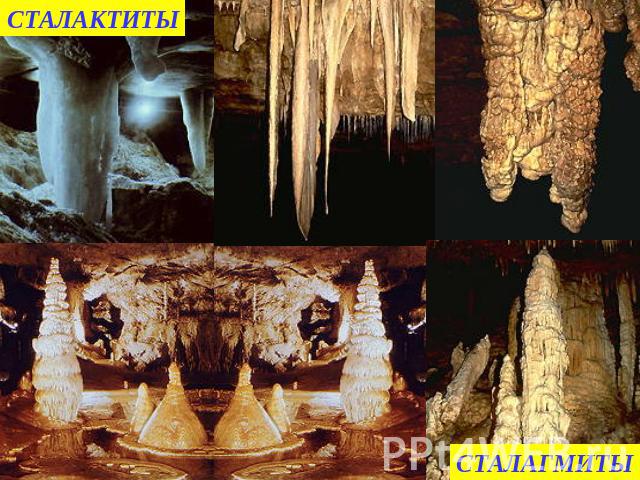
СТАЛАКТИТЫСТАЛАГМИТЫ

СТАНЦИЯ ПРАКТИЧЕСКАЯ

ИЗВЕСТНЯК – CaCO3

МРАМОР – CaCO3

МРАМОРНЫЙ ДВОРЕЦ

Na HCO3 – ПИТЬЕВАЯ СОДАNaHCO3 + HCl = NaCl + CO2 + H2O
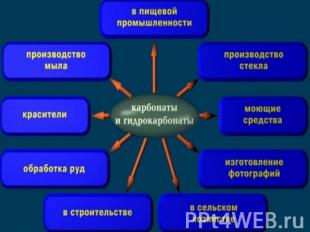

СТАНЦИЯ КОНЕЧНАЯ

1)Какие три брата из семейства карбонатов живут на Земле?Мрамор, известняк, мел.2) Зачем хозяйки добавляют питьевую соду в тесто?2NaHCO3 Na2CO3 + H2O+CO2 Углекислый газ делает тесто пористым.

3) Что такое сталактиты? Каменные сосульки в пещерах состоящие из карбоната кальция.4) Как химическим путем очистить яйцо от скорлупы, не разбивая его?Растворить скорлупу с помощью соляной кислоты.

5) Как еще называют гидрокарбонат натрия (NaHCO3)?Питьевая сода.6) Как вы посоветуете геологамв полевых условиях распознать карбонатные породы?Подействовать кислотой и наблюдать выделение газа.

Домашнее задание.Составить реакции к проведенному опыту.Конец.