Презентация на тему: Решение задач по уравнению реакции

МБОУ «Дмитриевогорская СОШ» Презентация к уроку химии в 8 классе Тема: Решение задач по уравнению реакции Подготовила: учитель химии Некрасова Нина Сергеевна 2012г 5klass.net

Декарт Решить задачу – значит выиграть сражение Элементарий

Цель урока : Научиться выигрывать сражения или Научиться решать задачи

символ элемента – формула соединения – уравнение химической реакции Какие задачи мы научились решать на уроках химии? 1. По символу химического элемента 2. По химической формуле сложного соединения

Тема урока Решение задач по уравнению химической реакции


Как называется это поле? H2SO4 СuSO4 NaOH FeCl3 PbO Ca (OН) 2 H2 PbS Б О Р О Д И Н О

1812 2012 200

Наполеон разрабатывает план сражения

Поможем Русской армии подготовиться к сражению. Доставить донесение в штаб: проверяем 36,5 62 , 56 63, 142 , 71

Кутузов планирует сражение

Алгоритм решения задачи 1. Читаю условие задачи. Провожу мысленный эксперимент 2. Запишу условие задачи (дано) 3. Напишу уравнение реакции, которое отвечает условию задачи, расставлю, если нужно, коэффициенты. 4. Подчеркну одной чертой формулу вещества, масса которого указана в условии задачи а двумя чертами – формулу вещества, массу которого необходимо вычислить 5. Помню, что коэффициенты перед формулами – это количества веществ, вступающих в реакцию и образующихся в результате реакции, (число молей). Если коэффициентов нет, мысленно ставлю коэффициент 1. Под формулами веществ напишу отношение этих веществ Генеральный план сражения

6. Помню, что вещества вступают в реакцию в количествах веществ, кратных их коэффициентам, рассчитаю по формуле количество вещества, указанного в условии задачи, предварительно найду молярную массу вещества 7. Запишу результат над формулой этого вещества, а над формулой искомого вещества поставлю х моль 8. Рассуждаю: По уравнению реакции вещества взаимодействуют в соотношении А по условию задачи: 9. Составляю пропорцию, нахожу х 10. По формуле нахожу массу вещества. 11. Запишу ответ

Молодцы! А теперь настал час сражения! Решаем задачу: Найти массу меди, которая выделится на железной пластинке, опущенной в раствор сульфата меди ,если масса растворенной соли равна 240г Выполняем пункт 1. Внимательно читаем условие и представляем, как мысленно провести эксперимент, описанный в задаче.

Пункты 2 , 3 и 4 Дано: mCuSO4=240г mCu=? СuSO4 + Fe = FeSO4 + Cu
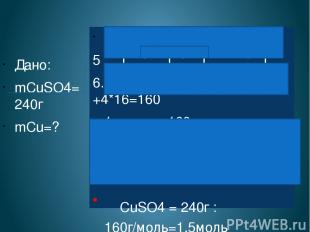
Дано: mCuSO4=240г mCu=? СuSO4 + Fe = FeSO4 + Cu 5 1 : 1 : 1 : 1 6. Найдем МCuSO4 64 +32 +4*16=160 1 моль = 160 г ν= m/M νCuSO4 = 240г :160г/моль=1,5моль
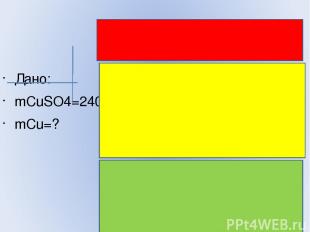
Дано: mCuSO4=240г mCu=? 1,5моль хмоль СuSO4 + Fe = FeSO4 + Cu 1 1 8. Рассуждаю: Из 1 моль ---------1 моль Из 1,5 моль -----------х моль 9. Составляю пропорцию, решаю 1 : 1,5 = 1 : х Х = 1,5 моль 10. По формуле нахожу массу меди: m = ν*MСu M Cu = 1,5моль * 64г/моль = 96г Ответ: на пластинке выделится 96г меди.

Великая битва при Бородино до сих пор не забыта народами Европы. Так кто же в ней победил? … Остаётся согласиться с мнением самого Наполеона, который считал, что в Бородинском сражении французы стали победителями, а русские – непобедимыми!

Что необходимо помнить, решая химические задачи 1. Правильно писать формулы веществ, соблюдая … 2. Не забывать выполнять закон сохранения массы вещества, т.е. … 3. Вести расчеты, используя химическое понятие… 4.При расчетах так же производить действия с … 5. Для перевода массы, объема в количество вещества использовать основные формулы:

Проверь себя 1. – степени окисления 2. расставить коэффициенты 3. - моль 4. наименованием 5. ν = m/M ν = V /Vm

Памятка решающему задачу 1. Вникни в смысл условия задачи, попытайся мысленно воспроизвести то, о чем говорится в задаче. 2. Правильно напиши уравнение реакции 3. Соблюдай закон сохранения массы вещества, расставь коэффициенты. 4. Составь пропорцию и реши уравнение

Подведение итогов 5 баллов – отметка «5» 4 балла – отметка «4»

На дом:§31 с. 103-113, задача 6 с.116

Спасибо за урок!