Презентация на тему: Реакции ионного обмена

УРОК «РЕАКЦИИ ИОННОГО ОБМЕНА» Мамлина Марина Станиславовна 245-325-357 900igr.net

Ошибка Убери лишнее. (Найдите неэлектролиты) О2 NaOH Ошибка NaCl Ошибка K2SO4 CO2 Ошибка H2SO4 CaCO3 Ошибка Mg(NO3)2 Ошибка CuCl2 BaSO4 H2O CaSO4 Cu(OH)2 SО3 Ошибка FeCl3 Ошибка NaNO3 Ошибка K2S Ошибка Ca(OH)2 Ошибка Al(NO3)3 Ошибка Na2CO3
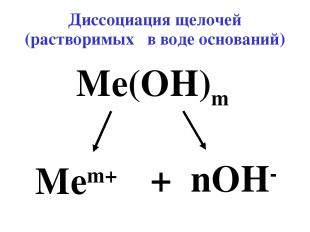
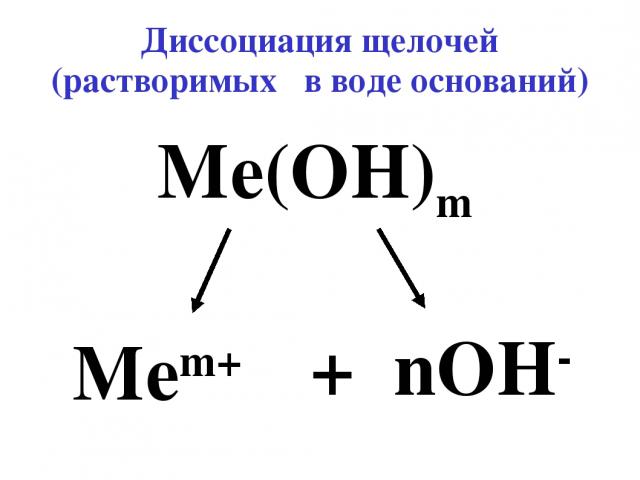
Диссоциация щелочей (растворимых в воде оснований) Me(OH)m Mem+ + nOH-
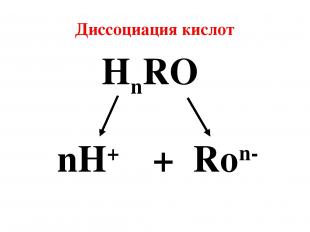
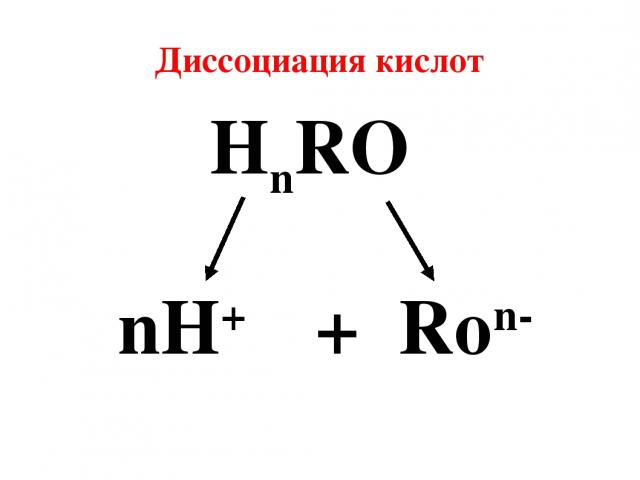
Диссоциация кислот HnRO nH+ + Ron-
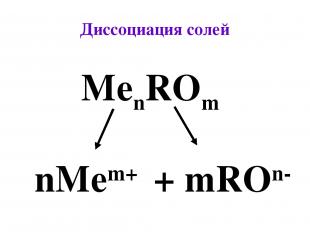
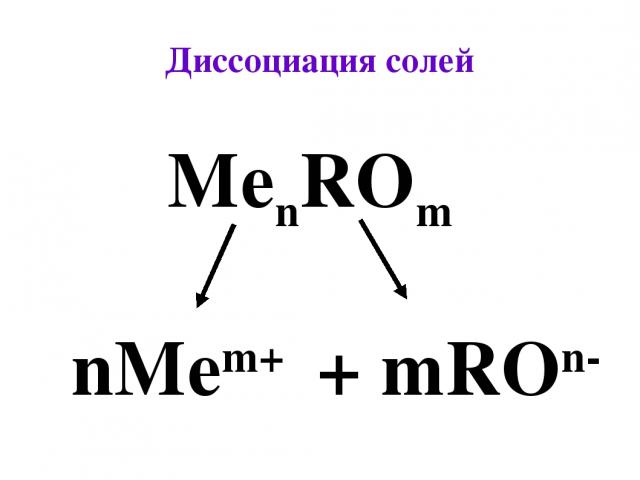
Диссоциация cолей MenROm nMem+ + mROn-

Реакции обмена
Ц И И С Р О А Н К А И О О Г М Е Р Е Б Н Н О Б К

Тема урока: Реакции ионного обмена.

Реакция ионного обмена РИО (реакции ионного обмена) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: 1. Записать уравнение реакции в молекулярном виде. BaCl2 + Na2SO4 = BaSO4 + NaCl

Реакция ионного обмена РИО (реакции ионого обмена) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: 2. Расставить коэффициенты. BaCl2 + Na2SO4 = BaSO4 + NaCl 2

Реакция ионного обмена РИО (реакции ионного обмена) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: 3. По таблице растворимости, определить нерастворимые вещества. Обозначить их стрелкой вниз. BaCl2 + Na2SO4 = BaSO4 + 2 NaCl ↓

Реакция ионного обмена РИО (реакции ионного обмена) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: Составить полное ионное уравнение (растворимые вещества расписать на ионы). BaCl2 + Na2SO4 = BaSO4 ↓ + 2 NaCl Ba2+ + 2Cl - + 2Na+ + SO4 2 - = BaSO4 ↓ + 2Na+ + 2Cl -

Реакция ионного обмена РИО (реакции ионного обмена) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: Сократить одинаковые ионы в левой и правой части полного ионного уравнения. BaCl2 + Na2SO4 = BaSO4 ↓ + 2 NaCl Ba2+ + 2Cl - + Na+ + SO4 2 - = BaSO4 ↓ + 2Na+ + 2Cl -

Реакция ионного обмена РИО (реакции ионного обмена) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: 6. Составить сокращенное ионное уравнение. BaCl2 + Na2SO4 = BaSO4 ↓ + 2 NaCl Ba2+ + 2Cl - + 2Na+ + SO4 2 - = BaSO4 ↓ + 2Na+ + 2Cl - Ba2+ + SO4 2 - = BaSO4 ↓
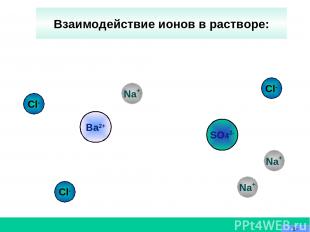
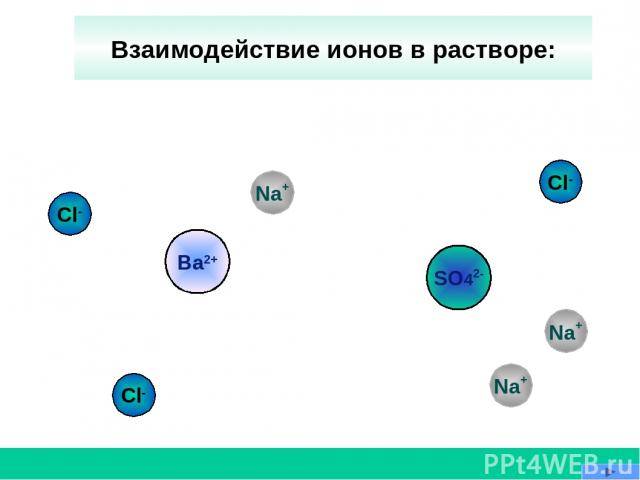
SO42- Na+ Na+ Ba2+ Cl- Cl- Cl- Взаимодействие ионов в растворе: Na+

Условия протекания реакций ионного обмена 1. Если образуется осадок. 2. Если образуется газ. CO2 Na2CO3 + H2SO4 = Na2SO4 + H2CO3 H2O 2Na+ + CO32- + 2H+ + SO42- = 2Na+ + SO42- + CO2↑+ H2O CO32- + 2Н+ = CO2↑+ H2O
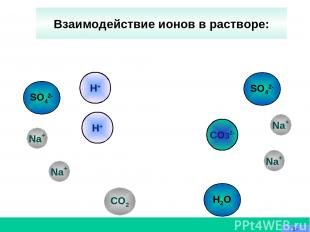
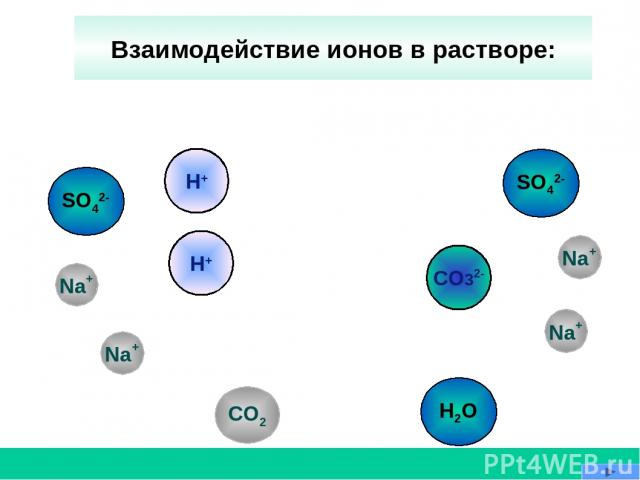
CO32- Na+ CO2 H+ SO42- Взаимодействие ионов в растворе: SO42- H2O Na+ H+ Na+ Na+

Условия протекания реакций ионного обмена 3. Если образуется вода. NaOH + H2SO4 = Na2SO4 + H2O 2 2 2Na+ + 2OH- + 2H+ + SO42 - = 2Na+ + SO42- + 2H2O 2OH- + 2H+ = 2H2O OH- + H+ = H2O Реакции нейтрализации – это реакции между щелочью и кислотой.
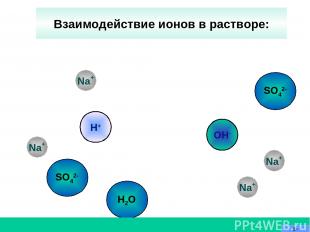
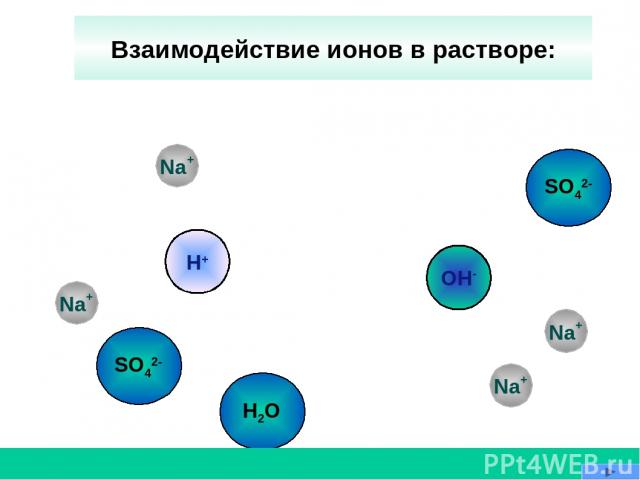
OH- Na+ Na+ H+ Н2О Взаимодействие ионов в растворе: Na+ SO42- Na+ SO42-
Тест Реакции ионного обмене – это реакции разложения замещения обмена соединения В А Б Д 1
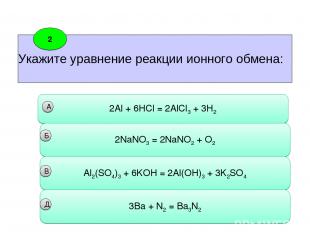
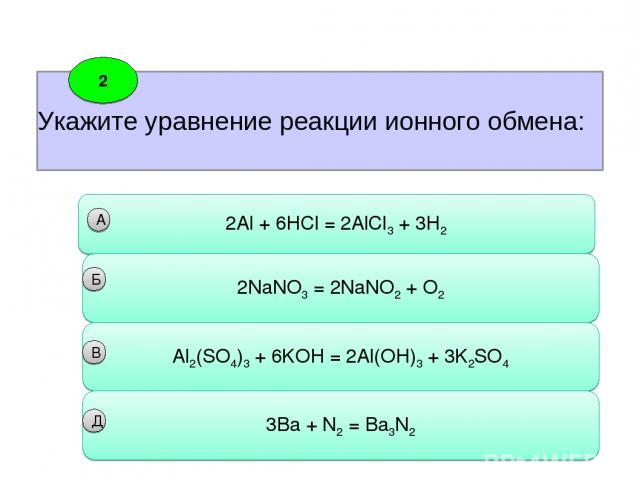
Укажите уравнение реакции ионного обмена: 2 2Al + 6HCl = 2AlCl3 + 3H2 А 2NaNO3 = 2NaNO2 + O2 Б Аl2(SO4)3 + 6KOH = 2Al(OH)3 + 3K2SO4 3Ba + N2 = Ba3N2 B Д
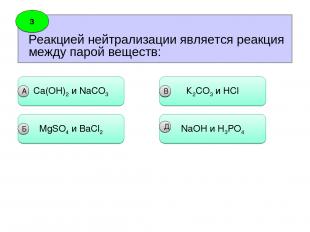
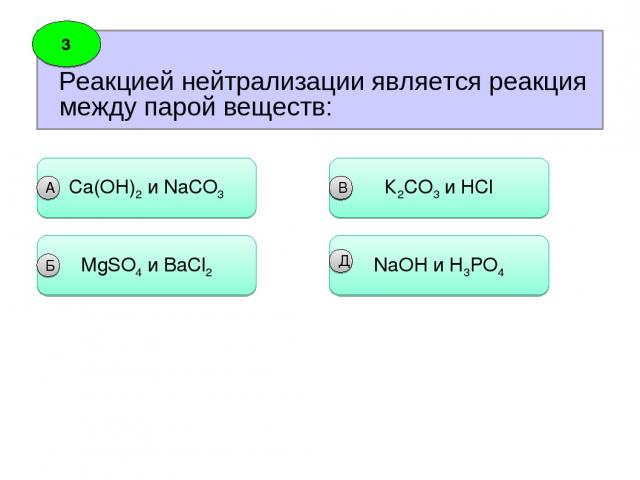
Реакцией нейтрализации является реакция между парой веществ: 3 Сa(OH)2 и NaCO3 А MgSO4 и BaCl2 Б К2СO3 и НCl В NaOH и Н3PO4 В Д
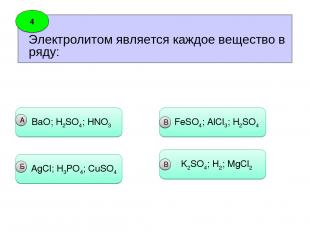
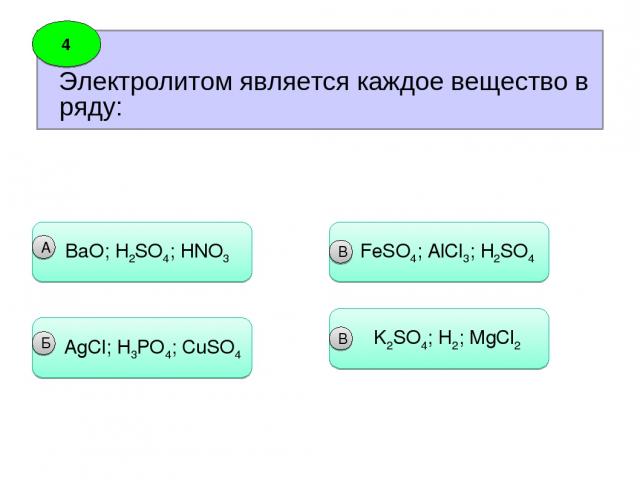
Электролитом является каждое вещество в ряду: 4 ВaO; H2SO4; HNO3 А AgCl; H3PO4; CuSO4 Б FeSO4; AlCl3; H2SO4 B K2SO4; H2; MgCl2 B

Формулы веществ, при взаимодействии которых образуется вода: 5 Fe(OH)2 и HNO3 А КOH и HNO3 Б КOH и Zn(NO3)2 B MgCO3 и Ba(NO3)2 Д

Ответы 1. В 2. В 3. Д 4. Б 5. Б

Оценка три задания правильно – «3» четыре задания правильно – «4» пять заданий правильно – «5»

Домашнее задание Составьте полные и сокращенные ионные уравнения реакций между растворами веществ: CuSO4 и KOH FeCl3 и NaOH LiOH и НС1 K2CO3 и H2SO4