Презентация на тему: Химия.Кислород


К. Шееле Дж. Пристли К. Шееле Дж. Пристли Эти два великих химика независимо друг от друга во второй половине XVIII века открыли кислород.

Антуан Лоран ЛАВУАЗЬЕ (1743-1794) Исследовал кислород и создал кислородную теорию горения, пришедшую на смену флогистонной теории.

В воздухе 21% (по объему), в земной коре 49% (по массе), в гидросфере 89% (по массе), в живых организмах до 65% массы.

Агрегатное состояние - газ при обычных условиях. При очень низких температурах (-183°С) переходит в жидкое агрегатное состояние (голубая жидкость), а при еще более низких температурах (-219°С) становится твёрдым (синие снежные кристаллы). Агрегатное состояние - газ при обычных условиях. При очень низких температурах (-183°С) переходит в жидкое агрегатное состояние (голубая жидкость), а при еще более низких температурах (-219°С) становится твёрдым (синие снежные кристаллы). Цвет – бесцветный. Запах - без запаха. Растворимость в воде - плохо растворяется. Тяжелее воздуха ( М воздуха = 29 г/моль, а МО2 = 32 г/моль.

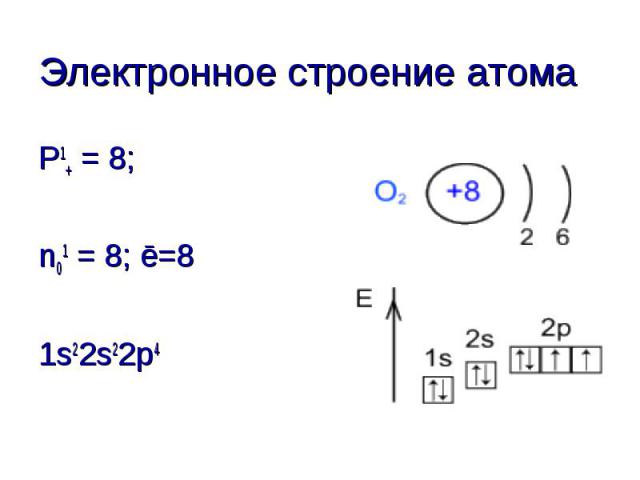
P1+ = 8; P1+ = 8; n01 = 8; ē=8 1s22s22p4

Кислород — очень сильный окислитель! Он окисляет многие вещества уже при комнатной температуре (медленное окисление) и тем более при нагревании или при горении вещества (быстрое окисление). Кислород — очень сильный окислитель! Он окисляет многие вещества уже при комнатной температуре (медленное окисление) и тем более при нагревании или при горении вещества (быстрое окисление). В реакциях со всеми элементами (кроме фтора) кислород всегда ОКИСЛИТЕЛЬ.

В результате реакции образуется оксид этого металла. Например, алюминий окисляется кислородом согласно уравнению: В результате реакции образуется оксид этого металла. Например, алюминий окисляется кислородом согласно уравнению: t° 4Al + 3O2 → 2Al2O3 Другой пример. При опускании раскалённой железной проволоки в склянку с кислородом, проволока сгорает, разбрызгивая в стороны снопы искр - раскалённых частичек железной окалины Fe3O4: t° 3Fe + 2O2 → Fe3O4

Образуется оксид неметалла. Образуется оксид неметалла. Горение фосфора с образованием оксида фосфора (V): t° 4Р + 5О2 → 2Р2О5

Горение серы в кислороде с образованием сернистого газа SO2: Горение серы в кислороде с образованием сернистого газа SO2: t° S + O2 → SO2 Горение угля в кислороде с образованием углекислого газа: t° С + О2 → СО2

В этом случае образуются оксиды элементов, из которых состоит молекула сложного вещества. В этом случае образуются оксиды элементов, из которых состоит молекула сложного вещества. Например, при обжиге сульфида меди (II) t° 2CuS + 3O2 → 2CuO + 2SO2 образуются два оксида — оксид меди (II) и оксид серы (IV). При обжиге сульфидов образуется всегда оксид серы, валентность серы в котором равна IV. Другой пример — горение метана СН4. Так как эта молекула состоит из атомов элементов углерода С и водорода Н, значит, образуется два оксида — оксид углерода (IV) СО2 и оксид водорода, то есть вода - Н2О: t° СН4 + 2О2 → СО2 + 2Н2О

Химическое взаимодействие вещества с кислородом называется реакцией окисления. Химическое взаимодействие вещества с кислородом называется реакцией окисления. Реакции окисления, сопровождающиеся выделением теплоты и света, называются реакциями горения. Реакции горения веществ — это примеры быстрого окисления, а вот гниение, ржавление и т.п. — это примеры медленного окисления веществ кислородом

разложение воды электрическим током разложение воды электрическим током разложение пероксида водорода Н2О2 под действием катализатора MnO2 разложение перманганата калия KMnO4 при нагревании.

В промышленности для получения чистого кислорода используют перегонку жидкого воздуха, основанную на разных температурах кипения компонентов воздуха. Воздух охлаждают примерно до -200°С и затем медленно нагревают. При достижении температуры -183°С из жидкого воздуха улетучивается кислород, остальные компоненты сжиженного воздуха при этой температуре остаются в жидком агрегатном состоянии. В промышленности для получения чистого кислорода используют перегонку жидкого воздуха, основанную на разных температурах кипения компонентов воздуха. Воздух охлаждают примерно до -200°С и затем медленно нагревают. При достижении температуры -183°С из жидкого воздуха улетучивается кислород, остальные компоненты сжиженного воздуха при этой температуре остаются в жидком агрегатном состоянии.

в строительстве и машиностроении - для кислородно - ацетиленовой газосварки и газорезки металлов - для напыления и наплавки металлов в нефтедобыче - при закачке в пласт для повышения энергии вытеснения в металлургии и горнодобывающей промышленности - при конвективном производстве стали, кислородном дутье в доменных печах, извлечение золота и руд, производстве ферросплавов, выплавке никеля, цинка свинца, циркония и др. цветных металлов - при прямом восстановлении железа - при огневой зачистке в литейном производстве - при огневом бурении твердых пород

в медицине в медицине - в оксибарокамерах - при заправке кислородных масок, подушек и т.д. - в палатах со специальным микроклиматом - для изготовления кислородных коктейлей - при выращивании микроорганизмов в экологии - при очистке питьевой воды - при вторичной переработке металлов - при продувке сточных вод кислородом - при обезвреживании химически активных отходов в очистных установках в мусоросжигательных печах

в химической промышленности в химической промышленности - при производстве ацетилена, целлюлозы, метилового спирта, аммиака, азотной и серной кислоты - при каталитической конверсии природного газа (при производстве синтетического аммиака) - при высокотемпературной конверсии метана в энергетике - при газификации твердого топлива - для обогащения воздуха для бытовых и промышленных котлов - для сжатия водно-угольной смеси

в военной технике в военной технике - в барокамерах - для работы дизельных двигателей под водой - в качестве окислителя топлива для ракетных двигателей в сельском хозяйстве - для обогащения кислородом водной среды в рыболовстве - при изготовлении кислородных коктейлей - для прибавки животных в весе

Озон О3 - газ голубого цвета с резким запахом. Каждый, кто обратил внимание на то, как пахнет воздух после грозы или вблизи источника электрического разряда, знает запах этого газа очень хорошо. Озон О3 - газ голубого цвета с резким запахом. Каждый, кто обратил внимание на то, как пахнет воздух после грозы или вблизи источника электрического разряда, знает запах этого газа очень хорошо. В природе озон образуется под действием ультрафиолетового излучения Солнца, а также получается при электрических разрядах в атмосфере:

Озон - очень сильный окислитель, поэтому его используют при обеззараживании питьевой воды. При контакте с большинством способных окисляться веществ происходит взрыв. Озон - очень сильный окислитель, поэтому его используют при обеззараживании питьевой воды. При контакте с большинством способных окисляться веществ происходит взрыв. Озон образуется в атмосфере Земли на высоте 25 км под действием солнечной радиации, он поглощает опасное излучение Солнца. Однако в озоновом "зонтике" Земли, толщиной всего около 30 метров, то и дело возникают "дыры". В воздух попадает все больше "вредных" для озона газов, вроде монооксида азота NO или тех веществ, которые используются для наполнения холодильных установок и аэрозольных баллончиков. Даже частичное исчезновение озонового слоя над Землей грозит всему живому гибелью...