Презентация на тему: ХИМИЯ В БЫТУ


1.Углеродное волокно 1.Углеродное волокно ♦ получение ♦ применение 2.Тефлон ♦ свойства 3.Фосфор ♦получение 4.Сода ♦ примечание

Углеродное волокно — материал, состоящий из тонких нитей диаметром от 3 до 15 микрон, образованных преимущественно атомами углерода. Атомы углерода объединены в микроскопические кристаллы, выровненные параллельно друг другу. Выравнивание кристаллов придает волокну большую прочность на растяжение. Углеродные волокна характеризуются высокой силой натяжения, низким удельным весом, низким коэффициентом температурного расширения и химической инертностью. Углеродное волокно — материал, состоящий из тонких нитей диаметром от 3 до 15 микрон, образованных преимущественно атомами углерода. Атомы углерода объединены в микроскопические кристаллы, выровненные параллельно друг другу. Выравнивание кристаллов придает волокну большую прочность на растяжение. Углеродные волокна характеризуются высокой силой натяжения, низким удельным весом, низким коэффициентом температурного расширения и химической инертностью.
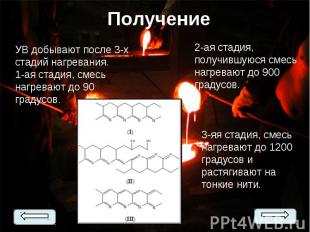

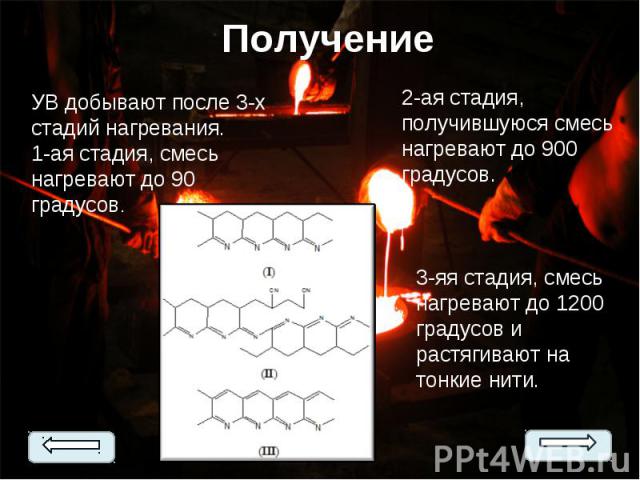
УВ нашло свое применение в машиностроении из-за своих свойств. УВ нашло свое применение в машиностроении из-за своих свойств. УВ обычно получают термической обработкой химических или природных органических волокон, при которой в материале волокна остаются главным образом атомы углерода.

Тефлон применяют в химической, электротехнической и пищевой промышленности, в медицине, в транспортных средствах, в военных целях, в основном в качестве покрытий. Наибольшую известность тефлон получил благодаря широкому применению в производстве посуды с антипригарным покрытием. Тефлон применяют в химической, электротехнической и пищевой промышленности, в медицине, в транспортных средствах, в военных целях, в основном в качестве покрытий. Наибольшую известность тефлон получил благодаря широкому применению в производстве посуды с антипригарным покрытием.

Физические Физические Тефлон — белое, в тонком слое прозрачное вещество, по виду напоминающее парафин или полиэтилен. Обладает высокой тепло- и морозостойкостью, остается гибким и эластичным при температурах от -70 до +270 °C, прекрасный изоляционный материал. Химические По своей химической стойкости превышает все известные синтетические материалы и благородные металлы. Не разрушается под влиянием щелочей, кислот и даже смеси азотной и соляной кислот. Разрушается расплавами щелочных металлов, фтороми трифторидом хлора.

Самый распространенный способ применения в быту фосфора, а именно красного фосфора – это спички. Он используется на чиркалке и на самой палочек. Самый распространенный способ применения в быту фосфора, а именно красного фосфора – это спички. Он используется на чиркалке и на самой палочек.

Красный фосфор получают в лабораторных условиях при возгорании белого фосфора без доступа Красный фосфор получают в лабораторных условиях при возгорании белого фосфора без доступа воздуха.

Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) —кислая соль угольной кислоты и натрия. Обыкновенно представляет собой мелкокристаллический порошок белого цвета. Используется в пищевой промышленности, в кулинарии, в медицине как нейтрализатор ожогов кожи человека кислотами и снижения кислотности желудочного сока. Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) —кислая соль угольной кислоты и натрия. Обыкновенно представляет собой мелкокристаллический порошок белого цвета. Используется в пищевой промышленности, в кулинарии, в медицине как нейтрализатор ожогов кожи человека кислотами и снижения кислотности желудочного сока.

Сода, из-за своих соединений, очень опасна в плане взрывоопасности. При взаимодействии с огнем, сода начинает воспламеняться или же взрываться. Сода, из-за своих соединений, очень опасна в плане взрывоопасности. При взаимодействии с огнем, сода начинает воспламеняться или же взрываться.

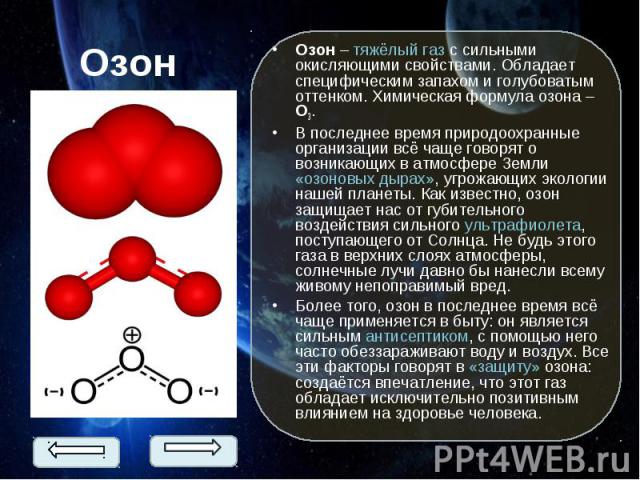
Озон – тяжёлый газ с сильными окисляющими свойствами. Обладает специфическим запахом и голубоватым оттенком. Химическая формула озона – О3. Озон – тяжёлый газ с сильными окисляющими свойствами. Обладает специфическим запахом и голубоватым оттенком. Химическая формула озона – О3. В последнее время природоохранные организации всё чаще говорят о возникающих в атмосфере Земли «озоновых дырах», угрожающих экологии нашей планеты. Как известно, озон защищает нас от губительного воздействия сильного ультрафиолета, поступающего от Солнца. Не будь этого газа в верхних слоях атмосферы, солнечные лучи давно бы нанесли всему живому непоправимый вред. Более того, озон в последнее время всё чаще применяется в быту: он является сильным антисептиком, с помощью него часто обеззараживают воду и воздух. Все эти факторы говорят в «защиту» озона: создаётся впечатление, что этот газ обладает исключительно позитивным влиянием на здоровье человека.

Тем не менее, при всей своей опасности, озон нередко можно встретить в нашей повседневной жизни. Он является сильным окислителем: с помощью него можно стерилизовать медицинские приборы, отбеливать ткани и бумагу, стерилизовать помещения. На основе озона производятся некоторые медицинские препараты, так что он уже успел внести неплохой вклад в наше здоровье. Тем не менее, при всей своей опасности, озон нередко можно встретить в нашей повседневной жизни. Он является сильным окислителем: с помощью него можно стерилизовать медицинские приборы, отбеливать ткани и бумагу, стерилизовать помещения. На основе озона производятся некоторые медицинские препараты, так что он уже успел внести неплохой вклад в наше здоровье.

• Однако право использовать озон в медицине до сих пор оспаривается. Существует отдельное направление в лечении, которое так и называется – «озонотерапия». Это метод физиотерапевтического воздействия на организм с применением озона, получаемого с помощью медицинского озонатора из кислорода. Некоторые врачи утверждают, что этот «тяжёлый газ» может применяться и внутривенно, и экстракорпорально, при этом принося немалую пользу человеку. • Однако право использовать озон в медицине до сих пор оспаривается. Существует отдельное направление в лечении, которое так и называется – «озонотерапия». Это метод физиотерапевтического воздействия на организм с применением озона, получаемого с помощью медицинского озонатора из кислорода. Некоторые врачи утверждают, что этот «тяжёлый газ» может применяться и внутривенно, и экстракорпорально, при этом принося немалую пользу человеку. • Существуют и противники этого мнения, говорящие совершенно обратное: озон, введённый в организм, может вызывать у человека мутации и осложнения уже существующих болезней. Как минимум, от озона просто не будет никакого эффекта, а это значит, что лекарственные препараты с его содержанием совершенно бессмысленны. • В большинстве стран в государственных больницах озонотерапия уже не приветствуется. В частных клиниках она всё ещё возможна, но больной должен быть проинформирован о возможных последствиях и дать своё письменное согласие на лечение.

Аммиак — это бесцветный газ с очень резким запахом. Длительное вдыхание аммиака может вызвать смерть. Незначительные количества аммиака присутствуют в воздухе при разложении животных и растительности. В незначительных количествах он может входить в состав дождевой воды. Аммиак — это бесцветный газ с очень резким запахом. Длительное вдыхание аммиака может вызвать смерть. Незначительные количества аммиака присутствуют в воздухе при разложении животных и растительности. В незначительных количествах он может входить в состав дождевой воды.

• После сжатия и охлаждения аммиак превращается в жидкость, напоминающую воду, но кипящую при температуре минус 34° С. По окончании сжатия аммиак испаряется. При этом он поглощает много тепла. Вот почему его используют в холодильниках. • После сжатия и охлаждения аммиак превращается в жидкость, напоминающую воду, но кипящую при температуре минус 34° С. По окончании сжатия аммиак испаряется. При этом он поглощает много тепла. Вот почему его используют в холодильниках. • Аммиак «домашнего применения», который может быть у тебя дома — это водный раствор аммиака. Его добавляют в воду во время стирки.

• Хлорид аммония применяется в сварке, при изготовлении сухих источников питания и в медицине. • Хлорид аммония применяется в сварке, при изготовлении сухих источников питания и в медицине. • Сульфат аммония является хорошим удобрением. Нитрат аммония используется как удобрение и как взрывчатое вещество.

• В медицине 10 % раствор аммиака, чаще называемый нашатырным спиртом, применяется при обморочных состояниях (для возбуждения дыхания), для стимуляции рвоты, а также наружно — невралгии, миозиты, укусах насекомых, для обработки рук хирурга. При неправильном применении может вызвать ожоги пищевода и желудка (в случае приёма неразведённого раствора) Нашатырный спирт также содержит карбонат аммония. • В медицине 10 % раствор аммиака, чаще называемый нашатырным спиртом, применяется при обморочных состояниях (для возбуждения дыхания), для стимуляции рвоты, а также наружно — невралгии, миозиты, укусах насекомых, для обработки рук хирурга. При неправильном применении может вызвать ожоги пищевода и желудка (в случае приёма неразведённого раствора) Нашатырный спирт также содержит карбонат аммония. • Пары нашатырного спирта способны изменять окраску цветов. Например, голубые и синие лепестки становятся зелеными, ярко красные — черными.

• Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать. Например, приятный аромат приобретают астры. • Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать. Например, приятный аромат приобретают астры. • Облака Юпитера состоят из аммиака.

Известь (из греч. ἄσβεστος «неугасимый») — материал, получаемый путем обжига (не до расплава) карбонатных горных пород (известняков, мела). По химическому составу она почти полностью состоит из свободных оксидов кальция и магния с преимущественным содержанием СаО. Применяется в строительстве, а также для получения различных химических веществ, некоторые из которых также носят название «известь». Известь (из греч. ἄσβεστος «неугасимый») — материал, получаемый путем обжига (не до расплава) карбонатных горных пород (известняков, мела). По химическому составу она почти полностью состоит из свободных оксидов кальция и магния с преимущественным содержанием СаО. Применяется в строительстве, а также для получения различных химических веществ, некоторые из которых также носят название «известь».

Оксид кальция — белое кристаллическое вещество, кристаллизующееся в кубической гранецентрированной кристаллической решетке, по типу хлорида натрия. Оксид кальция — белое кристаллическое вещество, кристаллизующееся в кубической гранецентрированной кристаллической решетке, по типу хлорида натрия.

• Основные объёмы используются в строительстве при производстве Силикатного кирпича. Раньше известь, так же использовали в качестве известкового цемента. Однако в настоящее время известковый цемент при строительстве жилых домов стараются не применять, так как полученные строения обладают способностью впитывать и накапливать сырость. • Основные объёмы используются в строительстве при производстве Силикатного кирпича. Раньше известь, так же использовали в качестве известкового цемента. Однако в настоящее время известковый цемент при строительстве жилых домов стараются не применять, так как полученные строения обладают способностью впитывать и накапливать сырость. • Категорически недопустимо использование известкового цемента при кладке печей — из-за термического разложения и выделения в воздух удушливого диоксида углерода. • Некоторое применение также находит в качестве доступного и недорогого огнеупорного материала.

• В небольших количествах оксид кальция также используется в лабораторной практике для осушения веществ, которые не реагируют с ним. • В небольших количествах оксид кальция также используется в лабораторной практике для осушения веществ, которые не реагируют с ним. • В пищевой промышленности зарегистрирован в качестве пищевой добавки E-529. • В промышленности для удаления диоксида серы из дымовых газов, как правило используют 15 % водяной раствор. • Так же используется в «самогреющей» посуде.

Химическое вещество, сильное основание. Представляет собой порошок белого цвета, плохо растворимый в воде. Химическое вещество, сильное основание. Представляет собой порошок белого цвета, плохо растворимый в воде. Гидроксид кальция является довольно сильным основанием, из-за чего водный раствор имеет щелочную реакцию. Растворимость падает с ростом температуры. Гашёная известь — так как её получают путём «гашения»

• При побелке помещений. • При побелке помещений. • При побелке деревянных заборов и обмазывании стропил — для защиты от гниения и возгорания. • Для приготовления известкового строительного раствора. • Для приготовления силикатного бетона. Состав силикатного бетона одинаков с составом известкового строительного раствора, однако он готовится другим методом.

• Для устранения карбонатной жёсткости воды (умягчение воды). Реакция идёт по уравнению: Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O. • Для устранения карбонатной жёсткости воды (умягчение воды). Реакция идёт по уравнению: Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O. • Для производства хлорной извести. • Для производства известковых удобрений. • Каустификация карбоната натрия и калия. • Дубление кож. • В пищевой промышленности зарегистрирован в качестве пищевой добавки E526.

• Известковая вода — прозрачный раствор гидроксида кальция. Она используется для обнаружения углекислого газа. При взаимодействии с ним она мутнеет, так как образуется нерастворимый карбонат кальция: Ca(OH)2 + CO2 → CaCO3↓ + H2O. • Известковая вода — прозрачный раствор гидроксида кальция. Она используется для обнаружения углекислого газа. При взаимодействии с ним она мутнеет, так как образуется нерастворимый карбонат кальция: Ca(OH)2 + CO2 → CaCO3↓ + H2O. • Известковое молоко — взвесь (суспензия) гидроксида кальция в воде, белая и непрозрачная. Она используется для производства сахара и приготовления смесей для борьбы с болезнями растений, побелки стволов.

• В стоматологии — для дезинфекции корневых каналов зубов. • В стоматологии — для дезинфекции корневых каналов зубов.

Спасибо за внимание Спасибо за внимание