Презентация на тему: Химическая связь

Химическая связь Учитель МОБУ СОШ ЛГО с.Пантелеймоновка Г.П. Яценко

Химическая связь. Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы.
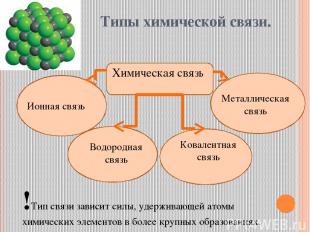
Типы химической связи. Химическая связь Ионная связь Металлическая связь Водородная связь Ковалентная связь !Тип связи зависит силы, удерживающей атомы химических элементов в более крупных образованиях.
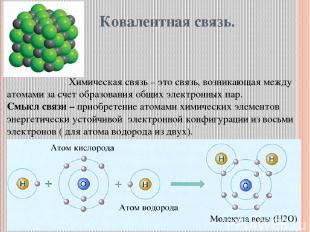
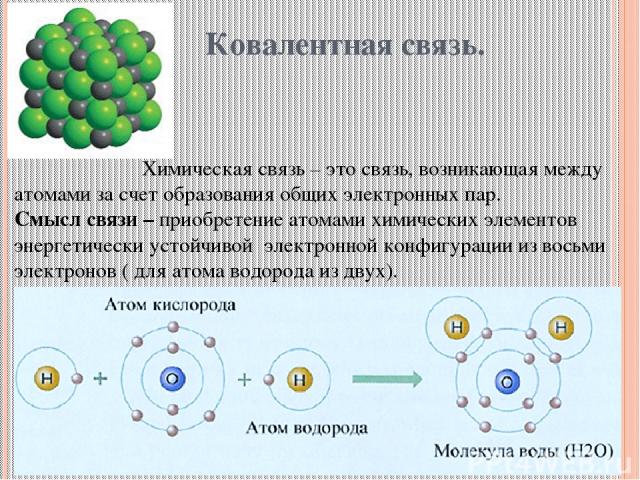
Ковалентная связь. Химическая связь – это связь, возникающая между атомами за счет образования общих электронных пар. Смысл связи – приобретение атомами химических элементов энергетически устойчивой электронной конфигурации из восьми электронов ( для атома водорода из двух).
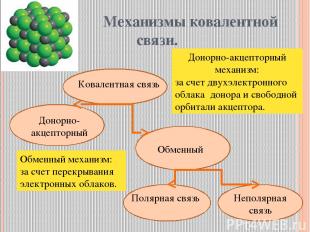
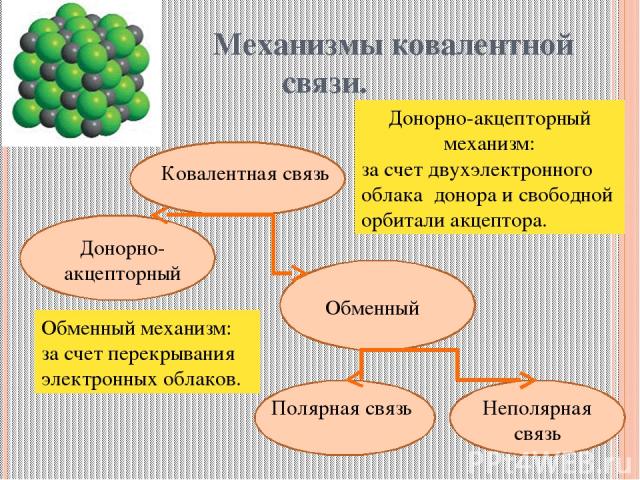
Механизмы ковалентной связи. Ковалентная связь Донорно-акцепторный Обменный Полярная связь Неполярная связь Обменный механизм: за счет перекрывания электронных облаков. Донорно-акцепторный механизм: за счет двухэлектронного облака донора и свободной орбитали акцептора.
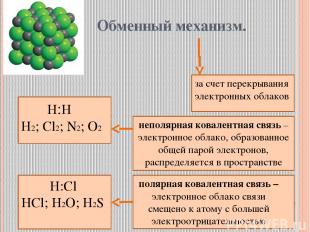
Обменный механизм. за счет перекрывания электронных облаков Н:Н Н2; Cl2; N2; O2 неполярная ковалентная связь – электронное облако, образованное общей парой электронов, распределяется в пространстве Н:Cl HCl; H2O; H2S полярная ковалентная связь – электронное облако связи смещено к атому с большей электроотрицательностью

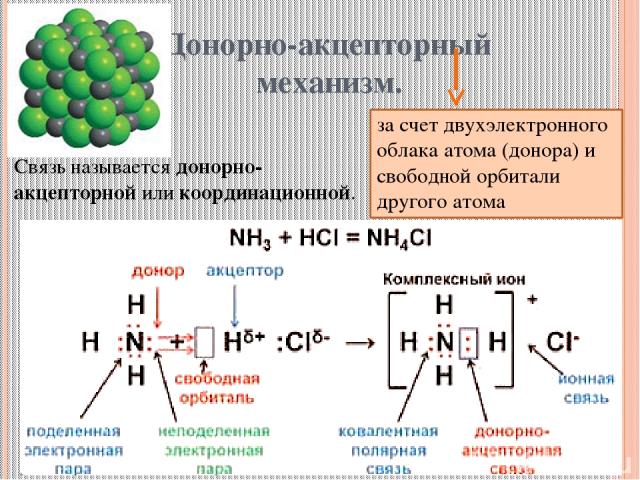
Донорно-акцепторный механизм. за счет двухэлектронного облака атома (донора) и свободной орбитали другого атома (акцептора) Связь называется донорно-акцепторной или координационной.
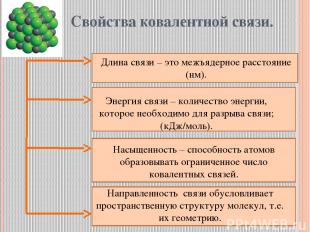
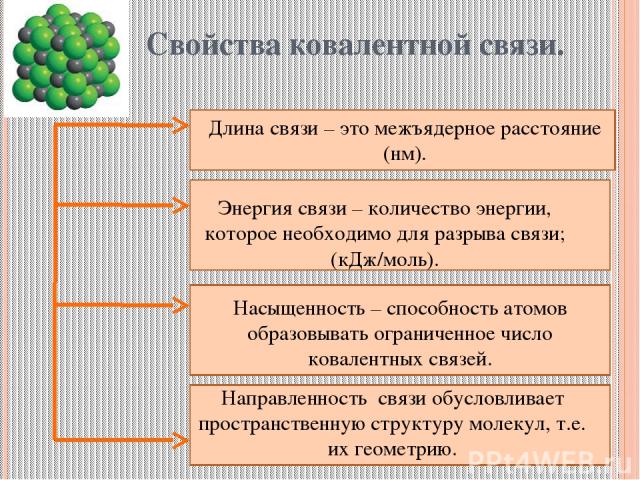
Свойства ковалентной связи. Длина связи – это межъядерное расстояние (нм). Энергия связи – количество энергии, которое необходимо для разрыва связи; (кДж/моль). Насыщенность – способность атомов образовывать ограниченное число ковалентных связей. Направленность связи обусловливает пространственную структуру молекул, т.е. их геометрию.

Способы перекрывания электронных облаков. σ– связь – перекрывание электронных облаков вдоль оси, соединяющей центры атомов. π – связь, возникающая между атомами, когда перекрывание электронных облаков происходит по обе стороны от линии, соединяющей ядра обоих атомов. S-S S - P P - P P - P

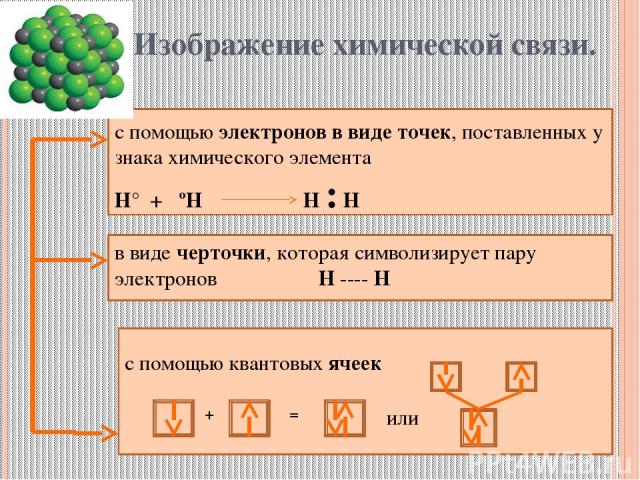
Изображение химической связи. с помощью электронов в виде точек, поставленных у знака химического элемента Н° + ºН Н : Н в виде черточки, которая символизирует пару электронов Н ---- Н с помощью квантовых ячеек + = или
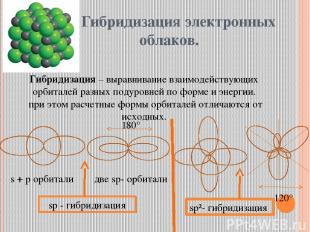
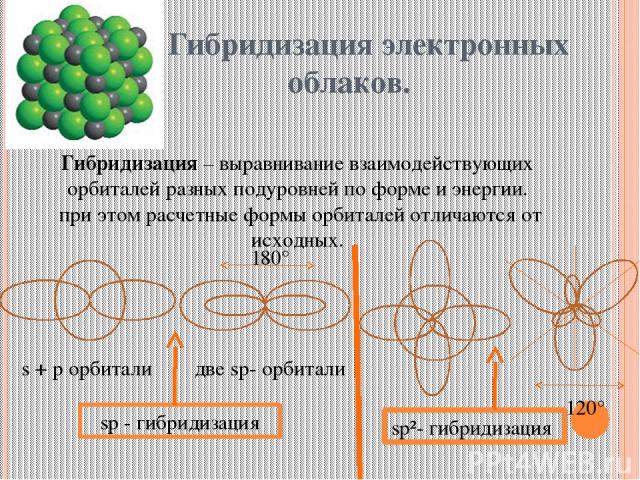
Гибридизация электронных облаков. Гибридизация – выравнивание взаимодействующих орбиталей разных подуровней по форме и энергии. при этом расчетные формы орбиталей отличаются от исходных. s + p орбитали две sp- орбитали sp - гибридизация 180° 120° sp²- гибридизация
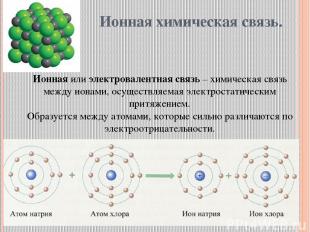
Ионная химическая связь. Ионная или электровалентная связь – химическая связь между ионами, осуществляемая электростатическим притяжением. Образуется между атомами, которые сильно различаются по электроотрицательности.
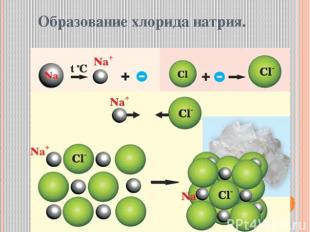
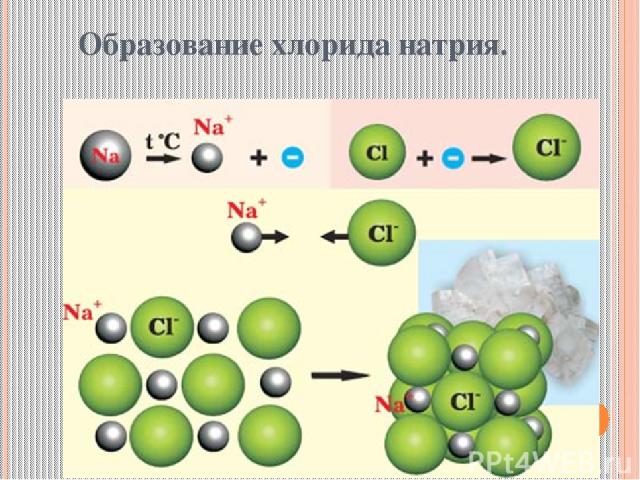
Образование хлорида натрия.
Свойства ионной химической связи. Ненаправленность. Каждый ион, представляющий как бы заряженный шар, может притягивать ион противоположного знака по любому направлению. Ненасыщаемость. Взаимодействие ионов противоположного знака не приводит к компенсации силовых полей способность притягивать по другим по другим направлениям остается.
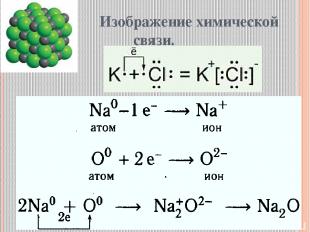
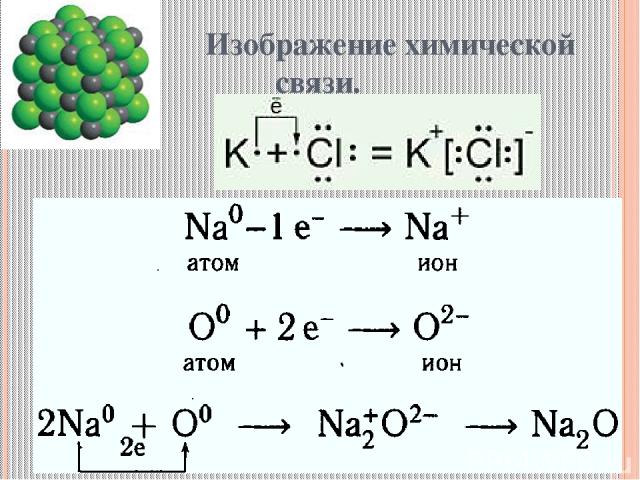
Изображение химической связи.

Полярные молекулы вещества. Молекулы при общей нейтральности представляют собой электрический диполь. Поляризуемость – способность атомов, ионов и молекул приобретать дипольный момент (μ ) в электрическом поле. μ = q · Ɩ электрический момент диполя. Мера полярности связи и молекулы. Выражается в Кл·м (Кулон-метр).

Неполярные молекулы. μ = 0 Молекулы, содержащие неполярную ковалентную связь – электронное облако симметрично по отношению к ядрам обоих атомов. Например: Н2 ; О2; F2; Cl2 и др.

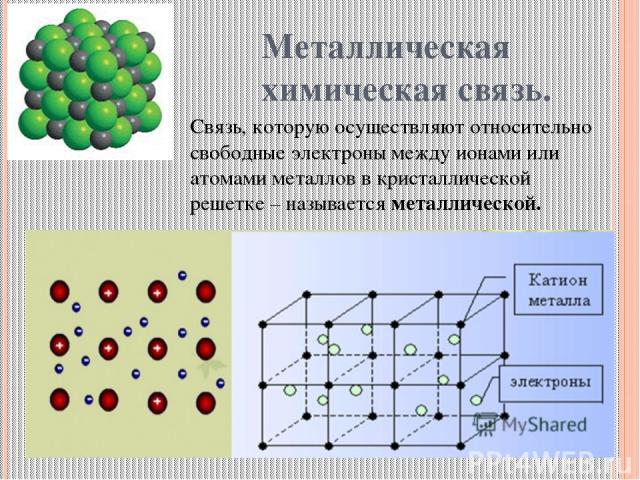
Металлическая химическая связь. Связь, которую осуществляют относительно свободные электроны между ионами или атомами металлов в кристаллической решетке – называется металлической.

Особенности металлической связи. 1. Металлическую связь образуют элементы, атомы которых на внешнем уровне имеют мало валентных электронов по сравнению с общим числом внешних энергетически близких орбиталей. Валентные электроны из-за небольшой энергии ионизации слабо удерживаются в атоме. Электроны, осуществляющие связь, обобществлены («электронный газ») и перемещаются по всему куску металла, в целом электронейтрального. Металлическая связь характерна для металлов твердом и жидком состоянии.
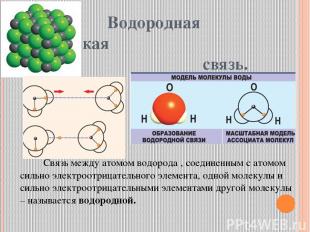
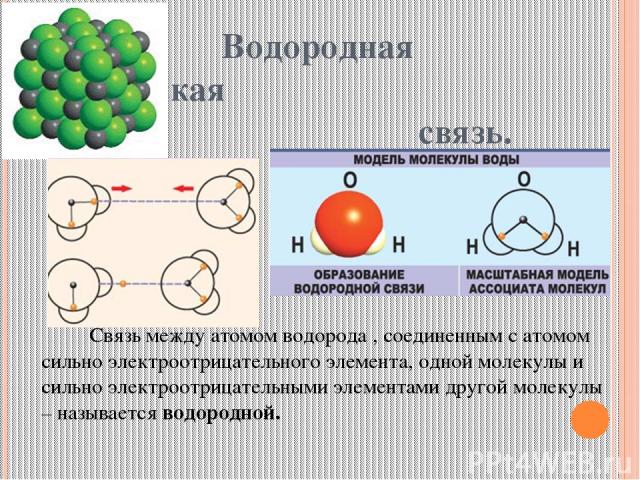
Водородная химическая связь. Связь между атомом водорода , соединенным с атомом сильно электроотрицательного элемента, одной молекулы и сильно электроотрицательными элементами другой молекулы – называется водородной.

Особенности водородной химической связи. Связь относится к межмолекулярной; возможно образование внутримолекулярной водородной связи. Водородная связь вторая по образованию в веществе, поэтому более слабая. Тем не менее она ответственна за ассоциацию молекул. Водородная связь оказывает влияние на свойства вещества, т.к. нужна дополнительная энергия для разрыва водородной связи.
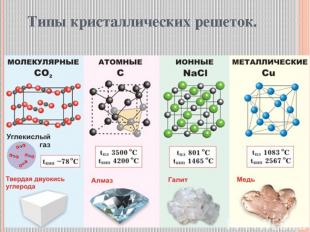
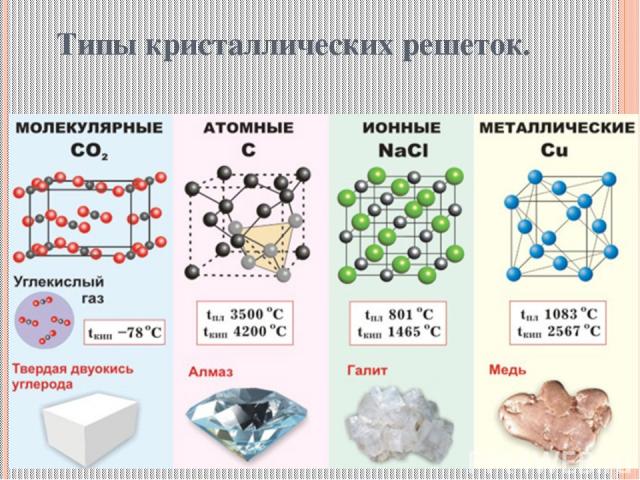
Типы кристаллических решеток.

Информация для педагога. Ресурс предназначен для учащихся 11 класса. Является иллюстрацией при освоении темы «Химическая связь». В презентации рассматриваются основные понятия темы, графическое изображение механизмов образования химических связей Материал может быть фрагментарно использован на уроках химии в 8 – 9 классах. Цор подходит для проведения дистанционного обучения. Ресурс рассчитан на использование УМК О.С. Габриеляна.

Материалы, используемые для оформления. http://elementy.ru/images/eltbook/chemical_bonds_rus1_720.jpg http://www.varson.ru/images/Himia_jpeg_big/2-10.jpg http://www.varson.ru/images/Himia_jpeg_big/2-11.jpg http://konspekta.net/studopediaorg/baza4/733777796720.files/image774.jpg http://images.myshared.ru/277791/slide_4.jpg https://upload.wikimedia.org/wikipedia/commons/thumb/0/06/Sigma_bond.svg/250px-Sigma_bond.svg.png http://arhe.msk.ru/wp-content/uploads/2014/03/17882_html_670f366a-335x230.png http://estnauki.ru/images/stories/water_molekula.jpg https://encrypted-tbn3.gstatic.com/images?q=tbn:ANd9GcTxFRG_40yv33-EqH9Ue_BtfBz5GQided0BtUHE_wRtFWVvD1Zc http://distant-lessons.ru/wp-content/uploads/2013/12/donorno-akceptornaja-kovalentnaja-svyaz.jpg