Презентация на тему: Химическая связь

Химическая связь

Цель урока: Вскрыть причину образования химической связиАктуализировать знания о видах химической связиПоказать относительный характер ее классификации.

Причиной образования химической связи является стремление системы к минимуму энергии: при её образовании, как правило, энергия выделяется, образующаяся система обладает меньшей энергией, чем изолированные атомы.Происходит уменьшение энергии на величину энергии связи(Есв.). Энергия связи (Есв.)- энергия, необходимая для разрушения этой связи.

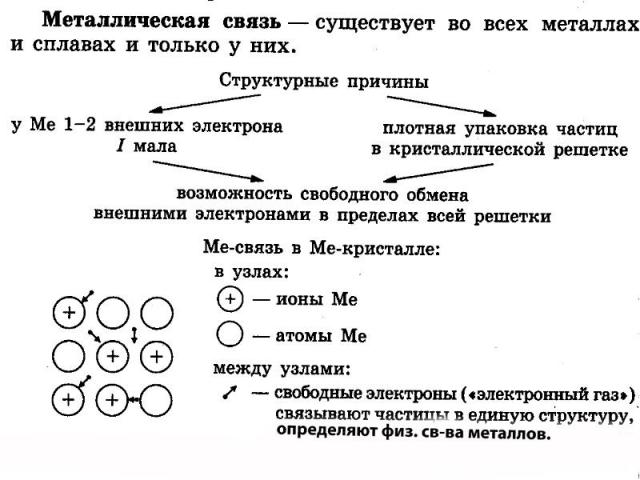
Химическая связь- взаимодействие между атомами, приводящее к образованию устойчивой системы- молекулы, иона, кристалла.

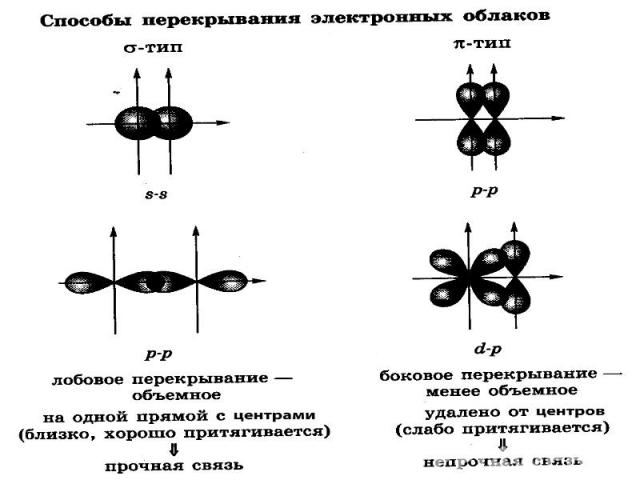
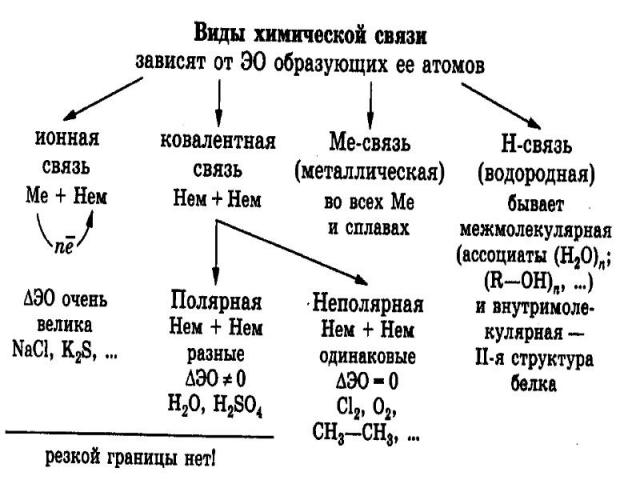
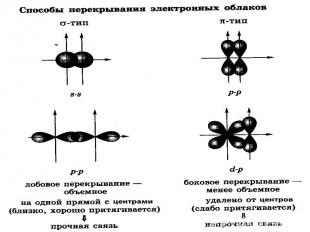
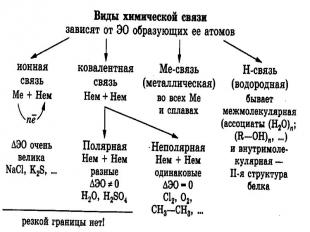
Ковалентная связь- связь между атомами, возникающая за счёт образования общих электронных пар. Способы образования общей электронной пары:- двумя неспаренными электронами-обменный механизм:А . + .В = А : В или А-В (1:1)-электронной парой и свободной орбиталью- донорно- акцепторный механизм:А: + В= А : В или А-В (2:0)

Полярность ковалентной связиОна определяется разницей значений э.о связанных атомов.


Ионная связь- электростатическое притяжение между ионами.Ионных соединений немного: элементы + элементы I и IIгр. гл. подгр. VI и VII гр. гл. подгр.Если значение э.о >= 2,то связь считают ионной.Если же значение э.о <2,то ковалентной полярной.Чёткой границы между ионной и ковалентной полярной связью НЕТ.
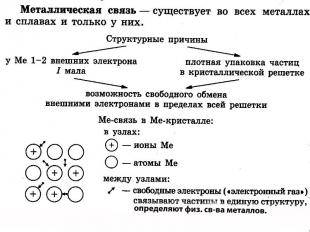

Водородная связь- электростатической притяжение между положительно поляризованными атомами водорода одной молекулы и отрицательно поляризованными атомами( F,O,N, реже S,Cl) другой молекулы.

Водородная связь бывает:МежмолекулярнаяВнутримолекулярная

Параграф 6, упражнение 4(стр. 56) Домашнее задание: