Презентация на тему: Химическая связь

ХИМИЧЕСКАЯ СВЯЗЬ План. 1.Электронная теория химической связи. 2. Ковалентная связь. Полярность связи, дипольный момент. 3. Ионная связь. Оценка степени ионности связи. 4. Донорно-акцепторный механизм образования ковалентной связи. 5. Водородная связь. 6. Силы межмолекулярного взаимодействия. По выражению г-на Брайка Кроуфорда мл. « Вопрос о природе химической связи – сердце всей химии (1953)
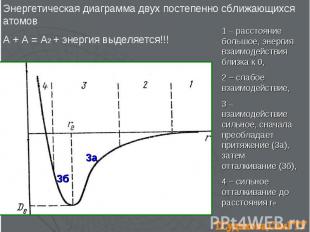
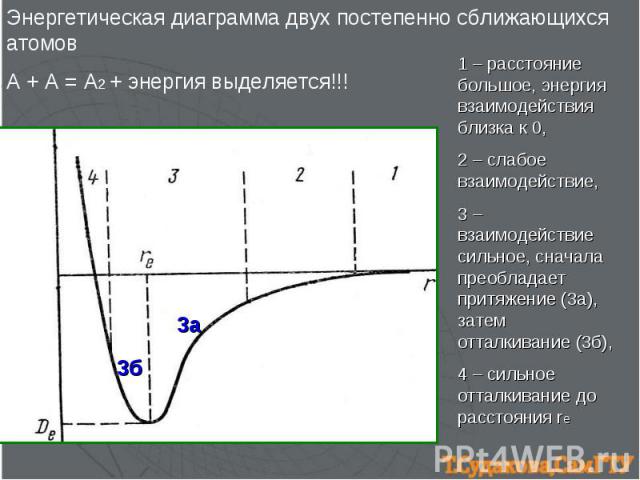
Энергетическая диаграмма двух постепенно сближающихся атомов А + А = А2 + энергия выделяется!!! 1 – расстояние большое, энергия взаимодействия близка к 0, 2 – слабое взаимодействие, 3 – взаимодействие сильное, сначала преобладает притяжение (3а), затем отталкивание (3б), 4 – сильное отталкивание до расстояния re 3а 3б

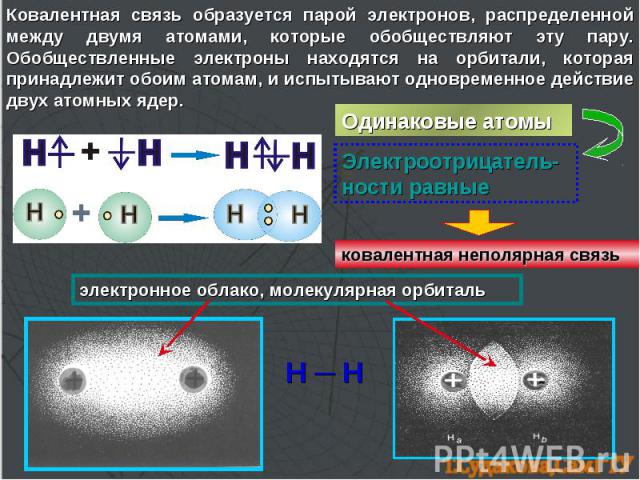
Ковалентная связь образуется парой электронов, распределенной между двумя атомами, которые обобществляют эту пару. Обобществленные электроны находятся на орбитали, которая принадлежит обоим атомам, и испытывают одновременное действие двух атомных ядер. Одинаковые атомы Электроотрицатель-ности равные ковалентная неполярная связь электронное облако, молекулярная орбиталь Н ─ Н
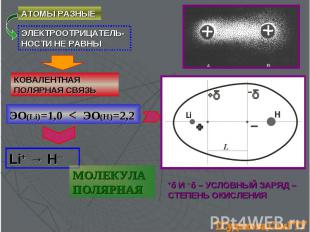
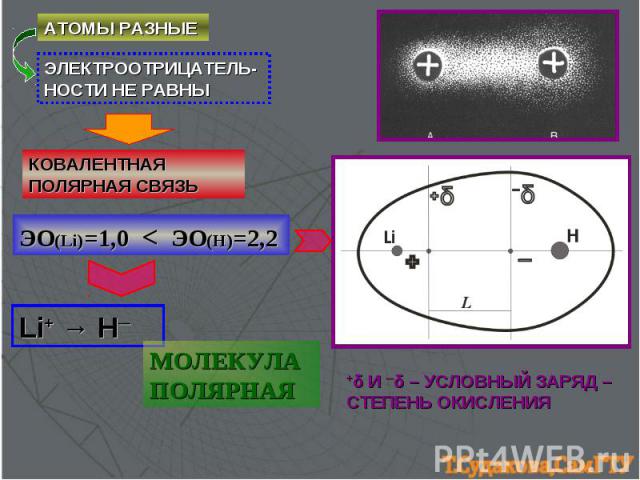
АТОМЫ РАЗНЫЕ ЭЛЕКТРООТРИЦАТЕЛЬ-НОСТИ НЕ РАВНЫ КОВАЛЕНТНАЯ ПОЛЯРНАЯ СВЯЗЬ +δ И ─δ – УСЛОВНЫЙ ЗАРЯД – СТЕПЕНЬ ОКИСЛЕНИЯ ЭО(Li)=1,0 < ЭО(H)=2,2 Li+ → H─ МОЛЕКУЛА ПОЛЯРНАЯ
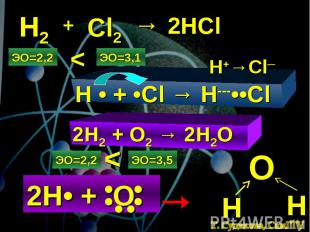
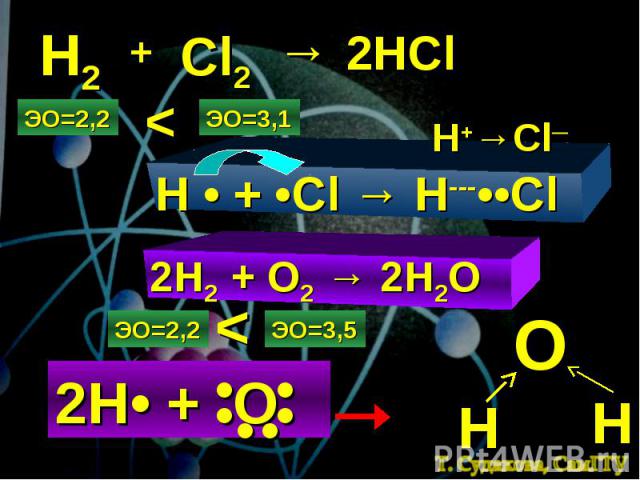
Н2 + Cl2 → 2HCl ЭО=2,2 ЭО=3,1 < H • + •Cl → H---••Cl H+→Cl─ 2H2 + O2 → 2H2O ЭО=2,2 ЭО=3,5 < 2Н• + О • • • • • • О Н Н
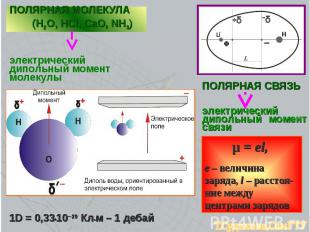
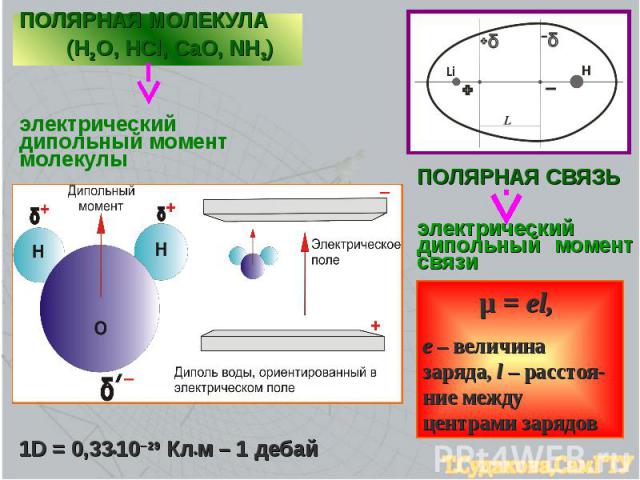
ПОЛЯРНАЯ СВЯЗЬ электрический дипольный момент связи μ = еl, е – величина заряда, l – расстоя-ние между центрами зарядов ПОЛЯРНАЯ МОЛЕКУЛА (H2O, HCl, CaO, NH3) электрический дипольный момент молекулы 1D = 0,33•10–29 Кл•м – 1 дебай
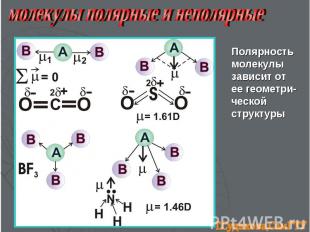
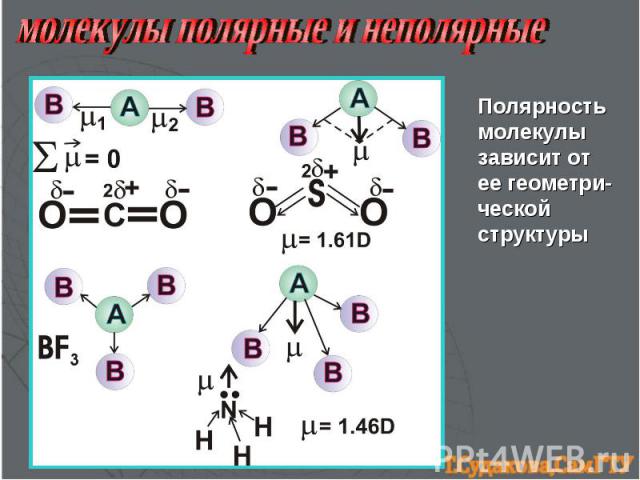
Полярность молекулы зависит от ее геометри-ческой структуры
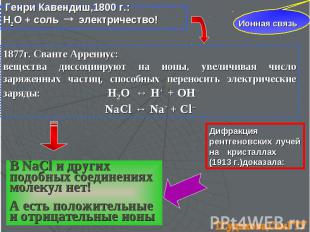
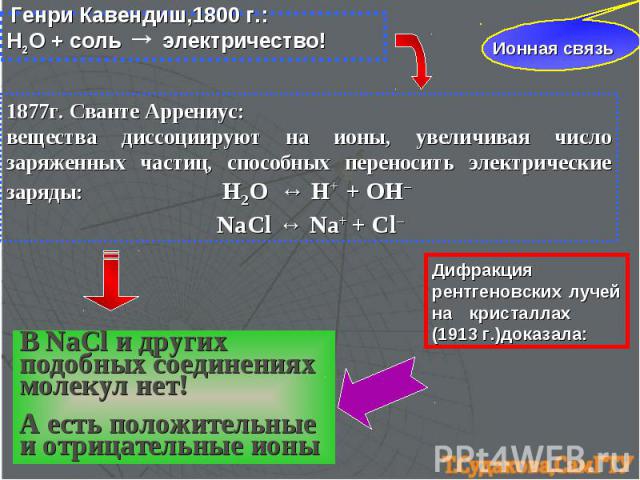
Ионная связь Генри Кавендиш,1800 г.: Н2О + соль → электричество! 1877г. Сванте Аррениус: вещества диссоциируют на ионы, увеличивая число заряженных частиц, способных переносить электрические заряды: H2O ↔ H+ + OH– NaCl ↔ Na+ + Cl– В NaCl и других подобных соединениях молекул нет! А есть положительные и отрицательные ионы Дифракция рентгеновских лучей на кристаллах (1913 г.)доказала:
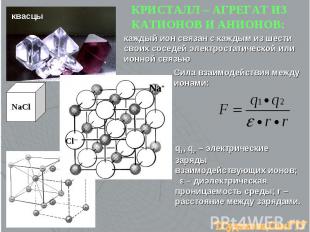
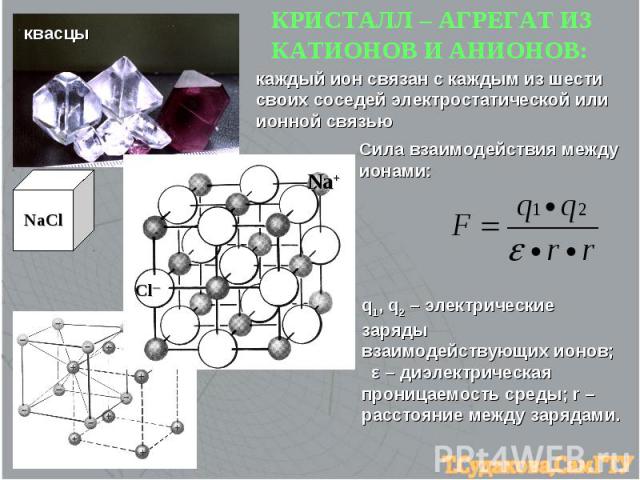
квасцы NaCl Cl─ Na+ КРИСТАЛЛ – АГРЕГАТ ИЗ КАТИОНОВ И АНИОНОВ: каждый ион связан с каждым из шести своих соседей электростатической или ионной связью Сила взаимодействия между ионами: q1, q2 – электрические заряды взаимодействующих ионов; ε – диэлектрическая проницаемость среды; r – расстояние между зарядами.
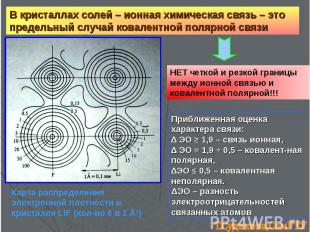
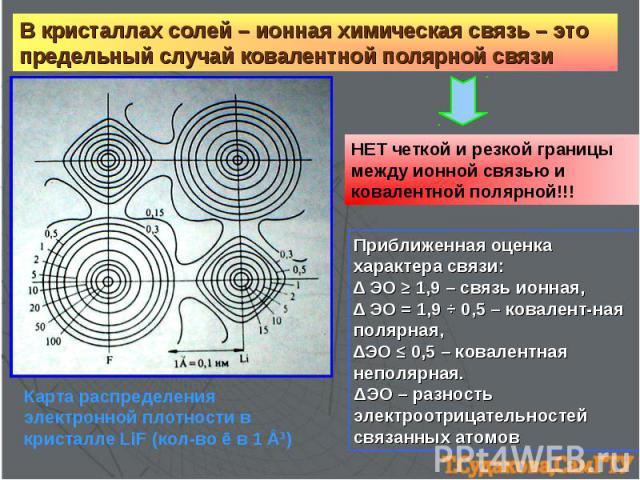
В кристаллах солей – ионная химическая связь – это предельный случай ковалентной полярной связи НЕТ четкой и резкой границы между ионной связью и ковалентной полярной!!! Приближенная оценка характера связи: ∆ ЭО ≥ 1,9 – связь ионная, ∆ ЭО = 1,9 ч 0,5 – ковалент-ная полярная, ∆ЭО ≤ 0,5 – ковалентная неполярная. ΔЭО – разность электроотрицательностей связанных атомов Карта распределения электронной плотности в кристалле LiF (кол-во ē в 1 Е3)
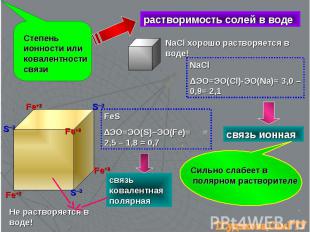
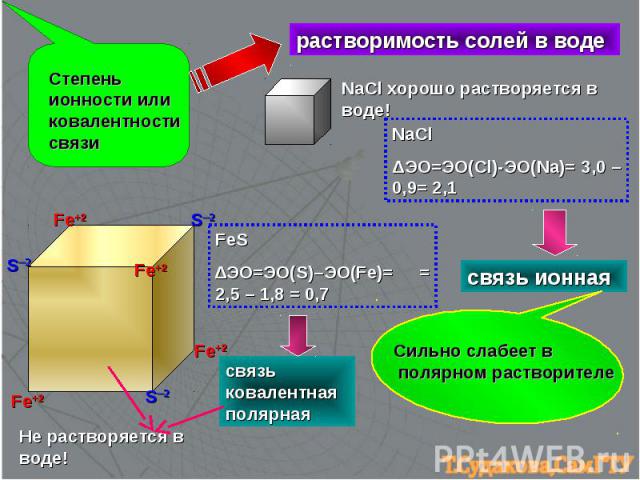
Степень ионности или ковалентности связи растворимость солей в воде Fe+2 Fe+2 Fe+2 Fe+2 S─2 S─2 S─2 Не растворяется в воде! NaCl хорошо растворяется в воде! FeS ∆ЭО=ЭО(S)–ЭО(Fe)= = 2,5 – 1,8 = 0,7 связь ковалентная полярная NaCl ΔЭО=ЭО(Cl)-ЭО(Na)= 3,0 – 0,9= 2,1 связь ионная Сильно слабеет в полярном растворителе
![ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО](https://fs1.ppt4web.ru/images/3018/64877/310/img11.jpg)
ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО неподелен-ная пара ē комплек-сный ион H2O: + H+-Cl− = [H3O]+Cl−
![комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ струк комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ струк](https://fs1.ppt4web.ru/images/3018/64877/310/img12.jpg)
комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ структура комплексного иона [Zn+2(NH3)04]2+ [Cu+2Cl─4]2─ ион-комплексообразователь лиганды координаци-онное число Комплексные соединения: [NH4]OH, [Zn(NH3)4]SO4, Na[Al(OH)4], Na[CuCl4] Сульфат тетраамминцинка, тетрахлорокупрат натрия

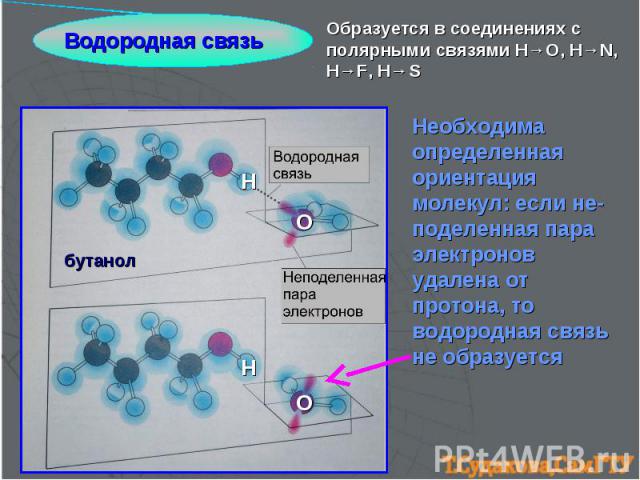
Водородная связь Образуется в соединениях с полярными связями H→O, H→N, H→F, H→S Н О Н О бутанол Необходима определенная ориентация молекул: если не- поделенная пара электронов удалена от протона, то водородная связь не образуется

Водородная связь между молекулами воды Водородная связь между молекулами фтороводорода кластер воды
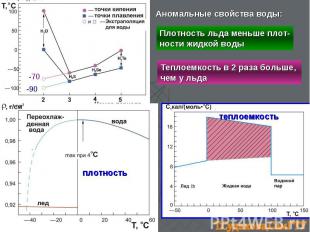
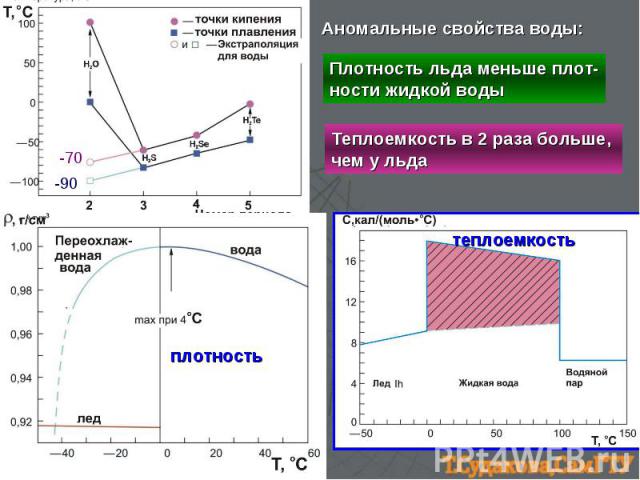
-90 -70 плотность теплоемкость Аномальные свойства воды: Плотность льда меньше плот- ности жидкой воды Теплоемкость в 2 раза больше, чем у льда
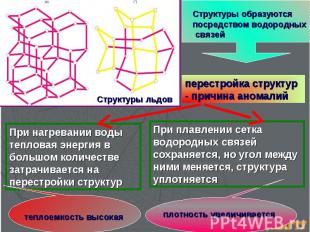
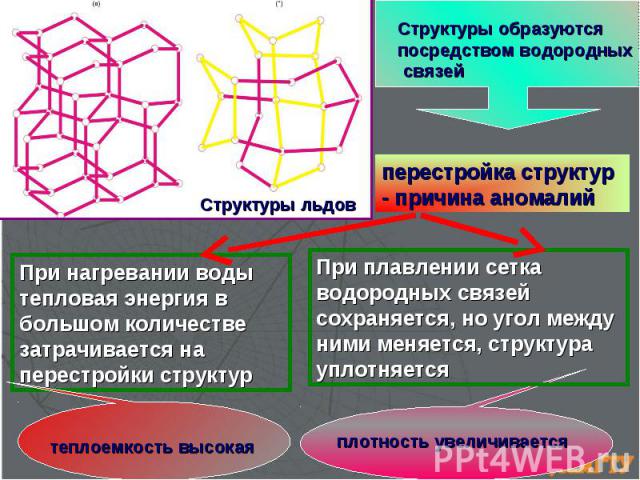
перестройка структур - причина аномалий Структуры образуются посредством водородных связей Структуры льдов При плавлении сетка водородных связей сохраняется, но угол между ними меняется, структура уплотняется При нагревании воды тепловая энергия в большом количестве затрачивается на перестройки структур плотность увеличивается теплоемкость высокая
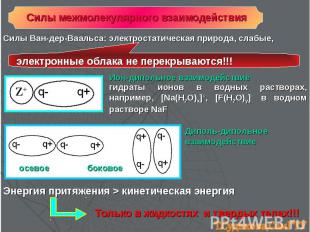
Силы межмолекулярного взаимодействия Силы Ван-дер-Ваальса: электростатическая природа, слабые, Ион-дипольное взаимодействие гидраты ионов в водных растворах, например, [Na(H2O)x]+, [F(H2O)y]− в водном растворе NaF Диполь-дипольное взаимодействие осевое боковое электронные облака не перекрываются!!! Энергия притяжения > кинетическая энергия Только в жидкостях и твердых телах!!!

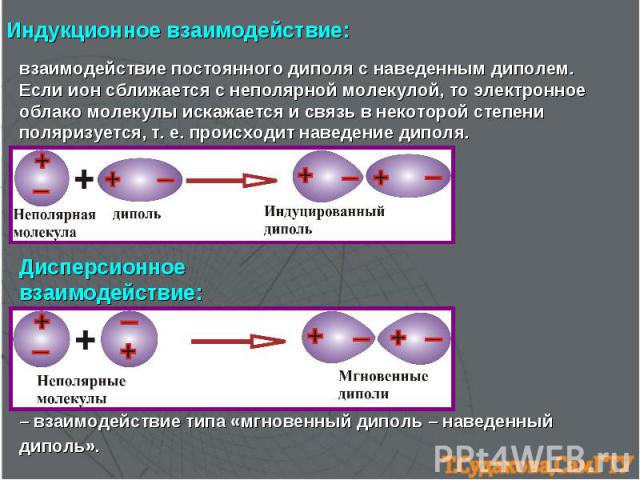
взаимодействие постоянного диполя с наведенным диполем. Если ион сближается с неполярной молекулой, то электронное облако молекулы искажается и связь в некоторой степени поляризуется, т. е. происходит наведение диполя. Индукционное взаимодействие: – взаимодействие типа «мгновенный диполь – наведенный диполь». Дисперсионное взаимодействие:

обусловлено отталкиванием атомных ядер разных молекул (касается только малых по размерам молекул, например, Н2) или, в общем случае, отталкиванием внутренних электронов. Эти силы действуют только на очень малых расстояниях. Межмолекулярное отталкивание: Энергия межмолекулярных взаимодействий очень мала и сильно зависит от расстояния между молекулами: Ориентационное, индукционное, дисперсионное: U ~ 1/(r6) , F ~ 1/(r7) U ~ r12, F ~ r13 Межмолекулярное отталкивание:

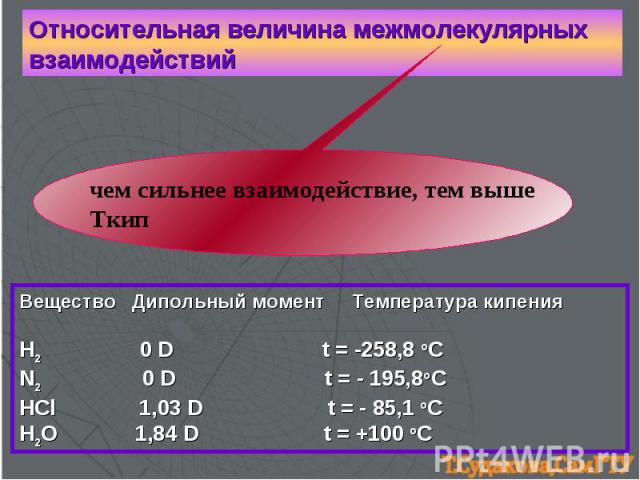
Относительная величина межмолекулярных взаимодействий чем сильнее взаимодействие, тем выше Ткип Вещество Дипольный момент Температура кипения H2 0 D t = -258,8 oC N2 0 D t = - 195,8oC HCl 1,03 D t = - 85,1 oC H2O 1,84 D t = +100 oC
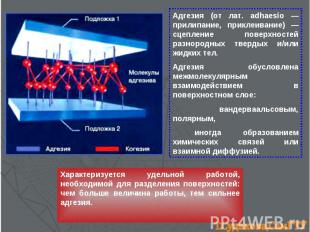
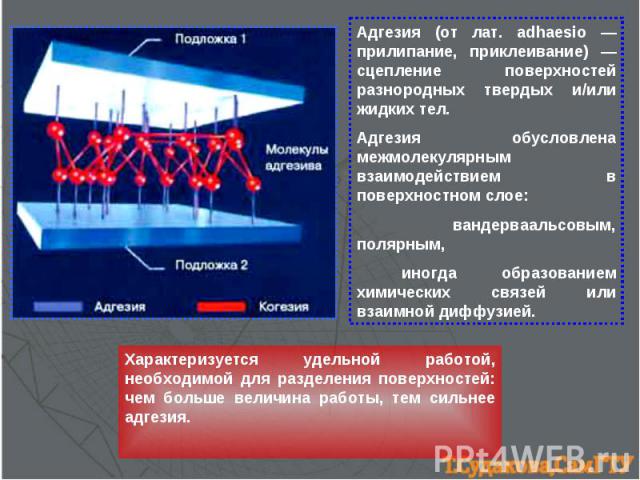
Адгeзия (от лат. adhaesio — прилипание, приклеивание) — сцепление поверхностей разнородных твердых и/или жидких тел. Адгезия обусловлена межмолекулярным взаимодействием в поверхностном слое: вандерваальсовым, полярным, иногда образованием химических связей или взаимной диффузией. Характеризуется удельной работой, необходимой для разделения поверхностей: чем больше величина работы, тем сильнее адгезия.

Кто это?

Геккон – безобидная красивая ящерка, обладающая уникальной способностью лазать где угодно и как угодно. Гекконы не только взбираются по отвесным стенам, они с такой же лёгкостью ходят по потолку или оконному стеклу, не падая! Разгадка была поразительной: при движении геккон использует законы молекулярной физики. Учёные изучили лапку геккона под микроскопом. Выяснилось, что она покрыта мельчайшими волосками диаметр которых в 10 раз меньше диаметра человеческого волоса. На кончике каждого волоска находятся тысячи мельчайших подушечек размером двести миллионных долей см. Снизу подушечки прикрыты листочками ткани, а каждый листочек покрыт сотнями тысяч тонких щетинок. А щетинки, в свою очередь, делятся на сотни плоских кончиков, диаметр каждого из которых всего 200 нм. Сотни миллионов этих волосков позволяют цепляться за малейшие неровности поверхности. Оказалось, здесь работают силы Ван-дер-Ваальса. Силы Ван-дер-Ваальса малы, но расположение волосков на пальчиках гекконов позволяет обеспечить достаточно большую поверхность взаимодействия, чтобы ящерица могла удержаться на потолке при помощи всего одного пальца своей пятипалой лапы или кончика хвоста.
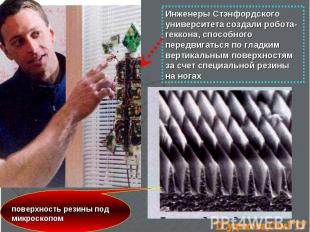
Инженеры Стэнфордского университета создали робота-геккона, способного передвигаться по гладким вертикальным поверхностям за счет специальной резины на ногах поверхность резины под микроскопом

Даже не думай!..... Тебе и в следующий раз придти придется!


![ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО неподелен-ная пара ē комплек-сный ион H2O: + H+-Cl− = [H3O]+Cl− ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО неподелен-ная пара ē комплек-сный ион H2O: + H+-Cl− = [H3O]+Cl−](https://fs1.ppt4web.ru/images/3018/64877/640/img11.jpg)
![комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ структура комплексного иона [Zn+2(NH3)04]2+ [Cu+2Cl─4]2─ ион-комплексообразователь лиганды координаци-онное число Комплексные соединения: [NH4]OH, [Zn(NH3)4]SO4, Na[Al(OH)4],… комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ структура комплексного иона [Zn+2(NH3)04]2+ [Cu+2Cl─4]2─ ион-комплексообразователь лиганды координаци-онное число Комплексные соединения: [NH4]OH, [Zn(NH3)4]SO4, Na[Al(OH)4],…](https://fs1.ppt4web.ru/images/3018/64877/640/img12.jpg)

![Силы межмолекулярного взаимодействия Силы Ван-дер-Ваальса: электростатическая природа, слабые, Ион-дипольное взаимодействие гидраты ионов в водных растворах, например, [Na(H2O)x]+, [F(H2O)y]− в водном растворе NaF Диполь-дипольное взаимодействие осе… Силы межмолекулярного взаимодействия Силы Ван-дер-Ваальса: электростатическая природа, слабые, Ион-дипольное взаимодействие гидраты ионов в водных растворах, например, [Na(H2O)x]+, [F(H2O)y]− в водном растворе NaF Диполь-дипольное взаимодействие осе…](https://fs1.ppt4web.ru/images/3018/64877/640/img17.jpg)