Презентация на тему: Кальций и его соединения


Дать общую характеристику металлов II-А группы по положению в ПСХЭ и строению атомов. Дать общую характеристику металлов II-А группы по положению в ПСХЭ и строению атомов. Рассмотреть свойства и применение кальция и его соединений. Узнать качественную реакцию на ион кальция. Показать значение кальция в организме человека.

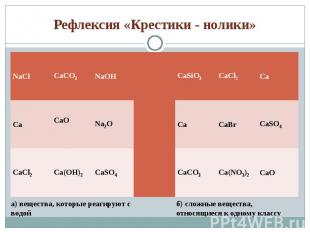
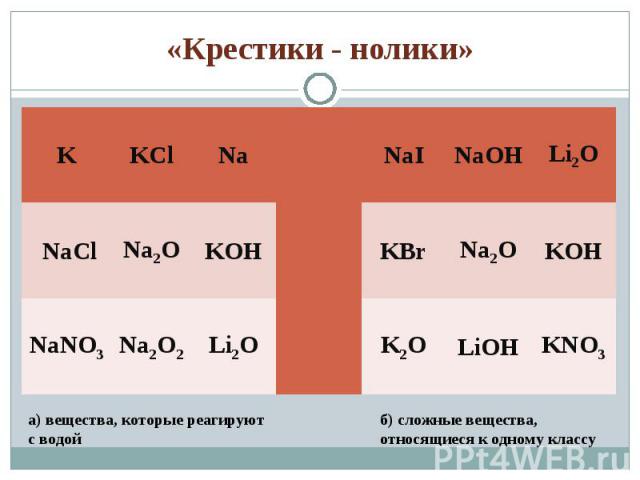
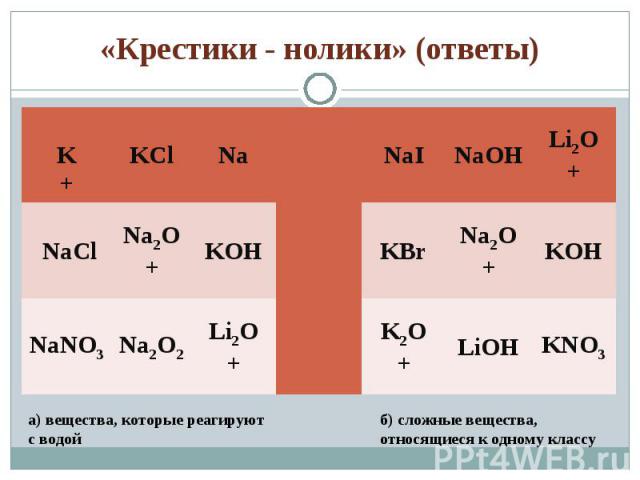
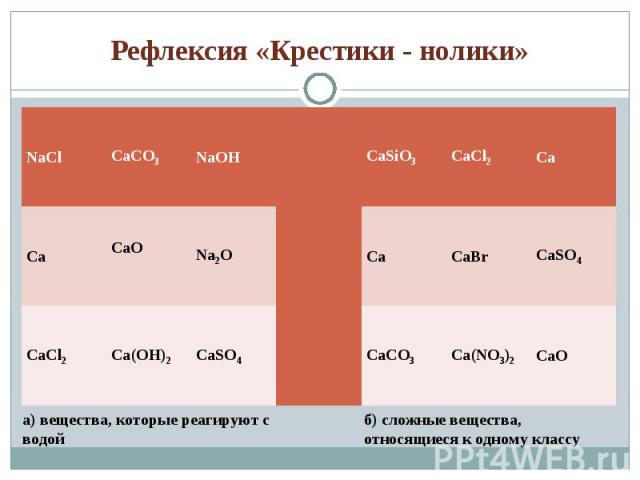
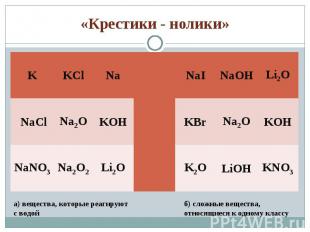
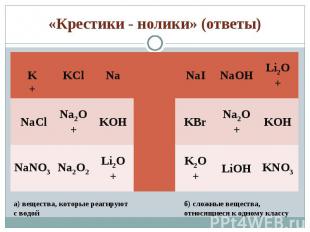
1) Допишите схемы тех реакций, которые протекают практически до конца: 1) Допишите схемы тех реакций, которые протекают практически до конца: а) Li + H2O → … б) NaOH(в избытке) + H3PO4 → … в) Na2O + SO2 → г) NaOH + BaCl2→ д) LiOH + CuSO4 → 2) Решите задачу: Для получения сульфида натрия взяли 4,6г натрия и 4г серы. Какая масса сульфида натрия образовалась при этом?


1. Очень реакционноспособны. 1. Очень реакционноспособны. 2. Обладают положительной валентностью +2. 3. Реагируют с водой при комнатной температуре (кроме Be) с выделением водорода. 4. Обладают большим сродством к кислороду (восстановители). 5. С водородом образуют солеобразные гидриды ЭH2. 6. Оксиды имеют общую формулу ЭО. Тенденция к образованию пероксидов выражена слабее, чем для щелочных металлов.

1 группа – Каково строение атома кальция? 2 группа – Какова его распространённость в природе? 3 группа – Как получают кальций? 4 группа – Каковы физические свойства кальция?



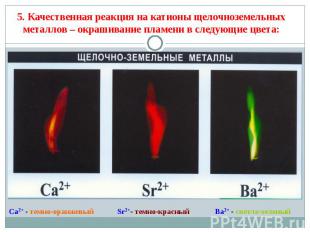
1. Реакция с водой. 1. Реакция с водой. В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями: Mg + 2H2O t° MgО + H2 Ca + 2H2O Ca(OH)2 + H2 2. Все металлы растворяются в кислотах: Ca + 2HCl → CaCl2 + H2

3. Реакция с кислородом. 3. Реакция с кислородом. Все металлы образуют оксиды RO, барий-пероксид – BaO2: 2Mg + O2 → 2MgO Ba + O2 → BaO2 2Ca + O2 → 2CaO 4. С другими неметаллами образуются бинарные соединения: Ca + H2 → CaH2(гидриды) Ca + 2C → CaC2(карбиды) Ca + N2 →Ca3N2(нитриды)

CaO – негашеная известь CaO – негашеная известь CaCO3 t° CaO + CO2 CaO + H2O Ca(OH)2 3CaO + P2O5 Ca3(PO4)2 CaO + 2HNO3 Ca(NO3)2 + H2O

CaO + H2O Ca(OH)2(гашеная известь) CaO + H2O Ca(OH)2(гашеная известь) Ca + 2H2O Ca(OH)2 + H2 Ca(OH)2 + SO2 CaSO3 + H2O Ca(OH)2 + 2HNO3 Ca(NO3)2 + 2H2O Ca(OH)2 + Na2CO3 CaCO3↓+ 2NaOH Ca(OH)2 + CO2 CaCO3+ H2O CaCO3 + CO2 + H2O Сa(HCO3)2 Сa(HCO3)2 t° CaCO3 + CO2 + H2O

А-1. Распределение электронов по электронным слоям в атоме химического элемента, заряд ядра которого +12, А-1. Распределение электронов по электронным слоям в атоме химического элемента, заряд ядра которого +12, 1) 2,8,8,1 2) 2,8,2 3) 2,8,8,2 4) 2,8,8 А-2. В ряду Mg – Ca – Sr – Ba металлические свойства 1) усиливаются 2 ) ослабевают 3) не изменяются 4) изменяются периодически А-3. Схеме превращения Ca0 → Ca+2 соответствует уравнение ХР 1) CaO + 2 HCl = CaCl2 + H2O 2) Ca(OH)2 + 2HCl2 = CaCl2 + 2H2O 3) Ca(OH)2 + CO2 = CaCO3↓ + H2O 4) 2Ca + O2 = 2CaO В-4. Расположите формулы оксидов в порядке усиления основных свойств. 1) MgO 2) SrO 3) BaO 4) CaO В-5. Установите соответствие между сокращённым ионным уравнением ХР обмена и веществами, вступающими в реакцию. 1) Ca2+ + CO32 – = CaCO3↓ А) BaCl2 и Na2SO4 2) BaCO3 + 2H+ = Ba2+ + CO2↑ + H2O Б) CaO и HNO3 3) Ba2+ + SO42 – = BaSO4↓ В) CaCl2 и Na2CO3 4) CaO + 2H+ = Ca2+ + H2O Г) BaCO3 и HCl

1) - 2 1) - 2 2) - 1 3) - 4 4) - 1423 5) - ВГАБ

Даны схемы превращений. Напишите уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого в 1 уравнении и для третьего во втором превращении составьте сокращённое ионное уравнение реакции. Даны схемы превращений. Напишите уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого в 1 уравнении и для третьего во втором превращении составьте сокращённое ионное уравнение реакции. 1) Ca(OH)2 → CaCO3→ X → K2CO3 2) CaO → Ca(OH)2 → X → AgCl Решите задачу: При обжиге 260 г известняка получили 112 г оксида кальция. Вычислите массу и массовую долю карбоната кальция, содержащегося в известняке.

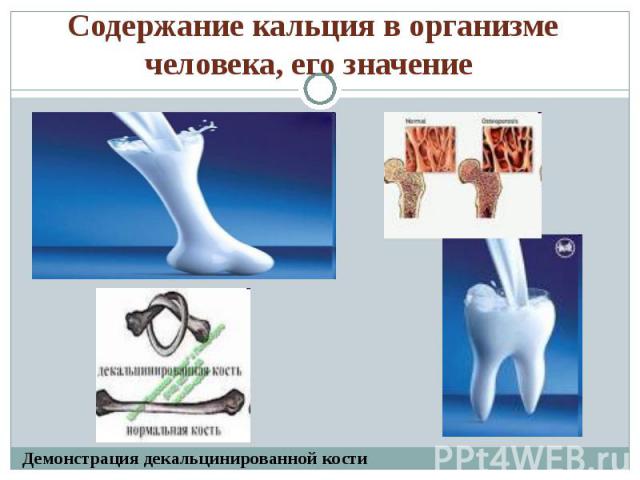
Кальций является основой костной ткани, зубов и придатков кожи – волос и ногтей. Кальций является основой костной ткани, зубов и придатков кожи – волос и ногтей. Он принимает участие в процессе сокращения миокарда – сердечной мышцы – и таким образом влияет на сердечные показатели – пульс, давление и другие. Кроме того, кальций участвует в работе центральной нервной системы и усвоении продуктов питания.

Дети до 3 лет — 600 мг. Дети до 3 лет — 600 мг. Дети от 4 до 10 лет — 800 мг. Дети от 10 до 13 лет — 1000 мг. Подростки от 13 до 16 лет — 1200 мг. Молодежь от 16 и старше — 1000 мг. Взрослые от 25 до 50 лет — от 800 до 1200 мг. Беременные и кормящие грудью женщины — от 1500 до 2000 мг.