Презентация на тему: Физические и химические свойства алюминия

Тема урока: «Алюминий, его физические и химические свойства». Из глины я обыкновенной, Но я на редкость современный. Я не боюсь электротока, Бесстрашно в воздухе лечу; Служу на кухне я без срока - Мне все задачи по плечу. Горжусь своим я именем: Зовусь я ........... 5klass.net

Цели урока: Дать характеристику алюминия по его положению в периодической системе химических элементов. На основе строения атома рассмотреть его физические и химические свойства. Познакомиться с промышленным способом получения алюминия и указать области его применения.

Из истории открытия алюминия… «Серебро из глины» В период открытия алюминия этот металл был дороже золота. Англичане хотели почтить богатым подарком великого русского химика Д.И Менделеева, подарили ему химические весы, в которых одна чашка была изготовлена из золота, другая - из алюминия. Чашка из алюминия стала дороже золотой. Полученное «серебро из глины» заинтересовало не только учёных, но и промышленников и даже императора Франции. Д.И.Менделеев

Интересные факты Немецкий учёный Ф.Велер (1827 г.) Памятник Дж. Вашингтону В лунном грунте обнаружен алюминий Самый большой телескоп в России

Применение алюминия

Авиастроение Применение алюминия и его сплавов во всех видах транспорта, а в особенности воздушного привело к уменьшению собственной массы транспортных средств и к резкому увеличению эффективности их использования.

Кораблестроение Алюминий и его сплавы применяют при отделке и изготовлении корпусов и дымовых труб судов, спасательных лодок, радарных мачт, трапов.

Машиностроение Моторы, блоки, головки цилиндров, картеры, коробки передач, насосы и многие другие детали также изготавливают из алюминия и его сплавов.

Пищевая промышленность Алюминиевая фольга дешевле оловянной и полностью заменила ее как упаковочный материал для пищевых продуктов. Все больше и больше используется алюминий при изготовлении тары для консервирования и храпения продуктов сельского хозяйства.

Электротехника Алюминий и его сплавы используют в электротехнической промышленности для изготовления кабелей, шинопроводов, конденсаторов, выпрямителей переменного тока.

Военная промышленность Алюминий, а также его сплавы является стратегическим металлом и широко используется в военной промышленности при строительстве военной техники и оружия: самолетов, танков, артиллерийских установок, ракет, зажигательных веществ, а также для других целей в военной технике.

Строительство Алюминий и его сплавы применяются в промышленном и гражданском строительстве при изготовления каркасов зданий, ферм, оконных рам, лестниц и др. конструкций.
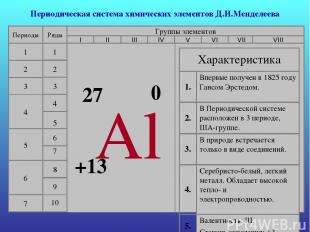
Периодическая система химических элементов Д.И.Менделеева Периоды 1 2 3 4 5 6 7 Ряды 1 2 3 4 10 9 8 7 5 6 Группы элементов I II VI V VII III IV VIII Al Характеристика 1. Впервые получен в 1825 году Гансом Эрстедом. 2. В Периодической системе расположен в 3 периоде, IIIА-группе. 3. В природе встречается только в виде соединений. 4. Серебристо-белый, легкий металл. Обладает высокой тепло- и электропроводностью. 5. Валентность: III. Степень окисления: +3.

27 +13 0 2 8 3 P = 13 e = 13 N = 14 − Краткая электронная запись:
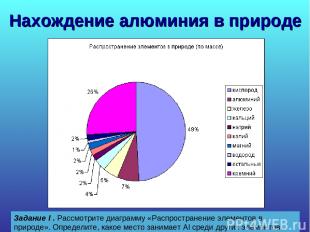
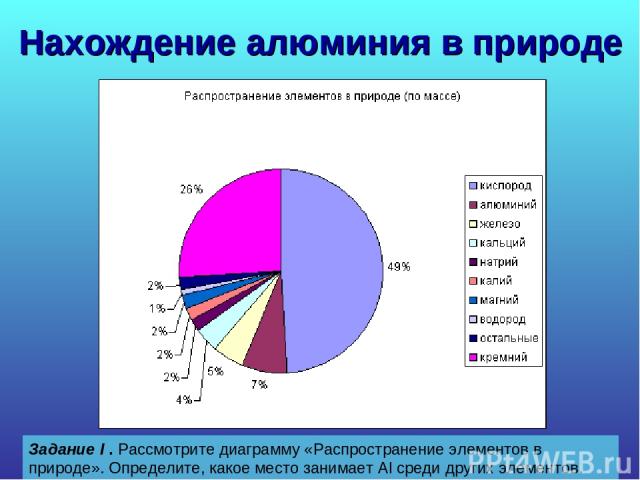
Нахождение алюминия в природе Задание I . Рассмотрите диаграмму «Распространение элементов в природе». Определите, какое место занимает Al среди других элементов.

Природные соединения алюминия Задание II. Рассмотрите образцы природных соединений, сравните их по твердости, прочности, цвету, рассчитайте содержание Al в некоторых из них. Нефелины — KNa3[AlSiO4]4 Глинозёмы (смеси каолинов с песком SiO2, известняком CaCO3, магнезитом MgCO3) Корунд (сапфир, рубин, наждак) — Al2O3 Полевые шпаты — (K,Na)2O·Al2O3·6SiO2, Ca[Al2Si2O8] Каолинит — Al2O3·2SiO2 · 2H2O Берилл (изумруд, аквамарин) — 3ВеО · Al2О3 · 6SiO2

Физические свойства алюминия. Лабораторная работа. Инструктивная карта. 1. Рассмотрите алюминиевую пластинку. 2. Определите агрегатное состояние вещества алюминия. 3. Какого цвета пластинка? 4. Определите, имеет ли блеск данная пластина? 5. Опустите пластинку на ¼ её длины в стакан с горячей водой на 10-15 секунд. Вытащите пластинку из воды, протрите салфеткой и определите, обладает ли алюминий теплопроводностью? 6. Возьмите в руки алюминиевую фольгу. Определите, обладает ли алюминий пластичностью? Лёгкий ли это металл? 7. Поместите в стакан с холодной водой алюминиевую пластинку, проверните несколько раз. Наблюдается растворение алюминия? 8. Кратко запишите свои наблюдения согласно плану: - агрегатное состояние, - цвет, - блеск, - теплопроводность, - пластичность, - растворимость в воде.

2Al +3O2 Al2O3 +3Cl2 2AlCl3 +3S Al2S3 +6HCl 2AlCl3 + 3H2 +3CuSO4 Al2(SO4)3 + 3Cu

Лабораторная работа: «Химические свойства алюминия». Инструктивная карта. 1. Возьмите две пробирки. В каждую положите по кусочку алюминия. Прилейте в одну из них 1-2 мл раствора соляной кислоты, а в другую столько же раствора серной кислоты. Что наблюдаете? Пробирки слегка нагрейте. Запишите уравнения соответствующих реакций. 2. Кусочек алюминия положите в пробирку. Прилейте 1,5 мл концентрированной серной кислоты. Что наблюдаете? Запишите уравнение реакции. 3. В пробирку поместите кусочек алюминия и прилейте раствор щёлочи. Содержимое пробирки нагрейте. Что происходит? Запишите уравнение реакции. 4. Результаты проделанной работы оформите в таблицу: № опыта Исходные вещества Наблюдения Уравнения реакций и выводы

Алюминий является амфотерным элементом: взаимодействует с кислотами и со щелочами. 2Al + 6HCl = 2AlCl3 + 3H2 2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2

Получение алюминия в промышленности Алюминий получают электрохимическим методом из бокситов. 2Al2O3 ток> 4Al + 3O2

Тест 1.Какова электронная конфигурация атома алюминия? А) 1s22s22p1 Б)1s22s22p3 B) 1s22s22p63s23p1 Г) 1s22s22p63s23p63d14s2 2. С какими из указанных веществ реагирует алюминий? А) СаО Б) HCl B) Cl2 Г) NaOH 3. Какие из указанных металлов являются более активными, чем алюминий? А) Na Б) Cu B) Ca Г) Fe 4. Наиболее характерная степень окисления алюминия: А) +1 Б) +2 В) +3 Г) +4 5. Алюминий в химических реакциях проявляет свойства: А) окислителя Б) инертного соединения В) восстановителя Г) окислителя и восстановителя 6. В промышленности алюминий получают: А) используя в качестве восстановителя металлический натрий Б) электролизом расплава оксида алюминия В) используя в качестве восстановителя оксид углерода (П) Г) электролизом раствора солей алюминия

Правильные ответы: 1 2 3 4 5 6 В Б, Г А, В В В Б

Домашнее задание: Учебник Г.Е.Рудзитиса, Ф.Г.Фельдмана «Химия 9 класс» 1) § 42 2) № 6, 7, стр. 130
















![Природные соединения алюминия Задание II. Рассмотрите образцы природных соединений, сравните их по твердости, прочности, цвету, рассчитайте содержание Al в некоторых из них. Нефелины — KNa3[AlSiO4]4 Глинозёмы (смеси каолинов с песком SiO2, известняк… Природные соединения алюминия Задание II. Рассмотрите образцы природных соединений, сравните их по твердости, прочности, цвету, рассчитайте содержание Al в некоторых из них. Нефелины — KNa3[AlSiO4]4 Глинозёмы (смеси каолинов с песком SiO2, известняк…](https://fs3.ppt4web.ru/images/132073/184056/640/img15.jpg)




















