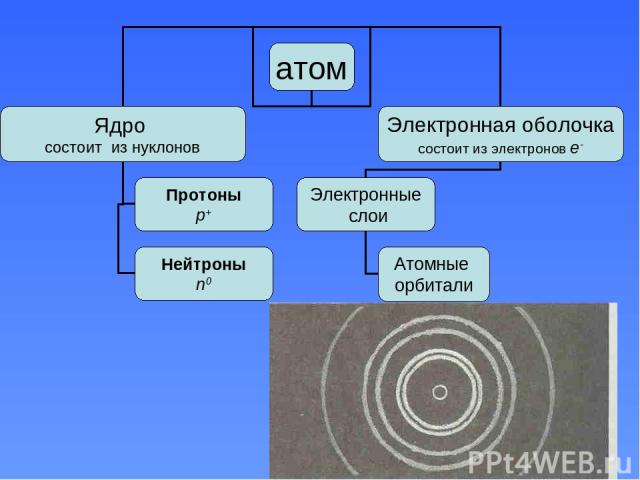
Презентация на тему: Атомы химических элементов

Атомы химических элементов (для учащихся 8 класса) 5klass.net

Содержание: Фундаментальные открытия конца IX начала X веков, доказывающие сложность строения атома Модели атома Состав атома Изотопы Строение электронных оболочек атомов Электронные конфигурации атомов

Атом – в переводе с греческого «неделимый» 1897 г. английский физик Джозев Томсон и французский – Жан Перрен открыли катодные лучи; установили «-» заряд электрона; 1891 г. ирландский физик Стони ввел понятие «электрон»; 1896 г. – физик Анри Беккерель открыл явления радиоактивности; a- лучи (частицы с зарядом +2 и массой 4) b- лучи (поток электронов) g- лучи (электромагнитные волны)

Модели строения атомов «Пудинг с изюмом» (1902 – 1904 гг., В. Кельвин и Дж. Томсон) Планетарная (1907г., Э. Резерфорд) Модель Бора (1913г.) Э. Резерфорд
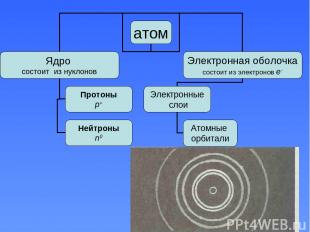

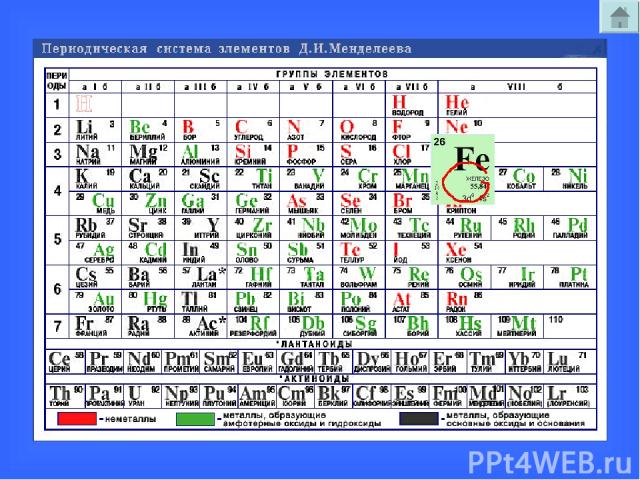
Связь строения атома с положением химического элемента в ПСХЭ Заряд ядра: np+ = Z Z – порядковый номер элемента в ПСХЭ Массовое число атома: A= nn0 + Z Общее число электронов: ne- = np+ = Z Число слоев в электронной оболочке равно № периода в ПСХЭ Число валентных электронов равно № группы в ПСХЭ
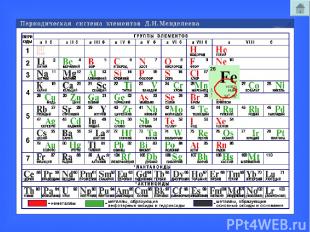
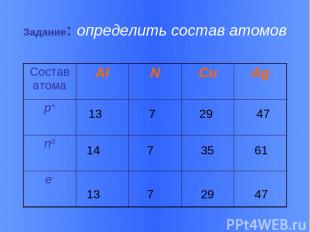
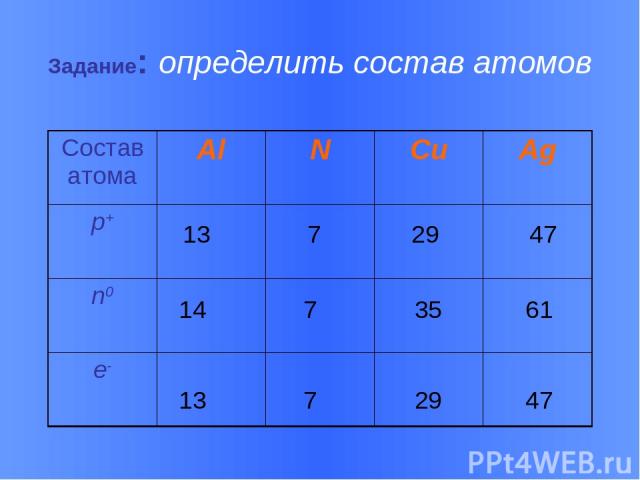
Задание: определить состав атомов 13 7 29 47 14 7 35 61 13 7 29 47 Состав атома Al N Cu Ag p+ n0 e-

Блиц-опрос: Какую информацию о составе атома дает порядковый номер химического элемента? Как связанны между собой положение хим. элемента в ПСХЭ и строение атомов? Из масс каких составляющих атом элементарных частиц складывается атомная масса?

Вставьте пропущенные слова: Атом серы содержит в ядре…..протонов и …..нейтронов. Число электронов, находящихся вокруг ядра, как и число протонов, равно ….. элемента. Число энергетических уровней определяется номером….. и равно….. Число валентных электронов определяется номером ….. и равно…..

Выводы: 1. Химический элемент – вид атомов с одинаковым зарядом ядра 2. Изотопы – разновидности одного элемента с разными массовыми числами 5. Что получится, если в ядре атома азота изменить число протонов? (добавить два р+; отнять один р+) число нейтронов? число электронов?
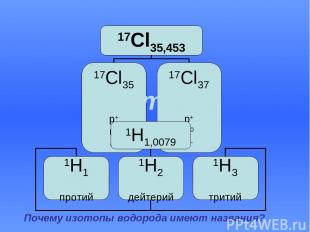
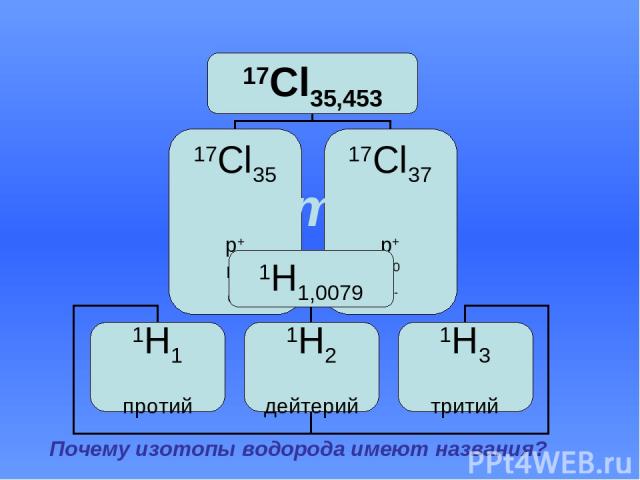
Изотопы Почему изотопы водорода имеют названия?

Сколько различных видов молекул воды можно получить из изотопов водорода 1Н, 2Н, 3Н и изотопа кислорода 16О? Каковы относительные молекулярные массы?

Электронная конфигурация атомов Электрон (е-) – элементарная частица, заряд которой принят равным -1. Спин электрона – характеристика электрона, связанная с направлением его движения вокруг своей оси. Атомная орбиталь – область вокруг ядра, где вероятность пребывания электрона составляет 90%. АО различаются энергией, формой, размерами. Энергетический уровень – совокупность атомных орбиталей, близких по форме и энергии
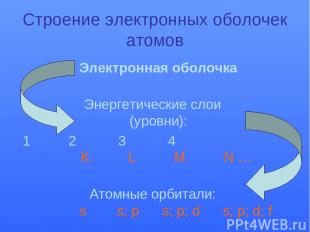
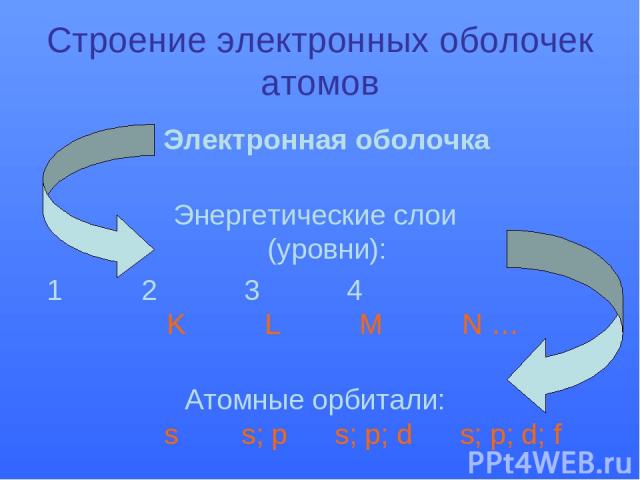
Строение электронных оболочек атомов Электронная оболочка Энергетические слои (уровни): 1 2 3 4 K L M N … Атомные орбитали: s s; p s; p; d s; p; d; f
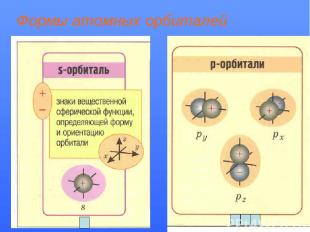
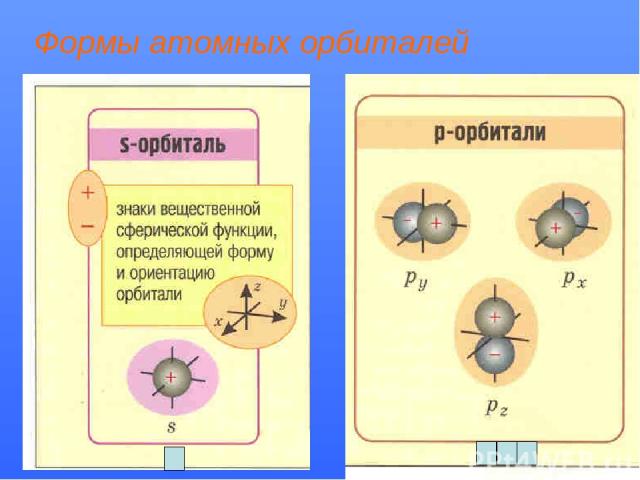
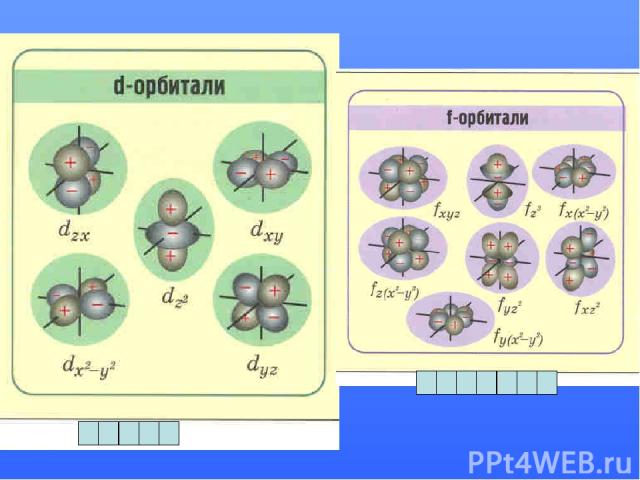
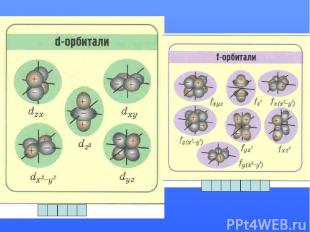
Формы атомных орбиталей
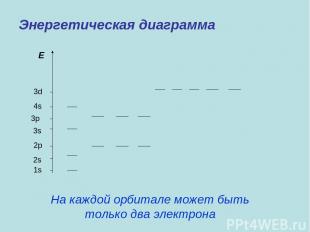
Энергетическая диаграмма E 3d 4s 3p 3s 2p 2s 1s На каждой орбитале может быть только два электрона

Строение атома железа 26Fe56 2е 8е 14е 2е +26 Е Электронная формула: 1s2 2s22p6 3s23p63d6 4s2 валентные электроны IV период; VIII Б группа р+ = 26 н0 = 56-26 = 30 е- = 26

Задание: Составить схемы распределения электронов по слоям; по орбиталям; электронные формулы для атомов № 3 -- № 18. Вывод: одинаковое строение внешних энергетических уровней периодически повторяется, поэтому повторяются и свойства химических элементов

Д.И. Менделеев Третья (современная) формулировка Периодического закона: свойства химических элементов и образованных ими веществ находятся в периодической зависимости от изменения внешних электронных структур их атомов