Презентация на тему: Методическая разработка урока по химии по теме «Железо и его соединения»






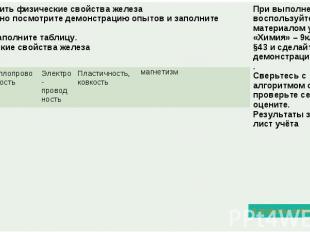
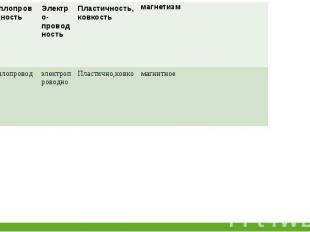

1. Взаимодействие с неметаллами. 1. Взаимодействие с неметаллами. Железо реагирует с неметаллами (слайд №6): Fe + S = FeS При нагревании до 200-250 0С реагирует с хлором 2Fe+3Cl2=2FeCl3 2. Взаимодействие с кислотами. Железо реагирует с кислотами (слайд №) Fe+H2SO4=FeSO4+H2 В концентрированных азотной и серной кислотах железо не растворяется, так как на поверхности металла возникает пленка, препятствующая реакции металла с кислотой, поэтому концентрированные серную и азотную кислоты можно перевозить в железной таре (происходит пассивация металла).

Fe + 2HCl = FeCl2 + H2 Fe + 2HCl = FeCl2 + H2 3. Взаимодействие с водой 4Fe + 3О2 + 6Н2О = 4Fe(ОН)3 4. Взаимодействие с солями Fe+CuSO4 = FeSO4 + Cu 5. Взаимодействие с кислородом 3Fe+2O2 = Fe2O3 • FeO (Феррит железа)


Fe + S = FeS Fe + S = FeS 2Fe+3Cl2=2FeCl3 Fe+H2SO4=FeSO4+H2 Fe + 2HCl = FeCl2 + H2 4Fe + 3О2 + 6Н2О = 4Fe(ОН)3 Fe+CuSO4 = FeSO4 + Cu 3Fe+2O2 = Fe2O3 • FeO


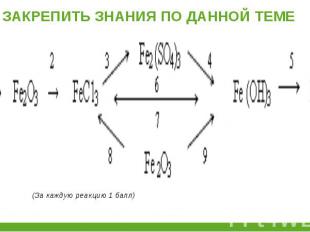


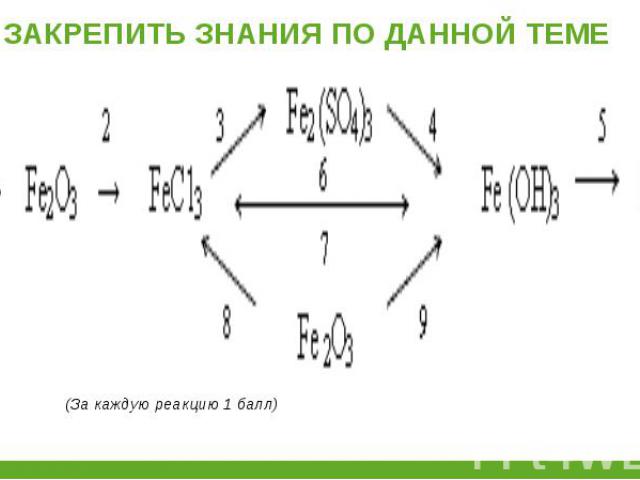
4Fе + 3О2 = 2Fе2О3 4Fе + 3О2 = 2Fе2О3 Fе2О3 + 6НС1 =2FеС13 + 3Н2О 2FеС13 + 3Аg2SО4 = Fе2(SО4)3+ 6 AgCl Fе2(SО4)3 + 6NаОН = 2Fе(ОН)3 Fе(ОН)3 + КОН = К [Fе(ОН)4] Fе(ОН)3 + 3НС1 = FеС13 + 3Н2О Fе2О3 + 6НС1 = 2FеС13 + 3Н2О 2Fе(ОН)3 = Fе2О3 + 3Н2О




www.catalogmineralov.ru – сайт содержит каталог минералов, большую коллекцию фотографий и описание минералов. www.catalogmineralov.ru – сайт содержит каталог минералов, большую коллекцию фотографий и описание минералов. http://.elementy.ru – сайт «Элементы большой науки», содержит каталоги и статьи научно-популярных журналов «Химия и жизнь», « Наука и жизнь», «Природа» и др. http://www.ovitanah.com - сайт посвящен витаминам и микроэлементам, содержит интересную информацию. http://alhimik.ru – сайт «Алхимик» содержит самую разнообразную информацию по химии.









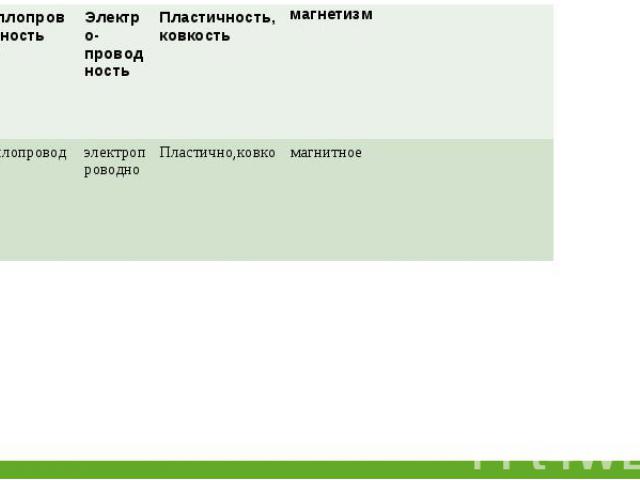







![4Fе + 3О2 = 2Fе2О3 4Fе + 3О2 = 2Fе2О3 Fе2О3 + 6НС1 =2FеС13 + 3Н2О 2FеС13 + 3Аg2SО4 = Fе2(SО4)3+ 6 AgCl Fе2(SО4)3 + 6NаОН = 2Fе(ОН)3 Fе(ОН)3 + КОН = К [Fе(ОН)4] Fе(ОН)3 + 3НС1 = FеС13 + 3Н2О Fе2О3 + 6НС1 = 2FеС13 + 3Н2О 2Fе(ОН)3 = Fе2О3 + 3Н2О 4Fе + 3О2 = 2Fе2О3 4Fе + 3О2 = 2Fе2О3 Fе2О3 + 6НС1 =2FеС13 + 3Н2О 2FеС13 + 3Аg2SО4 = Fе2(SО4)3+ 6 AgCl Fе2(SО4)3 + 6NаОН = 2Fе(ОН)3 Fе(ОН)3 + КОН = К [Fе(ОН)4] Fе(ОН)3 + 3НС1 = FеС13 + 3Н2О Fе2О3 + 6НС1 = 2FеС13 + 3Н2О 2Fе(ОН)3 = Fе2О3 + 3Н2О](https://fs1.ppt4web.ru/images/55329/108424/640/img16.jpg)
















