Презентация на тему: ОСТРЫЙ ИНФАРКТ МИОКАРДА

ОСТРЫЙ ИНФАРКТ МИОКАРДА: СОВРЕМЕННЫЕ ПОДХОДЫ К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ Профессор И.С. Курапеев Кафедра анестезиологии и реаниматологии СПб МАПО
ОСТРЫЙ ИНФАРКТ МИОКАРДА: СОВРЕМЕННЫЕ ПОДХОДЫ К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ
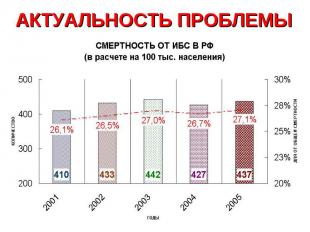

В развитых странах 20% больных острым инфарктом миокарда погибают до оказания медицинской помощи (большинство - от аритмии), а общая 30-дневная летальность достигает 30%.

ЧТО ЖЕ ДЕЛАТЬ?

НЕОБХОДИМО: быстро диагностировать инфаркт миокарда немедленно начать лечебные мероприятия

СОВРЕМЕННЫЕ ПОДХОДЫ К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ОСТРОГО КОРОНАРНОГО СИНДРОМА ОСНОВЫВАЮТСЯ НА ПРИНЦИПАХ ДОКАЗАТЕЛЬНОЙ МЕДИЦИНЫ

Главный постулат доказательной медицины состоит в том, что каждое клиническое решение или выполнение определенной технологической операции должно базироваться на строго доказанных научных фактах.

В 1980 году Американский Колледж Кардиологов и Американская Сердечная Ассоциация (ACC/AHA) впервые создали практические рекомендации (Guidelines) в области сердечно-сосудистых заболеваний. Каждые 2 года они пересматриваются.

ACC/AHA Guidelines for the Management of Patients with ST-Elevation Myocardial Infarction (Circulation, Aug., 2004;110:e82-e292)




КЛАССИФИКАЦИЯ РЕКОМЕНДАЦИЙ И ЭФФЕКТИВНОСТИ ДИАГНОСТИЧЕСКИХ И ЛЕЧЕБНЫХ ПРОЦЕДУР

Возможны следующие варианты манифестации острого коронарного синдрома: нестабильная стенокардия инфаркт миокарда без зубца Q инфаркт миокарда с зубцом Q

Диагностическая классификация острых коронарных синдромов
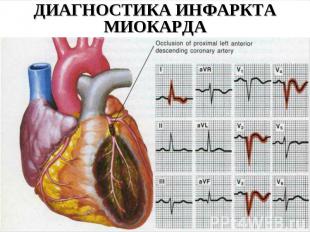
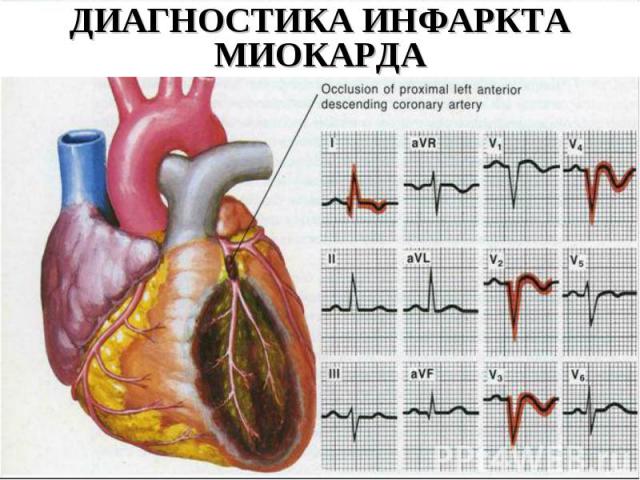
ДИАГНОСТИКА ИНФАРКТА МИОКАРДА

Острый инфаркт миокарда может быть определен совокупностью клинических, электрокардиографических, эхокардиографических биохимических и патологических характеристик.

НЕМНОГО ИСТОРИИ Честь первого описания клиники инфаркта миокарда принадлежит русским ученым Василию Пармёновичу Образцову и Николаю Дмитриевичу Стражеско. Obrastzov W.P., Strazhesko N.D. Zur Kenntnis der Thrombose der Koronararterien des Herzens. Z Klin Med 1910;71:116-132. Электрокардиографические критерии инфаркта миокарда впервые разработаны в 1912 году американским кардиологом John Herrick. Herrick J.B. Certain clinical features of sudden obstruction of the coronary arteries. JAMA 1912;59:2015-2020. В 1887 году голландский физиолог Willem Einthoven демонстрирует на конгрессе физиологов в Лондоне кривую потенциалов действия сердца, которой он присваивает ей название "ЭЛЕКТРОКАРДИОГРАММА". Лауреат Нобелевской премии (1924 г.) в области медицины.

Значение ЭКГ в диагностике инфаркта миокарда трудно переоценить. Это не только важнейший инструмент диагностики, но и первостепенный фактор в выборе стратегии реперфузионной терапии

СОВРЕМЕННЫЕ БИОХИМИЧЕСКИЕ МАРКЕРЫ ИНФАРКТА МИОКАРДА До недавнего времени «золотым стандартом» биохимической диагностики инфаркта миокарда было исследование изофермента МВ креатинкиназы (КК-МВ). На сегодняшний день наибольшую диагностическую ценность имеют: тесты на Тропонин Т и I. использование количественного определения изофермента МВ креатинкиназы КК-МВmass

Тропонин (белок тропонинового комплекса миокарда) появляется в крови раньше (через 2,5 часа), чем КК-МВ (4-5 часов), достигает максимума через 8-10 часов (первый пик) и на 3-4 сутки (второй пик). Уровень нормализуется через 10-14 дней.

Уровень Tропонина T больше, чем 0,1 ng/mL, является важным индикатором последующих событий при остром коронарном синдроме. В этой случае полагают, что больные нестабильной стенокардией или не Q инфарктом миокарда, имеют высокий риск возникновения инфаркта с подъемом сегмента ST и/или внезапной смерти в течение ближайших 6 недель.

Внедрение методов определения тропонинов не только существенно повысило значение биохимического компонента в диагностике острого инфаркта миокарда, но и послужило основой для текущего пересмотра критериев диагностики заболевания.


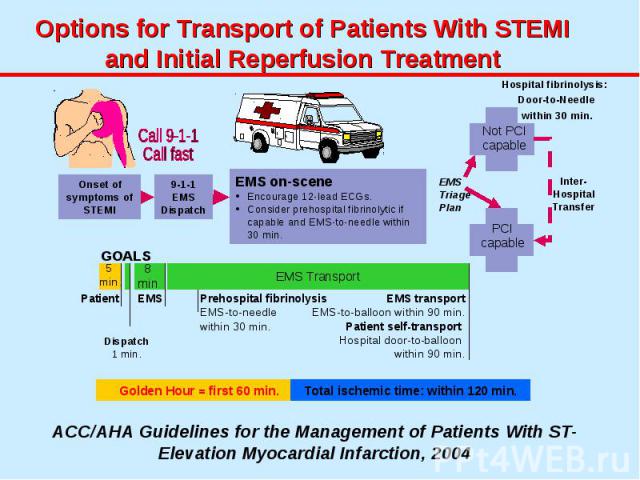
Лечение и диагностику ОИМ в ранние сроки заболевания можно условно разделить на 4 этапа распознавание симптоматики пациентом транспортировка поступление в стационар реперфузия
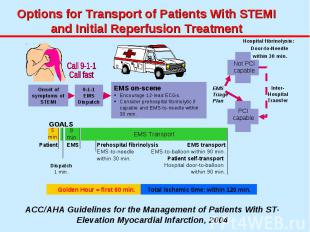
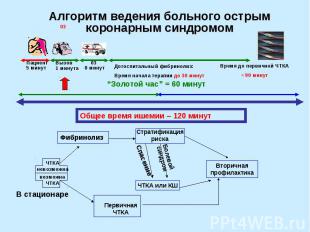
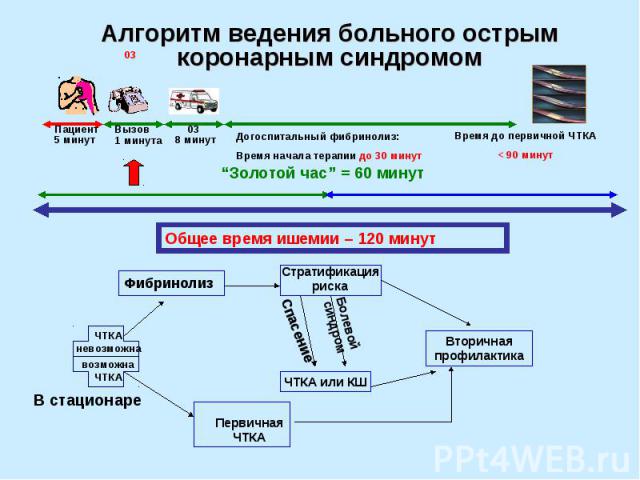
Алгоритм ведения больного острым коронарным синдромом

В отношении пациентов с болью в груди, система скорой медицинской помощи должна действовать безотлагательно!

Когда скорая помощь прибывает к пациенту с подозреваемым острым инфарктом миокарда, он должен получить помощь как можно быстрее, потому что польза от восстановления кровотока (реперфузии) самая большая, если терапия начата рано.

ПЕРВИЧНАЯ ОЦЕНКА СОСТОЯНИЯ ПАЦИЕНТА ДОЛЖНА БЫТЬ ВЫПОЛНЕНА В ПРЕДЕЛАХ 10-20 МИНУТ С МОМЕНТА ПРИБЫТИЯ СКОРОЙ ПОМОЩИ!

Целью любой современной программы организации помощи больным острым инфарктом миокарда является сокращение времени от начала ангинозного приступа до начала любой процедуры реперфузии миокарда: тромболитическая терапия чрескожная транслюминальная ангиопластика коронарное шунтирование

Первичная оценка пациента с болью в груди при сборе анамнеза и параллельной регистрации ЭКГ в 12-ти отведениях должна быть выполнена по следующим 4-м критериям: определенный инфаркт миокарда вероятный инфаркт миокарда вероятно «не инфаркт миокарда» определенно «не инфаркт миокарда»

Программа в первые часы инфаркта миокарда включает следующие основные компоненты: Этапность лечения. Совмещение диагностических и лечебных мероприятий. Учет тяжести больных (степени риска, осложнений и смерти). Учет срока от начала инфаркта до поступления больного в cтационар. Дифференцированный мониторинг.

Рекомендации по первичному лечению при подозрении на инфаркт миокарда Первичная оценка ЭКГ < 10 мин после поступления Оксигенация через носовой катетер Обеспечение венозного доступа Мониторинг ЭКГ Нитроглицерин под язык (сист. АД > 90 мм рт.ст., ЧСС > 50 но < 100 уд/мин)

Рекомендации по первичному лечению при подозрении на инфаркт миокарда Обезболивание (морфин!) Аспирин (160-325 мг per os) Определение электролитов, ферментов Тромболизис или коронаропластика при элевации сегмента ST > l mV Коронарное шунтирование.

ТРОМБОЛИТИЧЕСКАЯ ТЕРАПИЯ ОСТРОГО ИНФАРКТА МИОКАРДА

Сравнительные многоцентровые исследования тромболитической терапии В настоящее время проведено более 10 больших проспективных двойных слепых плацебо-контролируемых рандомизированных исследований по оценке влияния раннего тромболизиса на смертность. Они четко показали уменьшение смертности на 25-30% независимо от применяемого тромболитического препарата.

При применении тромболитической терапии доказан выраженный время-зависимый эффект Наибольшая польза бывает получена, если тромболизис был начат в течение первых 6 часов от начала инфаркта, хотя определенная польза может быть получена и до 12 часов.

РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ТРОМБОЛИТИЧЕСКОЙ ТЕРАПИИ ПРИ ОСТРОМ ИНФАРКТЕ МИОКАРДА

КЛАСС I Польза >>> Риск Процедура/лечение ДОЛЖНО быть осуществлено/ назначено Элевация сегмента ST > 1 мм в двух или более отведениях Время от появления симптомом < 12 часов Возраст < 75 лет Блокада ветви пучка Гиса и данные анамнеза, позволяющие предположить наличие инфаркт миокарда

КЛАСС IIа Польза >> Риск ПРИЕМЛЕМО осуществить процедуру/ назначить лечение Подъем сегмента ST Возраст > 75 лет

КЛАСС III Риск ≥ Польза Процедуру/лечение НЕ СЛЕДУЕТ осуществлять/назначать, поскольку они не являются полезными и могут принести вред исключительно депрессия сегмента ST элевация сегмента ST время от появления симптомов > 24 часов отсутствие болевого синдрома

АБСОЛЮТНЫЕ ПРОТИВОПОКАЗАНИЯ К ТРОМБОЛИТИЧЕСКОЙ ТЕРАПИИ Геморрагический инсульт в анамнезе (независимо от давности) Выявленные структурные сосудистые нарушения в головном мозге (например, артериовенозные образования) Выявленные злокачественные новообразования в головном мозге (первичные и метастазы) Ишемический инсульт с давностью до 3 месяцев, ЗА ИСКЛЮЧЕНИЕМ острого ишемического инсульта в течение 3 часов Подозрение на расслаивающую аневризму аорты Продолжающееся кровотечение или геморрагический диатез (кроме менструации) Достоверная травма околосердечных анатомических структур или травма лица давностью до 3 месяцев

ОТНОСИТЕЛЬНЫЕ ПРОТИВОПОКАЗАНИЯ К ТРОМБОЛИТИЧЕСКОЙ ТЕРАПИИ Хроническая, тяжелая, плохо контролируемая артериальная гипертензия в анамнезе Гипертонический криз (АДсист. > 180 мм рт.ст, АДдиаст. > 110 мм рт.ст) Ишемический инсульт с давностью более 3 месяцев, деменция или интракраниальная патология, не входящая в список абсолютных противопоказаний Травматичная или продолжительная (более 10 мин) реанимация или большое оперативное вмешательство (давностью менее 3 недель) Недавнее (до 2-4 недель) внутреннее кровотечение Пункция сосуда, недоступного для остановки кровотечения методом компрессии Для стрептокиназы/антистреплазы: их предшествующее применение (более 5 дней назад) или выявленная ранее аллергическая реакция на эти препараты Беременность Обострение пептической язвы Терапия антикоагулянтами: чем больше MHO, тем выше риск кровотечения

В НАСТОЯЩЕЕ ВРЕМЯ ПРИМЕНЯЮТ СЛЕДУЮЩИЕ ТРОМБОЛИТИЧЕСКИЕ СРЕДСТВА Препараты I поколения (стрептокиназа, урокиназа) Препараты II поколения (проурокиназа, АПСАК) Препараты III поколения тканевые активаторы плазминогена человеческого типа (альтеплаза).

Сравнительная характеристика тромболитеческих препаратов, используемых для лечения инфаркта миокарда

Стрептокиназа обычно назначается в дозе 1.500.000 ЕД, которая разводится в 100 мл изотонического раствора хлорида натрия или 5% раствора глюкозы и вводится внутривенной инфузией течение 30-60 мин. Выпускается под различными коммерческими названиями: "стрептаза", "кабикиназа", "авелизин", "целиаза" и др.

Проурокиназа вводится внутривенно в дозе 8.000.000 МЕ: 2.000.000 МЕ болюс + 6.000.000 МЕ инфузия. Содержимое одного флакона (2.000.000 МЕ) разводится в 20 мл изотонического раствора натрия хлорида и вводится болюсно. Содержимое трех флаконов (6.000.000 МЕ) разводится в 100 мл изотонического раствора натрия хлорида и вводится внутривенно за 60 мин.

Представляет собой гликопротеин, который непосредственно активирует плазминоген, превращая его в плазмин. При в/в введении препарат относительно неактивен в системном кровотоке. Активируется лишь при соединении с фибрином, индуцируя превращение плазминогена в плазмин, что, в результате, приводит к растворению фибринового сгустка. Влияние на компоненты свертывающей системы крови незначительно, поэтому при применении Актилизе, в отличие от других фибринолитиков, не повышается риск развития кровотечений.

СХЕМА ВВЕДЕНИЯ АКТИЛИЗЕ ПРИ ИНФАРКТЕ МИОКАРДА В ПЕРИОД ОТ 6 ДО 12 ЧАСОВ ОТ ПОЯВЛЕНИЯ СИМПТОМОВ 10 мг в виде в/в болюса за 1-2 мин 50 мг в виде в/в инфузии за первый час с последующим введением по 10 мг за каждые 30 мин до общей дозы 100 мг у больных с массой тела менее 65 кг общая доза не должна превышать 1,5 мг/кг массы тела

ОСОБЫЕ УКАЗАНИЯ ПО ТРОМБОЛИТИЧЕСКИХ ПРЕПАРАТОВ Одновременно с введением рекомендуют назначать, антитромбоцитарных препаратов (аспирин в дозе 160-300; клопидогрель-плавикс по 75 мг/сутки). Гепарин следует назначать по схеме: перед началом тромболизиса вводят в/в болюс 5.000 МЕ затем поддерживающую инфузию со скоростью ~1.000 МЕ/час с учетом значений активированного частичного тромбопластинового времени, которые должны быть в пределах 1,5-2,5 раз выше исходных показателей. При возникновении опасного для жизни кровотечения введение препаратов следует прекратить!

ПОБОЧНЫЕ ЭФФЕКТЫ ТРОМБОЛИЗИСА Реперфузионные аритмии. Кровотечение незначительное (из места пункции, изо рта, из носа). Кровотечение тяжелое (желудочно-кишечное, внутричерепное). Частота кровотечений: желудочно-кишечные - 5%, внутричерепные - 0,5-1,0%. Лихорадка. Возникает у 5% больных. Лечение: аспирин или парацетамол. Артериальная гипотония. Возникает у 10-15% больных. Лечение: инфузионная терапия. Сыпь. Возникает у 2-3% больных. Лечение: антигистаминные препараты в/в или внутрь. В тяжелых случаях - кортикостероиды.

Тромболизис высокоэффективен, но возможности его ограничены: вероятность восстановления перфузии не превышает 80%, при этом возможны тяжелые кровотечения. Сегодня показания к тромболизису ограничены (в США его проводят у 25-35%). В связи с этим во многих учреждениях вместо или в дополнение к тромболизису проводят экстренную коронарную ангиопластику.

ЧРЕСКОЖНАЯ ТРАНСЛЮМИНАЛЬНАЯ КОРОНАРНАЯ АНГИОПЛАСТИКА
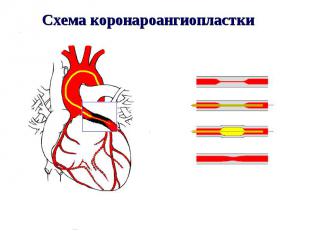

РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ПЕРВИЧНОЙ АНГИОПЛАСТИКИ ПРИ ОСТРОМ ИНФАРКТЕ МИОКАРДА

АБСОЛЮТНЫЕ ПОКАЗАНИЯ К ПЕРВИЧНОЙ АНГИОПЛАСТИКЕ Класс I Должна быть выполнена в инфаркт зависимой артерии в течении первых 12 часов после приступа. Пациенты моложе 75 лет, перенесшие кардиогенный шок в течение 36 часов после инфаркта, которые по данным коронарографии подходят для реваскуляризации и она может быть выполнена в течение 18 часов после шока. Пациенты с кардиогенным шоком или отеком легких, если от начала симптомов прошло не более 12 часов.

АБСОЛЮТНЫЕ ПРОТИВОПОКАЗАНИЯ К ПЕРВИЧНОЙ АНГИОПЛАСТИКЕ КЛАСС III Не должна выполняться в не инфаркт зависимой артерии у пациентов без гемодинамической нестабильности. Не должна выполняться у бессимптомных пациентов через 12 и более часов от начала ИМ с элевацией ST при условии гемодинамической и электрической стабильности.
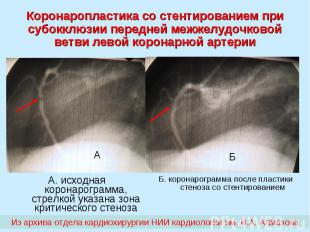
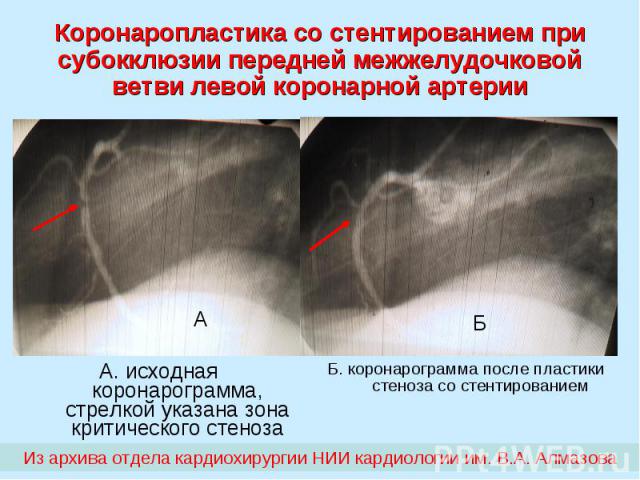
Коронаропластика со стентированием при субокклюзии передней межжелудочковой ветви левой коронарной артерии А. исходная коронарограмма, стрелкой указана зона критического стеноза

АБСОЛЮТНЫЕ УСЛОВИЯ ДЛЯ ПРОВЕДЕНИЯ КОРОНАРНОЙ АНГИОПЛАСТИКИ ПРИ ОСТРОМ КОРОНАРНОМ СИНДРОМЕ Должна быть выполнена в инфаркт зависимой артерии в течение первых 12 часов после приступа. Должна быть выполнена в первые 90 минут после поступления больного в приемный покой. Должна выполняться опытным хирургом, выполняющим более 75 процедур в год в коллективе выполняющем более 200 плановых процедур в год и в клинике с кардиохирургической операционной. Если от начала приступа прошло менее 3 часов и есть возможность выполнить первичную ангиопластику в течение часа. Если таких условий в вашем стационаре нет предпочтительна тромболитическая терапия.

ПРИ ВЫПОЛНЕНИИ ТРАНСЛЮМИНАЛЬНОЙ АНГИОПЛАСТИКИ КАРДИОХИРУРГИЧЕСКОЕ ОТДЕЛЕНИЕ ДОЛЖНО БЫТЬ ГОТОВО ДЛЯ ВЫПОЛНЕНИЯ НЕОТЛОЖНОГО КОРОНАРНОГО ШУНТИРОВАНИЯ!
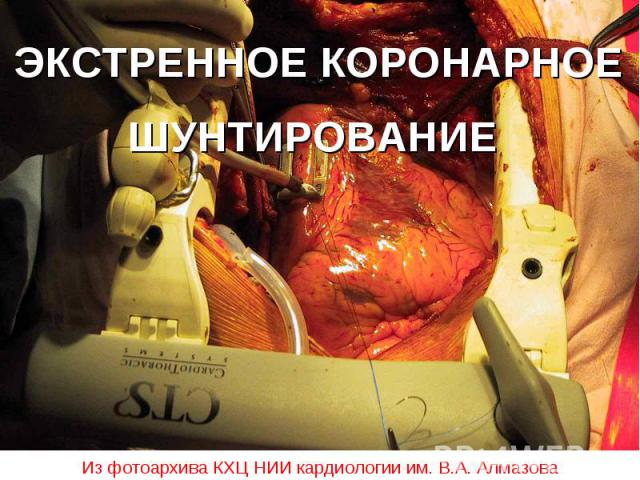
ЭКСТРЕННОЕ КОРОНАРНОЕ ШУНТИРОВАНИЕ

РЕКОМЕНДАЦИИ ПО ЭКСТРЕННОМУ КОРОНАРНОМУ ШИНТИРОВАНИЮ ПРИ ОСТРОМ ИНФАРКТЕ МИОКАРДА

ПОКАЗАНИЯ ДЛЯ ЭКСТРЕННОГО И СРОЧНОГО КОРОНАРНОГО ШУНТИРОВАНИЯ (КШ) КЛАСС I боль или гемодинамическая нестабильность, продолжающиеся после неудачного ЧKB, если коронарная анатомия позволяет выполнить КШ (Уровень достоверности В); продолжающаяся или рецидивирующая ишемия, рефрактерная к медикаментозной терапии при наличии значительного объема миокарда в зоне риска, при условии, что пациент не является кандидатом для ЧKB или ТЛТ (Уровень достоверности В); КШ, сопровождающее хирургическую коррекцию постинфарктного разрыва МЖП или митральной недостаточности (Уровень достоверности В); кардиогенный шок, осложнивший ИМ с элевацией ST, развившийся в первые 36 часов ИМ, у пациентов моложе 75 лет с тяжелым многососудистым поражением или стенозом ствола ЛКА, с коронарной анатомией, доступной для реваскуляризации, которая может быть выполнена в пределах 18 часов течения шока (Уровень достоверности А); жизнеугрожающая желудочковая аритмия при стенозе ствола ЛКА > 50% и/или многососудистом поражении. (Уровень достоверности В).

ПОКАЗАНИЯ ДЛЯ ЭКСТРЕННОГО И СРОЧНОГО КОРОНАРНОГО ШУНТИРОВАНИЯ (КШ) КЛАСС IIa Экстренное КШ может быть выбрано в качестве метода первичной реперфузии в ранние сроки ИМ (6-12 часов), особенно при многососудистом поражении или стенозе ствола ЛКА, если не представляется возможным провести ТЛТ или ЧKB, а коронарная анатомия позволяет выполнить КШ. (Уровень достоверности В) Экстренное КШ может быть эффективным при кардиогенном шоке, осложнившем ИМ с элевацией ST в первые 36 часов ИМ, у пациентов старше 75 лет с тяжелым многососудистым поражением или стенозом ствола ЛКА, с коронарной анатомией, доступной для реваскуляризации, которая может быть выполнена в пределах 18 часов течения шока. Дополнительным условием является хороший предшествующий функциональный статус, согласие больного на дальнейшее инвазивное лечение. (Уровень достоверности В).

Абсолютные противопоказания к экстренному коронарному шунтированию Класс III если, несмотря на сохраняющуюся стенокардию, риску подвергается небольшой объем миокарда и отсутствует нестабильность гемодинамики, проведение экстренного КШ нецелесообразно. (Уровень достоверности С); экстренное КШ не показано, если после удачной реперфузии эпикардиальной артерии возникают выраженные нарушения микроциркуляции в коронарном русле. (Уровень достоверности С).

З А П О М Н И Т Е ! Больные инфарктом миокарда с элевацией сегмента ST, что является очевидным признаком тромботической окклюзии коронарной артерии, делает их кандидатами для немедленной реперфузионной терапии одним из методов: тромболизиз ангиопластика коронарное шунтирование.

Для достоверного снижения существующей 30% летальности от инфаркта миокарда необходимо: Снизить на 50% время от возникновения симптомов до поступления больного в стационар. Более широкое использование тромболизиса. Ежедневное использование аспирина в дозе 160-325 мг в течение неопределенного периода, возможно это является единственным наиболее важным и универсальным методом лечения больных инфарктом миокарда. Для пациентов, не переносящих или устойчивых к аспирину альтернативой, является тиклопидин (плавикс). Широкое и повсеместное внедрение методов интервенционной кардиологии и кардиохирургии.

«Отделение интенсивной терапии для больных с острым коронарным синдромом – самое важное улучшение в лечении острого инфаркта миокарда. Оно базируется на результатах 4-х разработок: возможности продолжительного мониторирования ЭКГ важность оценки аритмий, как основных причин ранней смерти при инфаркте миокарда обучение медсестер алгоритмам лечения жизнеугрожающих аритмий, которые они должны были выполнять в отсутствие врачей развитие непрямой сердечной реанимации» Braunwald's Heart Disease: A Textbook of Cardiovascular Medicine, 7th ed., 2005 Saunders.