Презентация на тему: Закон сохранения массы веществ. Уравнения химических реакций

Общая средняя школа № 36 имени Казыбек би Закон сохранения массы веществ. Уравнения химических реакций. Составила : учитель химии, биологии высшей квалификационной категории: Палжанова А.Ш. 2011 год

Единственный путь, ведущий к знанию, - это деятельность. Цели урока: Обучающие - экспериментально доказать закон сохранения массы веществ. На основе этого закона сформировать понятие о материальном балансе химической реакции. Сформировать понятие об уравнении химической реакции как об условной записи, отображающей превращения веществ. Развивающие - развивать умения ставить несложные проблемы, формулировать гипотезы и проводить их опытную проверку; совершенствовать умения работать с лабораторным оборудованием и реактивами ; развивать способность к логическому мышлению.Воспитательные - продолжить формирование научного мировоззрения учащихся; воспитывать коммуникативную компетентность, а также наблюдательность, внимание, инициативу. На примере жизни и деятельности М. В. Ломоносова воспитывать интерес к изучению химии.

Открытие закона сохранения массы веществ

Бойль проделал множество опытов по прокаливанию металлов в запаянных ретортах и всякий раз масса окалины оказывалась больше массы прокаливаемого металла.

Вот что записал учёный после одного из своих опытов в 1673 году. «После двух часов нагревания был открыт запаянный кончик реторты, причём в неё ворвался с шумом наружный воздух. По нашему наблюдению при этой операции была прибыль в весе на 8 гранов…»

Русский учёный М.В. Ломоносов предположил, что чувственный опыт обманывает нас. 5 июля 1748 года он написал в письме Леонарду Эйлеру:

«Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимется, столько же присовокупится к другому. Так, ежели где убудет материи, то умножится в другом месте; сколько часов положит кто на бдение, столько же сну отнимет...»

«Масса веществ, вступивших в реакцию, равна массе образовавшихся веществ в результате реакции» - современная формулировка закона сохранения массы веществ.


Лишь в 1756 году Ломоносову удалось проверить опытным путём теоретически открытый закон сохранения массы веществ. Подобно Бойлю русский учёный делал опыт в запаянных ретортах. Но, в отличие от Бойля, Ломоносов взвешивал сосуды как до, так и после прокаливания не вскрывая.


Значительно позже этот закон,независимо от М.В. Ломоносова,был открыт французским ученым А.Лавуазье.


Химическая формула – условная запись состава вещества с помощью химических знаков и индексов. Индекс показывает число атомов в формульной единице вещества. Коэффициент показывает число несоединенных друг с другом частицНа основании данного закона составляютуравнения химических реакций с помощью химических формул, коэффициентов и математических знаков.

Химические уравнения Химическое уравнение – условная запись химической реакции с помощью химических формул и коэффициентов
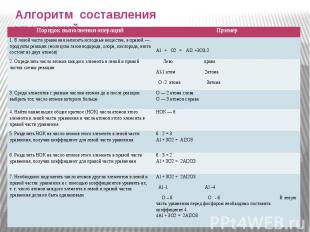
Алгоритм составления уравнений

составить уравнения химических реакций 1) Са + О2 → СаО 2) К + О2 → K2O3) H2 + O2 →H2O

Cu + Cl2 → CuCl2

Запишите уравнение реакции взаимодействия меди с кислородом ( вспомните видеофрагмент)

Домашнее задание: § 14,15 стр.40 №6,7.