Презентация на тему: Соединения химических элементов. Степень окисления

Соединения химических элементов Степень окисленияСоставила учитель химииМБОУ «Октябрьская ООШ №2»Потапова Нина Ивановна

Бинарные соединения – сложные вещества, состоящие из двух химических элементов. NaCl Хлорид натрия Na0+Cl0=Na+Cl‾ Связь ионная +11Na )2)8)1 Атом натрия передал свой внешнийэлектрон атому хлора и превратился с зарядом +1, а атом хлора принял электрон и превратился в ион с зарядом -1 HClХлороводородHδ+Clδ-Связь ковалентная полярная +1Н )1 +17Cl )2)8)7 В молекуле хлороводорода связь образуется за счёт спаривания одиночных внешних электронов и образования общей электронной пары, которая смещена в сторону более электроотрицательного атома хлора.

Степень окисления – это условный заряд атомов химических элементов в соединении. Она может иметь отрицательное, положительное или нулевое значение. Ставится над символом элемента сверху. Необходимо запомнить!В соединениях с ионной связью степени окисления элементов равны зарядам ионов.Na+1Cl-1, Ca+2F2-1, Mg+2O-2.В соединениях с ковалентной неполярной связью (в молекулах простых веществ) степень окисления элементов равна нулю.H2º, Cl2º, O2º, F2º, Siº, Cº, Sº …В соединениях с ковалентной полярной связью степень окисления элемента – это условный заряд его атома в молекуле, если считать, что молекула состоит из ионов.H+1Cl-1, H2+1O-2Алгебраическая сумма степеней окисления в соединении всегда равна нулю.

Элементы с постоянной степенью окисления Щелочные металлы ( I группа, главная подгруппа) +1Li, Na, K, Rb, Cs, FrЭлементы II группы (кроме Hg) +2Be, Mg, Ca, Sr, Ba, Ra, Zn, CdАлюминий Al +3Фтор F -1Все другие элементы имеют переменную степень окисления
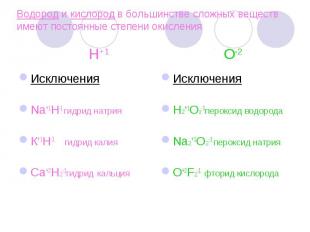
Водород и кислород в большинстве сложных веществ имеют постоянные степени окисления Н+1 О-2 ИсключенияNa+1H-1 гидрид натрияК+1Н-1 гидрид калияСа+2Н2-1гидрид кальция ИсключенияН2+1О2-1пероксид водородаNa2+1O2-1 пероксид натрияO+2F2-1 фторид кислорода

Степень окисления сокращённо обозначают с.о. Для того, чтобы рассчитать с.о. одного элемента в соединении, надо знать с.о. другого элемента. Найдите с.о. хлора в соединениях Cl2O, Cl2O7. Мы знаем с.о. кислорода Cl2O-2.Определим общий отрицательный заряд кислорода:(-2)·1=-2Общий заряд двух атомов хлора должен быть +2, чтобы суммарная с.о. была =0.Найдём заряд одного атома хлора:(+2) : 2=+1Следовательно степень окисления хлора =+1Cl2+1O-2

Определите самостоятельно с.о. элементов в следующих соединениях:NO, NO2, CuCl2-1, CuCl-1, BaH2, MgF2, Al2S3. Проверьте себя:N+2O-2, N+4O2-2, Cu+2Cl2-1, Cu+1Cl-1, Ba+2H2-1, Mg+2F2-1, Al2+3S3-2.Домашнее задание: § 17 (ст. 26-28)Определите с.о. элементов в следующих соединениях:N2O5, N2O3, K3N, Ca3N2, MnCl2, MnCl4, PCl3, PCl5.