Презентация на тему: Строение электронных оболочек атомов

Строение электронных оболочек атомов Задачи урока: Познакомиться со строением электронных оболочек атомов Научиться составлять схемы строения электронных оболочек

Соотнесите химические формулы и формы существования химических элементов1) 2S2) S83) 3H2O4) Al2O35) 2Al6) CuO1) свободные атомы2) простые вещества3) сложные вещества

1) Атом – это частица, состоящая из ……2) Целочисленное значение массы атома определяется суммой масс частиц: …3) Порядковый номер элемента показывает число ….. и число ….. в атоме4) Атомы одного химического элемента, отличающиеся величиной относительной атомной массы называют ……. 5) Вид атомов с определенным зарядом ядра называют ….6)Запишите с помощью условных обозначений состав атома цинка. Вариант 21) Атомное ядро состоит из ….2) Изотопы отличаются количеством …..3) Массовое число атома – это сумма масс частиц ….4) Число ….. = числу .... = порядковому номеру элемента.5)Электрон обозначается …., имеет заряд …., массу приблизительно равную ….6) Запишите с помощью условных обозначений состав атома меди.

Вариант 1 протонов, нейтронов, электронов протонов и нейтронов протонов и электронов 4) изотопы 5) химический элемент 6) P = 30, n = 35, e = 30 Вариант 21) протонов и нейтронов 2) нейтронов 3) протонов и нейтронов 4) протонов = электронов5)е, -1, 0 6) P = 29, n = 35, e = 29

Почему в Периодической системе относительная атомная масса элементов имеет дробное значение?Какие изотопы (легкие или тяжелые) более распространены в природе для элементов:А) калияБ) аргонаВ) хлора

«Сведение множества к единому – в этом первооснова красоты». Пифагор.



В микромире иные законыОбсуждая строение электронных оболочек создаем их модель

Энергетические уровни Какой электрон имеет наибольший запас энергии?Какие электроны имеют примерно одинаковый запас энергии?
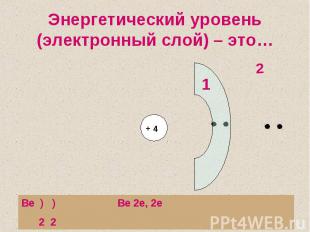
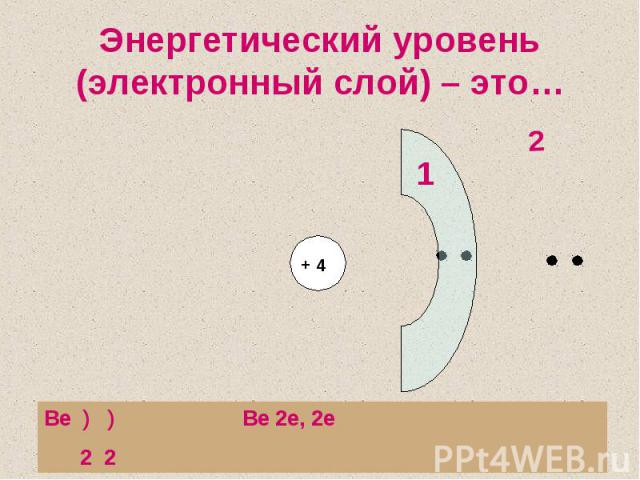
Энергетический уровень (электронный слой) – это…
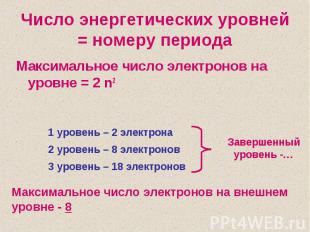
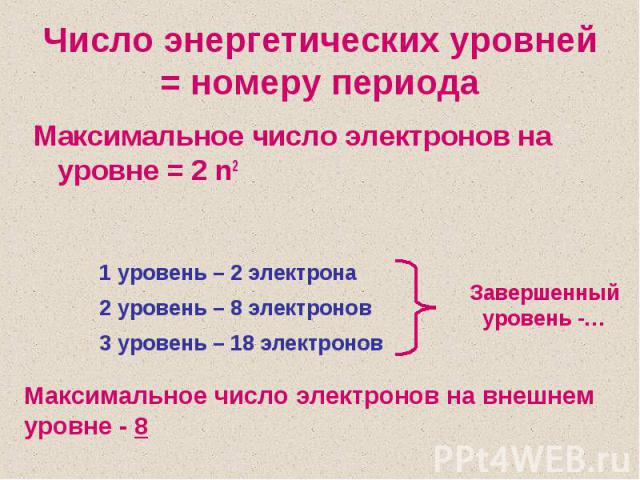
Число энергетических уровней = номеру периодаМаксимальное число электронов на уровне = 2 n2Максимальное число электронов на внешнем уровне - 8

Запишите схемы строения электронных оболочек атомов: углерода, азота,кислорода, фтора.Соотнесите число электронов на внешнем уровне и номер группыЧисло электронов на внешнем уровне равно номеру группы

Повторение1. Электроны в атомах располагаются …2. Электроны одного энергетического уровня имеют примерно одинаковый …3. Число уровней равно ….4. Максимальное число электронов на уровне = …5. Уровень, содержащий максимальное количество электронов называют …6. Завершенный внешний уровень содержит ….. электронов7. Число электронов на внешнем уровне = …

Электронная облако. Электронная орбитальS - орбиталь

Электронная орбитальР - орбиталь

Электронная орбиталь

На одной орбитали не может находится более 2 электроновКоличество орбиталей на уровнях равно номеру уровня.1 уровень – S - орбиталь2 уровень – S, P - орбитали

Электронные формулыH )1 1S1He )2 1S2C )2 )41S2 2S22P2OFNa

Повторение 1. Пространство вокруг ядра атома ,где наиболее вероятно нахождение электрона называют ….2. S и P – орбитали различаются ….3. Каждый уровень начинается ... орбиталью4. На S – орбитали может находиться …. электрона, на Р – орбиталях - …. Электронов5. Объясните, что обозначают цифры и буквы в записи: 1S2 2S22P2