Презентация на тему: Строение электронных оболочек атомов

Интегрированный урок. Интеграция физики с химией 8 класс. Учитель физики: Литовченко Любовь Михайловна. Учитель химии: Орлова Ирина Григорьевна. «Отыщи всему начало и ты многое поймёшь». (Кузьма Прутков.) 900igr.net

Тема урока "Строение атома и его электронных оболочек». Цель урока: сформировать у учащихся понятия о строении атома и электронных оболочек, познакомить с планетарной моделью по Резерфорду. Научить составлять электронные формулы атомов.

Актуализация знаний: а) Как на опыте показать, что электрический заряд делится на части? б) Можно ли электрический заряд делить бесконечно? в) Как называют частицу с самым малым зарядом? г) Что вы знаете о заряде и массе электрона? д) Назовите величины, не имеющие единиц измерения. е) Определите Аr(О), Аr(К), Аr(Ва), Аr(В).

В 1903г. английский физик Джозеф Джон Томсон предложил одну из первых моделей строения атома.

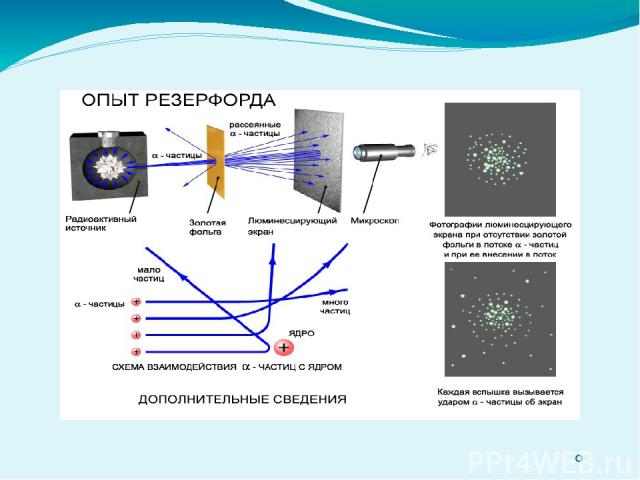
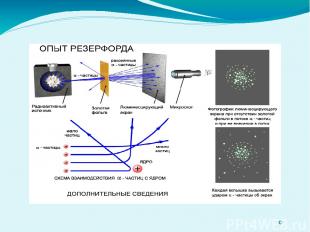
Модель строения атома Томсона нуждалась в экспериментальной проверке Поэтому в 1911 г. Резерфорд совместно со своими сотрудниками провел ряд опытов по исследованию состава и строения атомов. Эрнест Резерфорд (1871-1937) — английский физик, один из создателей учения о радиоактивности и строении атома, основатель научной школы, иностранный член-корреспондент РАН (1922) и почетный член АН СССР (1925).
°

Резерфорд предложил ядерную («планетарную») модель атома: * атомы любого элемента состоят из положительно заряженной части, получившей название ядра; * в состав ядра входят положительно заряженные элементарные частицы- протоны (позднее было установлено, что и нейтральные нейтроны); * вокруг ядра вращаются электроны, образующие так называемую электронную оболочку атома.
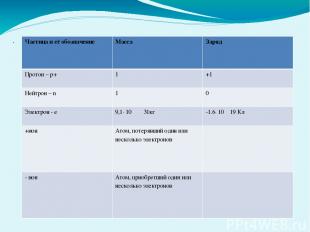
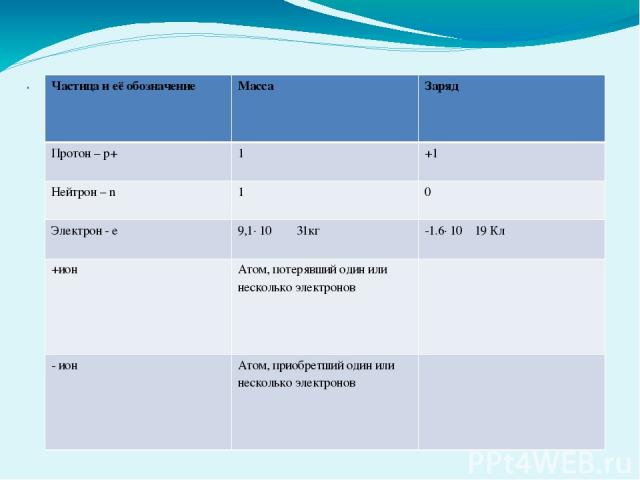
. Частица и её обозначение Масса Заряд Протон – р+ 1 +1 Нейтрон –n 1 0 Электрон - е 9,1∙ 10 31кг -1.6∙ 10 19Кл +ион Атом, потерявший один или несколько электронов - ион Атом, приобретший один или несколько электронов

Максимальное число электронов на энергетическом уровне. I ___ 2 II_______ 8 III___________18 Число энергетических уровней равно номеру периода в таблице Д.И.Менделеева.
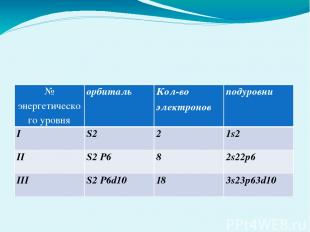
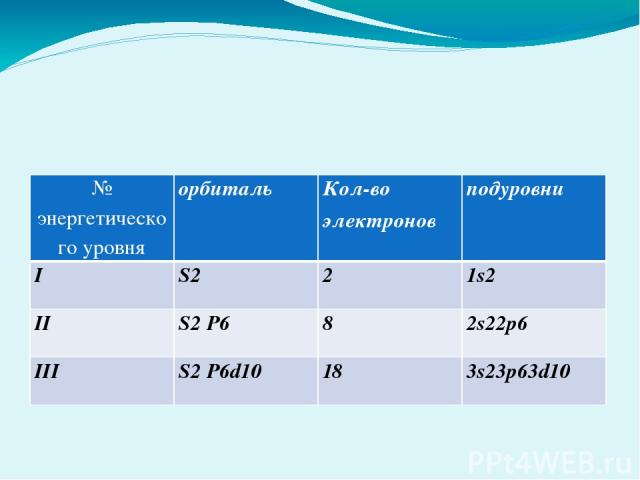
№ энергетического уровня орбиталь Кол-во электронов подуровни I S2 2 1s2 II S2P6 8 2s22p6 III S2P6d10 18 3s23p63d10

Обобщение изученного материала. В ядре атома углерода содержится 12 частиц. Вокруг ядра движутся 6 электронов. Сколько в ядре этого атома, протонов и сколько нейтронов? Атом хлора принял один электрон. Как называется полученная частица? Какой ее заряд? Какая модель атома вытекает из опытов Э. Резерфорда? Почему модель, предложенная Э. Резерфордом, называется планетарной? Чему равно число энергетических уровней химического элемента в таблице Д.И.Менделеева? Сколько электронов находится на III энергетическом уровне?

Домашнее задание: по физике: §30. Упр.11. Используя изученные на уроке термины: атом, ядро, оболочка, протон, нейтрон, электрон; фамилии ученых: Томсон, Резерфорд, составить кроссворд. По химии: §8.Упр.3.