Презентация на тему: Скорость химической реакции

ХИМИЧЕСКАЯ КИНЕТИКА Скорость химической реакции - - развитие реакции во времени Лектор Мирошниченко Ю.Ю. 900igr.net

План лекции 1. Основные понятия 2. Классификация процессов 3. Скорость химической реакции 4. Влияние концентрации реагента на скорость реакции 5. Влияние температуры на скорость 6. Явление катализа

Химическая кинетика - раздел химии, изучающий скорость и механизмы химических реакций Термодинамика - наука о макросистемах Химическая кинетика рассматривает их механизм реакций на уровне отдельных частиц Кинетика и термодинамика дают целостное представление о закономерностях протекания реакций

Классификация процессов по фазовому составу 1) гомогенные - протекающие по всему объему реагирующих веществ 2) гетерогенные - протекающие на границе фаз 3) топохимические c изменением структуры реагирующих твердых в-в Пример: разложение карбонатов при to CaCO3 (кр)=CaO(кр)+CO2 (газ)

Классификация по механизму реакции Механизм реакций - совокупность элементарных стадий слагающих процесс Простой процесс - протекает в одну стадию (реагент продукт) Сложный процесс – многостадийный (реагент промежуточные продукты конечный продукт)

Молекулярность реакций По числу молекул одновременно участвующих в хим. превращении простые реакции делятся на: Мономолекулярные N2O4 = 2NO2 Бимолекулярные NO + H2O = NO2 + H2 Тримолекулярные 2NO + Cl2 = 2NOCl

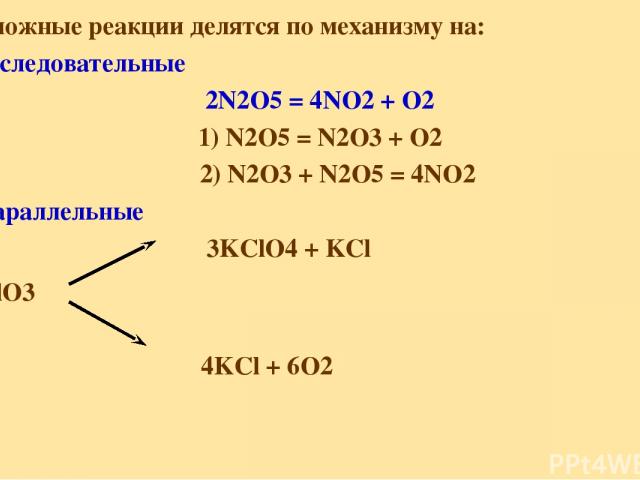
Сложные реакции делятся по механизму на: последовательные 2N2O5 = 4NO2 + O2 1) N2O5 = N2O3 + O2 2) N2O3 + N2O5 = 4NO2 Параллельные 3KClO4 + KCl 4KClO3 4KCl + 6O2

Цепные - неразветвленные р-ции Это реакции, в которых возникают промежуточные активные частицы, вызывающее большое число (цепь) превращений исходной молекулы Пример: H2+Cl2 = 2HCl Cl2 = 2Cl• H2 + Cl• = HCl + H• H• + Cl2 = HCl + Cl• и т.д. h

Цепные - разветвленные реакции Н2 + 0,5О2 = Н2О Зарождение цепи: Н2+ О2 = 2ОН Развитие цепи: ОН + Н2 = Н2О + Н Разветвление цепи: Н +О2 = ОН + О О + Н2 = ОН + Н Обрыв цепей: ОН + ОН Н2О2 О + О О2 Обрыв цепи осуществляют ингибиторами [Pb(C2H5)4 , добавляемый в бензин]

Лимитирующая стадия это самая медленная стадия в сложном процессе и скорость ее протекания определяет (лимитирует) скорость всего процесса

Скорость химической реакции это число элементарных актов взаимодействия, происходящих в единицу времени в единице объема для гомогенных реакций или на единице поверхности раздела фаз для гетерогенных реакций: Vгом = = Vгетер = n V t n S t C t

Скорость как функция изменения концентрации Взаимодействия атомов и молекул фиксировать невозможно, поэтому о скоростях реакций судят по изменению различных параметров: концентрации реагентов или продуктов за определенный промежуток времени, (а также массы, давления, объема, окраски, электропроводности, и т. д.)
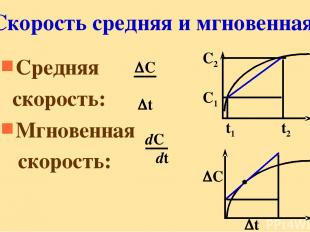
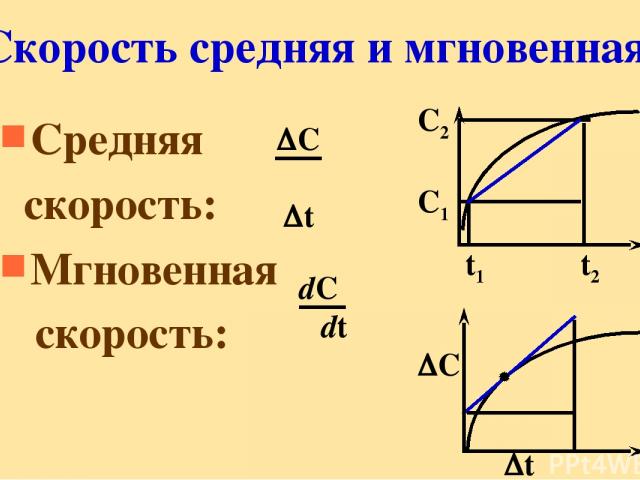
Скорость средняя и мгновенная Средняя скорость: Мгновенная скорость: С2 С1 t1 t2 C t C t dC dt

Для реакции в общем виде скорость химической реакции с учетом стех-ких коэффициентов: aA + bB = cC + dD Vt = - = - = = dCA dt dCD dt dCB dt dCC dt

Общая закономерность Скорость химической реакции, проводимой без добавления реагентов извне, максимальна в начале (конц-ции реагентов мах) и минимальна в конце (конц-я реагентов - мin)

Реакции, скорость которых постоянна: Автокаталитические реакции - скорость возрастает скорость возрастает в некоторые промежутки времени от начала реакции (продукты реакции являются её катализаторами) Автоколебательные реакции - скорость то ум-ся, то ув-ся

Факторы, влияющие на скорость реакции Природа Концентрация веществ Температура Катализаторы На скорость гетерогенных р-ций кроме того влияет величина поверхности, т.е. размер частиц твердого вещества На скорость цепных реакций – размеры и форма реакционного сосуда

Влияние природы и концентрации реагентов на скорость реакций Закон действующих масс К. Гульдберг, П. Вааге (1867), Я. Вант-Гофф (1877) Скорость простой реакции при постоянной температуре пропорциональна произведению концентраций реагентов в степени их стехиом-х коэффициентов

В общем случае: aA + bB + dD + ..... V = kC C C ...... a A b B d D

Кинетическое уравнение Для простой реакции: аА + bВ = сС +dD математическое выражение ЗДМ: V = k C C V – скорость реакции k – константа скорости реакции CA и CB – молярные конц-ции реаг-в а и b – кинетический порядок реакции по веществу А и В соответственно a A b B

Пример записи кинетического уравнения простой реакции 1) C2H5OH = C2H4 + H2O V=kС(C2H5OH) 2) 2HI = H2 + I2 V = k С2(HI) 3) 2NO + Cl2 = 2NOCl V = k C2(NO)C(Cl2) Общий кинетич-й порядок простой реакции равен ее молекулярности
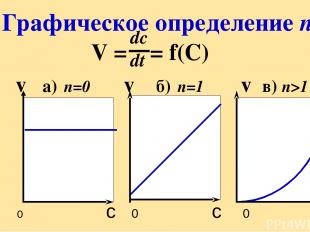
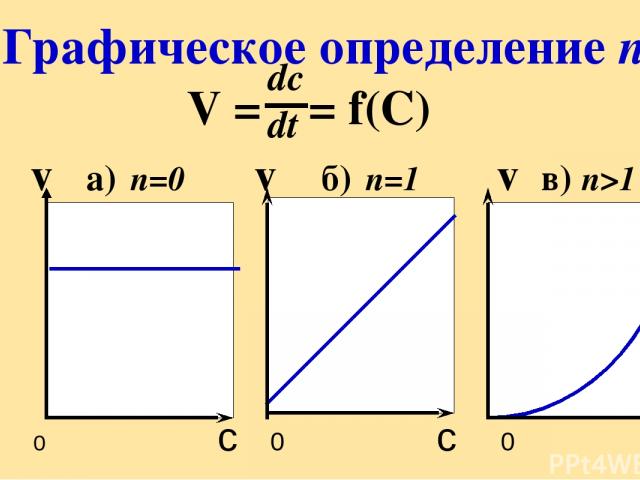
V = = f(С) v а) n=0 v б) n=1 v в) n>1 Графическое определение n 0 c 0 c 0 c dc dt

Кинетическое уравнение сложной реакции аА + bВ=сС + dD V = k C C m и n – небольшие целые или дробные числа, определяются опытным путем (не совпадает с коэффициентами в уравнении) m A n B

Пример: Реакцию 2H2(г) + O2(г) = 2H2O(г) провели при одном давлении, а затем при давлении в 10 раз большем. Как изменилась скорость реакции , если кинетическое уравнение сложной цепной реакции имеет вид: V = k [H2]0,4 • [O2]0,3 Решение: При росте Р в 10 раз [H2] и [O2] ув-ся в 10 раз, тогда V1 = k(10[H2])0,4(10[O2])0,3 = 100,7 Ответ: Cк-ть увел-сь в 100,7, т.е. в 5 раз

Константа скорости реакции Физ. смысл k вытекает из V = k C C При конц-циях реагентов CA = CB = 1 моль/л - это удельная скорость реакции Константа при постоянной to зависит только от природы веществ и не зависит от их концентрации Размерность К n=0, [K] = [моль/лс] n=1, [K] = [1/с] n=2, [K] = [л/мольc] a A b B

Период полупревращения Время полупревращения (t1/2) для реакций называют периодом полураспада (не зависит от начальной концентрации вещества) n = 0; t1/2 = C0/2k n = 1; t1/2 = 0,69/k n = 2; t1/2 = 1/C0k

Скорость гетерогенных реакций зависит от удельной поверхности и концентраций реагентов в газовой фазе или в растворе V=kSуд(реаг)С(реаг) Пример: CaO(к)+CO2(г)=CaCO3(г) V=kSуд(CaO)С(CO2) Sуд(CaO) – уд. поверхность оксида

Уд. поверхность по ходу реакции мало изменяется , поэтому ее объединяют с конст. скорости р-ции Пример: записать кинетическое уравнение гетерогенной реакции: C(к) + O2(г) = CO2 (г) объяснить, почему на тепловых электростанциях уголь перед сжиганием измельчают Ответ:V = kSуд(C)С(O2) или V =ki С(O2)

Константа равновесия с позиции кинетики Для простой обратимой реакции: аА+bВ сС+dД V = Vпр–Vобр = kпрC C –kобрC C В состоянии равновесия: Vпр = Vобр; kпр[A]a[B]b = kобр[C]c[Д]d a A b B c C d D

Зависимость скорости от температуры (Правило Вант-Гоффа) При увеличении температуры на 10 градусов скорость простой реакции возрастает в 2 4 раза: Т Т0 , - темпер-ый коэф-т

Теория активации Аррениуса Хим. реакция может происходить только при столкновении активных частиц, т.е. тех, которые обладают характерной для данной реакции энергией, необходимой для преодоления сил отталкивания между электронными оболочками частиц

Энергия активации (Еа, кДж/моль) – это избыточный запас энергии молекулы над средне статистическим запасом энергии, позволяющий молекуле реализовать хим. взаимодействие

Cогласно молекулярно-кинетической теории газов для каждой системы существует порог энергии Еа , начиная с которого энергия достаточна для протекания реакции Еа меняется от 0 до 500кДж/моль

Еа - велика, скорость реакции – мала Еа – мала, скорость – велика Уравнение Аррениуса

ПРЕДЭКСПОНЕНТА И ЭКСПОНЕНТА Предэкспоненциальный множитель (А) дает некоторую характеристику полного числа столкновений доля результативных столкновений
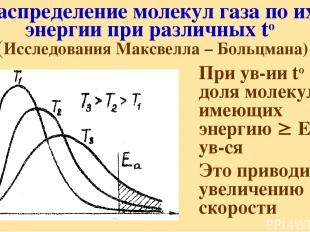
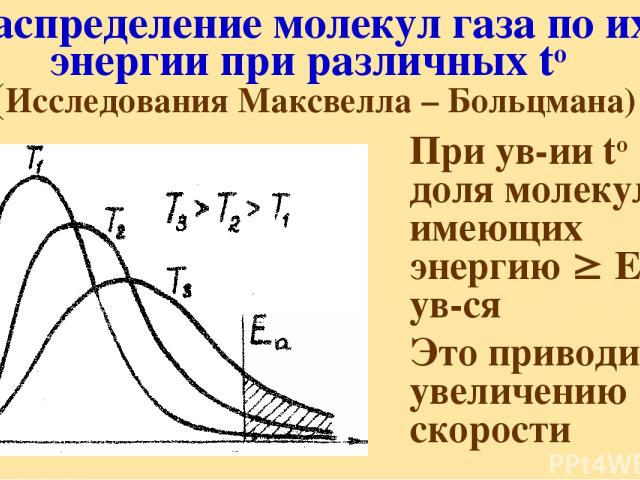
Распределение молекул газа по их энергии при различных to (Исследования Максвелла – Больцмана) При ув-ии to доля молекул, имеющих энергию Еа ув-ся Это приводит к увеличению скорости
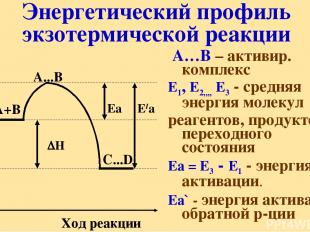
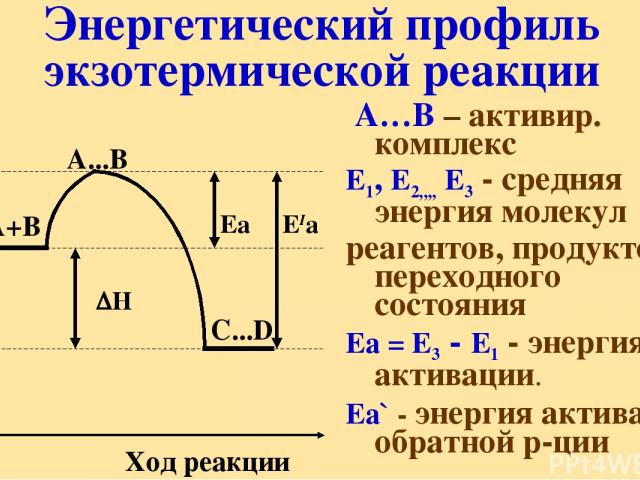
ЕIа А…В – активир. комплекс Е1, Е2,,,, Е3 - средняя энергия молекул реагентов, продуктов, переходного состояния Еа = Е3 - Е1 - энергия активации. Еа` - энергия активации обратной р-ции Энергетический профиль экзотермической реакции
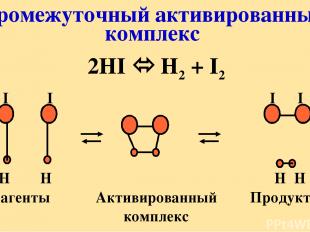
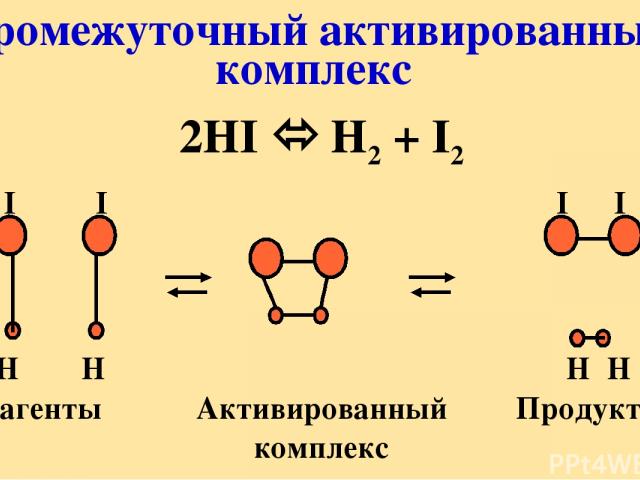
Промежуточный активированный комплекс 2HI H2 + I2 I I I I H H H H Реагенты Активированный Продукты комплекс

Определение энергии активации

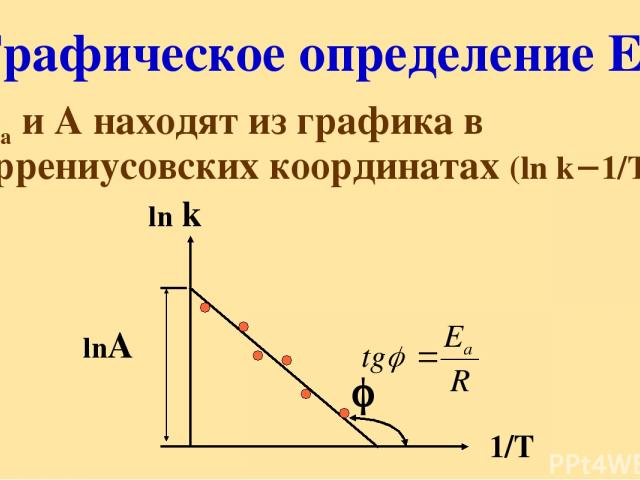
Графическое определение Еа Еа и А находят из графика в аррениусовских координатах (ln k 1/Т) ln k lnА

Способы активации молекул термический светом ионизирующее излучение , - излучение корпускулярные и др. механохимическая звуковая активация

Катализ

Катализ – это явление ускорения реакции под действием веществ не расходующихся в реакции Каталитические реакции – это реакции, в которых изменяется путь при неизменных реагентах и продуктах

Катализатор – это вещество, которое многократно участвует в промежуточных стадиях реакции, но выходит из нее химически неизменным Еа промежуточных стадий с участием катализатора меньше, чем Еа р-ции без катализатора
![Энергетический профиль реакции А + В = АВ (без катализатора) А+ В + К [AK] + В [ Энергетический профиль реакции А + В = АВ (без катализатора) А+ В + К [AK] + В [](https://fs3.ppt4web.ru/images/132073/183920/310/img44.jpg)
Энергетический профиль реакции А + В = АВ (без катализатора) А+ В + К [AK] + В [AKB] AB + K (с кат.)
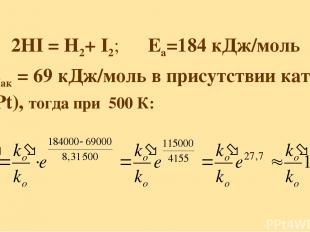
2HI = H2+ I2; Еа=184 кДж/моль Еак = 69 кДж/моль в присутствии кат-ра (Pt), тогда при 500 К:

Гомогенный катализ (кат-р и реагент образуют одну фазу) Пример: получение SO3 окислением SO2 в технологии получения H2SO4 Катализатор NO2 ; все вещества - газы 1) SO2 + NO2 = SO3 + NO 2) NO + 1/2О2 = NO2 SO2 + 1/2О2 = SO3

Гетерогенный катализ Получение H2SO4 с помощью Pt кат-ра SO2 (г) + 1/2О2 (г) = SO3 (г) Эффективность гетерогенных кат-ров больше чем гомогенных Скорость реакций в гомогенном катализе зависит от концентрации кат-ра, а для гетерогенного - от его удельной поверхности





















![Пример: Реакцию 2H2(г) + O2(г) = 2H2O(г) провели при одном давлении, а затем при давлении в 10 раз большем. Как изменилась скорость реакции , если кинетическое уравнение сложной цепной реакции имеет вид: V = k [H2]0,4 • [O2]0,3 Решение: При росте Р … Пример: Реакцию 2H2(г) + O2(г) = 2H2O(г) провели при одном давлении, а затем при давлении в 10 раз большем. Как изменилась скорость реакции , если кинетическое уравнение сложной цепной реакции имеет вид: V = k [H2]0,4 • [O2]0,3 Решение: При росте Р …](https://fs3.ppt4web.ru/images/132073/183920/640/img23.jpg)




![Константа равновесия с позиции кинетики Для простой обратимой реакции: аА+bВ сС+dД V = Vпр–Vобр = kпрC C –kобрC C В состоянии равновесия: Vпр = Vобр; kпр[A]a[B]b = kобр[C]c[Д]d a A b B c C d D Константа равновесия с позиции кинетики Для простой обратимой реакции: аА+bВ сС+dД V = Vпр–Vобр = kпрC C –kобрC C В состоянии равновесия: Vпр = Vобр; kпр[A]a[B]b = kобр[C]c[Д]d a A b B c C d D](https://fs3.ppt4web.ru/images/132073/183920/640/img28.jpg)











![Энергетический профиль реакции А + В = АВ (без катализатора) А+ В + К [AK] + В [AKB] AB + K (с кат.) Энергетический профиль реакции А + В = АВ (без катализатора) А+ В + К [AK] + В [AKB] AB + K (с кат.)](https://fs3.ppt4web.ru/images/132073/183920/640/img44.jpg)














