Презентация на тему: Серная кислота

Определение и свойства Определение и свойства Название Олеум Химические свойства История Сырье для производства Стадии получения Процесс добычи
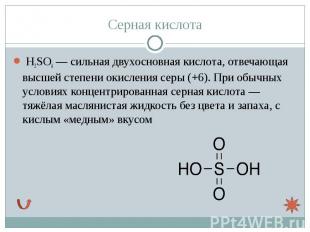
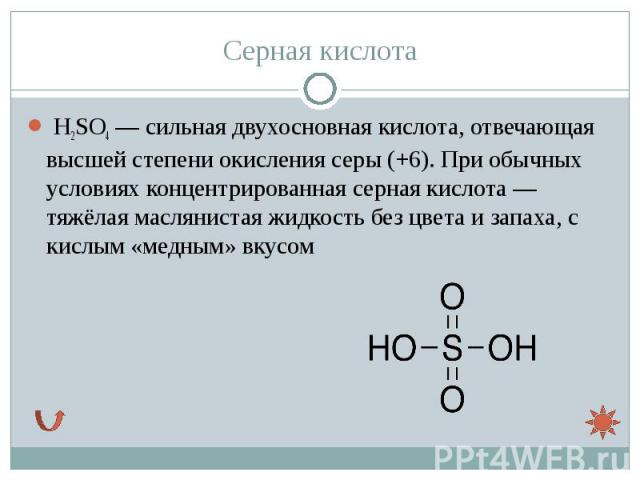
H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с кислым «медным» вкусом H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с кислым «медным» вкусом
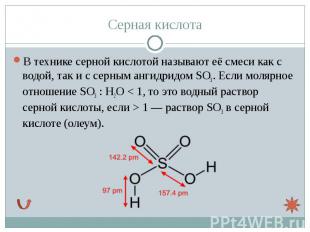
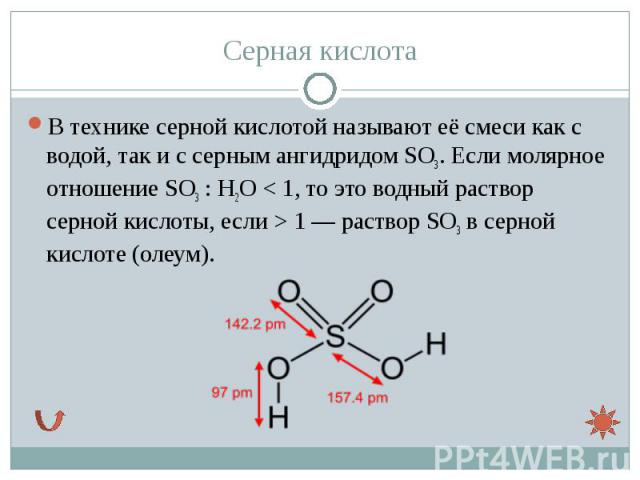
В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O < 1, то это водный раствор серной кислоты, если > 1 — раствор SO3 в серной кислоте (олеум). В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O < 1, то это водный раствор серной кислоты, если > 1 — раствор SO3 в серной кислоте (олеум).

До XX века часто серную кислоту называли купоросом (как правило это был кристаллогидрат, по консистенции напоминающий масло) или купоросным маслом, очевидно отсюда происхождение названия ее солей (а точнее именно кристаллогидратов) — купоросы. До XX века часто серную кислоту называли купоросом (как правило это был кристаллогидрат, по консистенции напоминающий масло) или купоросным маслом, очевидно отсюда происхождение названия ее солей (а точнее именно кристаллогидратов) — купоросы.

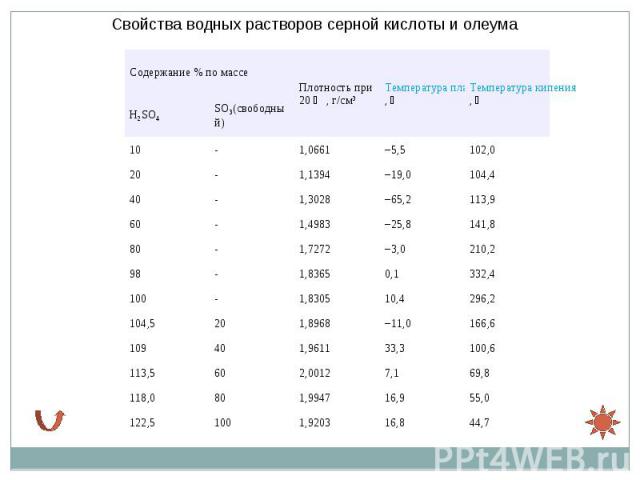
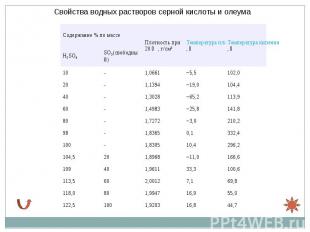
Растворы серного ангидрида SO3 в серной кислоте называются олеумом, они образуют два соединения H2SO4·SO3 и H2SO4·2SO3. Растворы серного ангидрида SO3 в серной кислоте называются олеумом, они образуют два соединения H2SO4·SO3 и H2SO4·2SO3. Олеум содержит также пиросерные кислоты, получающиеся по реакциям: Температура кипения водных растворов серной кислоты повышается с ростом ее концентрации и достигает максимума при содержании 98,3 % H2SO4.

Серная кислота — довольно сильный окислитель, особенно при нагревании и в концентрированном виде; окисляет HI и частично HBr до свободных галогенов, углерод до CO2, серу — до SO2, окисляет многие металлы (Cu, Hg и др.). При этом серная кислота восстанавливается до SO2, а наиболее сильными восстановителями — до S и H2S. Концентрированная H2SO4 частично восстанавливается водородом, из-за чего не может применяться для его сушки. Разбавленная H2SO4 взаимодействует со всеми металлами, находящимися в электрохимическом ряду напряжений левее водорода с его выделением. Окислительные свойства для разбавленной H2SO4 нехарактерны. Серная кислота образует два ряда солей: средние — сульфаты и кислые —гидросульфаты, а также эфиры. Известны пероксомоносерная (или кислота Каро) H2SO5 и пероксодисерная H2S2O8 кислоты. Серная кислота — довольно сильный окислитель, особенно при нагревании и в концентрированном виде; окисляет HI и частично HBr до свободных галогенов, углерод до CO2, серу — до SO2, окисляет многие металлы (Cu, Hg и др.). При этом серная кислота восстанавливается до SO2, а наиболее сильными восстановителями — до S и H2S. Концентрированная H2SO4 частично восстанавливается водородом, из-за чего не может применяться для его сушки. Разбавленная H2SO4 взаимодействует со всеми металлами, находящимися в электрохимическом ряду напряжений левее водорода с его выделением. Окислительные свойства для разбавленной H2SO4 нехарактерны. Серная кислота образует два ряда солей: средние — сульфаты и кислые —гидросульфаты, а также эфиры. Известны пероксомоносерная (или кислота Каро) H2SO5 и пероксодисерная H2S2O8 кислоты.

Серная кислота реагирует также с основными оксидами, образуя сульфат и воду. На металлообрабатывающих заводах раствор серной кислоты применяют для удаления слоя оксида металла с поверхности металлических изделий, подвергающихся в процессе изготовления сильному нагреванию. Так, оксид железа удаляется с поверхности листового железа действием нагретого раствора серной кислоты.

Несмотря на то, что серная кислота давно известна, вначале ее получали сухой перегонкой, поэтому упоминается под названием "купоросное масло", в промышленных количествах она стала производиться относительно недавно. Несмотря на то, что серная кислота давно известна, вначале ее получали сухой перегонкой, поэтому упоминается под названием "купоросное масло", в промышленных количествах она стала производиться относительно недавно.

Сырьём для ее получения служат элементарная сера, сульфиды и сульфаты металлов, сероводород, отходящие газы теплоэлектростанций, использующих неочищенную нефть, и др. Основным сырьём является пирит. Сырьём для ее получения служат элементарная сера, сульфиды и сульфаты металлов, сероводород, отходящие газы теплоэлектростанций, использующих неочищенную нефть, и др. Основным сырьём является пирит.

Сжигание или обжиг сырья в кислороде с получением SO2 Сжигание или обжиг сырья в кислороде с получением SO2 Очистка от примесей газа Окисление SО2 в SO3 Абсорбция SO3 водой.

C XIV века серную кислоту получали "камерным" методом, в основе которой лежала реакция горения на воздухе смеси серы и калийной селитры, описанная алхимиком Валентином. Процесс проводился в камерах, обитых свинцом, нерастворимым в серной кислоте. Продуктами горения являлись оксиды азота, соли калия и SO3. Последний поглощался водой, находящейся в камере. Таким способом удавалось получить кислоту небольшой крепости, которую концентрировали известными методами. C XIV века серную кислоту получали "камерным" методом, в основе которой лежала реакция горения на воздухе смеси серы и калийной селитры, описанная алхимиком Валентином. Процесс проводился в камерах, обитых свинцом, нерастворимым в серной кислоте. Продуктами горения являлись оксиды азота, соли калия и SO3. Последний поглощался водой, находящейся в камере. Таким способом удавалось получить кислоту небольшой крепости, которую концентрировали известными методами.

В зависимости от соотношения реагентов получался разный состав твердого остатка. Одна из схем получения камерной серной кислоты, наиболее полно расходующая нитрат калия: В зависимости от соотношения реагентов получался разный состав твердого остатка. Одна из схем получения камерной серной кислоты, наиболее полно расходующая нитрат калия: 2KNO3 + 2S + 2O2 → K2SO4 + SO3 + NO2 + NO SO3 + H2O → H2SO4