Презентация на тему: Простейшие гальванические элементы.

Тема урока: Простейшие гальванические элементы.

Цель урока: 1.Обучающая: изучить устройство и принцип работы гальванического элемента. Научиться собирать электрическую цепь с гальваническим элементом. 2.Развивающая: развить электротехнические навыки в сборке электрических цепей. 3. Воспитывающая: воспитать аккуратность, целеустремленность, достижение цели.

Вопросы по пройденной теме: 1.Какие вы знаете источники электрической энергии? 2.Чем отличается проводники электрического тока от изоляторов? 3.Что называется электрической цепью? 4. Из каких элементов состоит электрическая схема карманного фонарика?

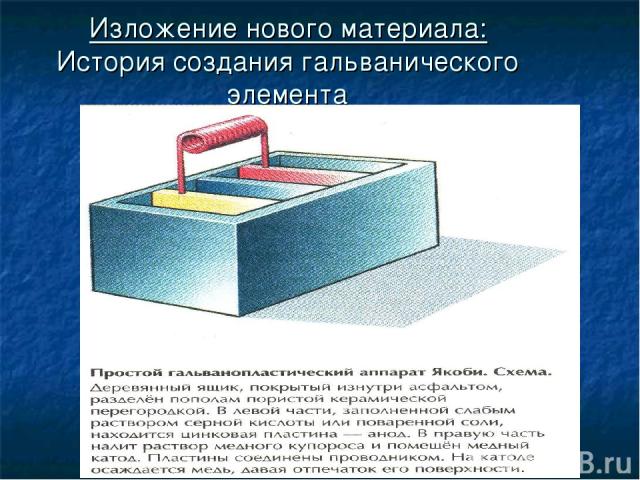
Изложение нового материала: История создания гальванического элемента
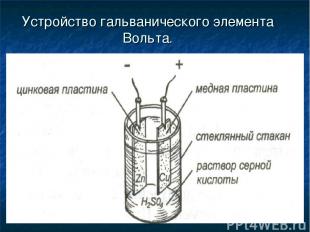
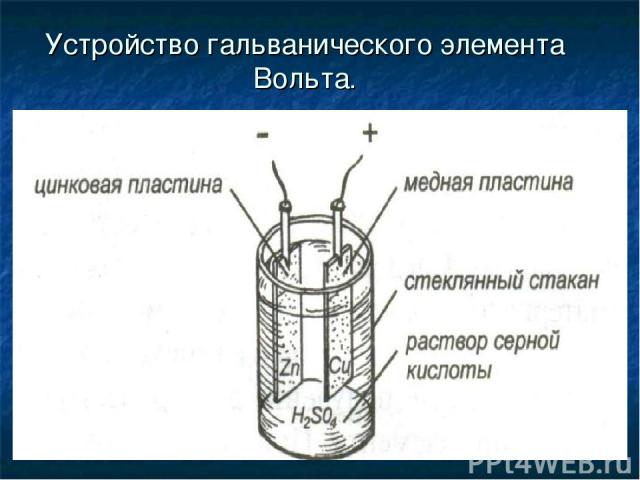
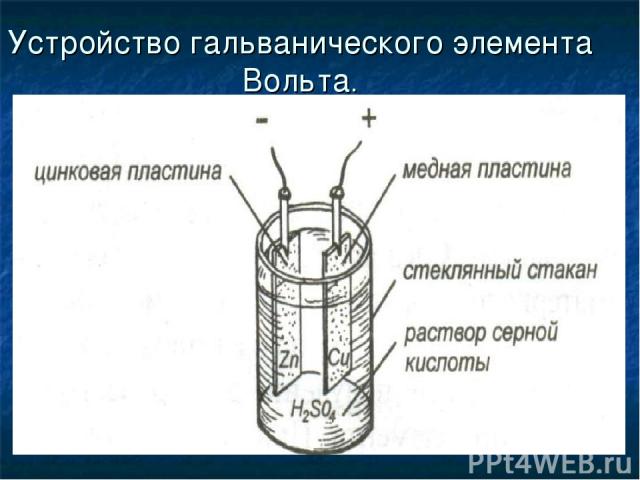
Устройство гальванического элемента Вольта.
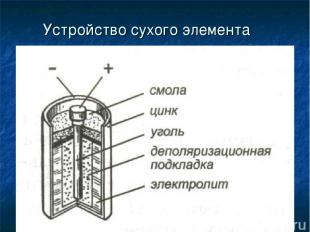
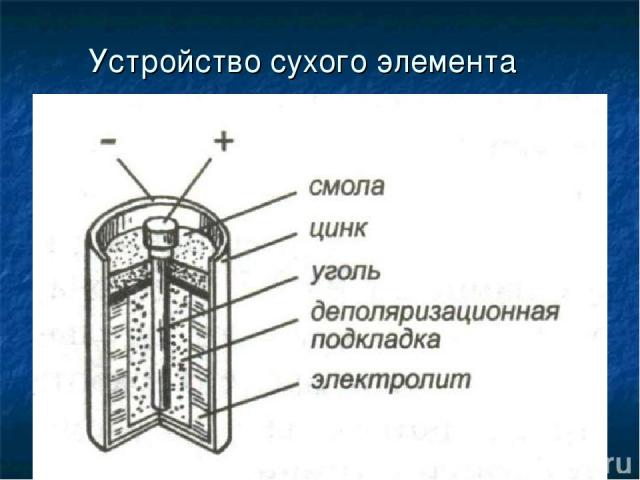
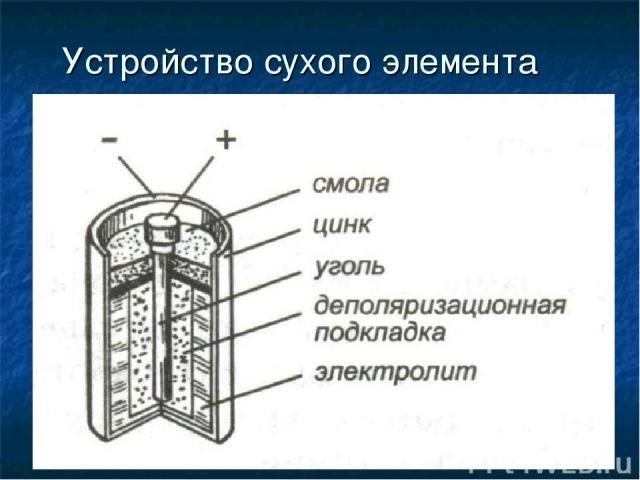
Устройство сухого элемента
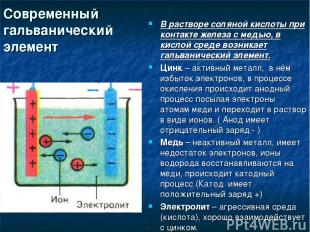
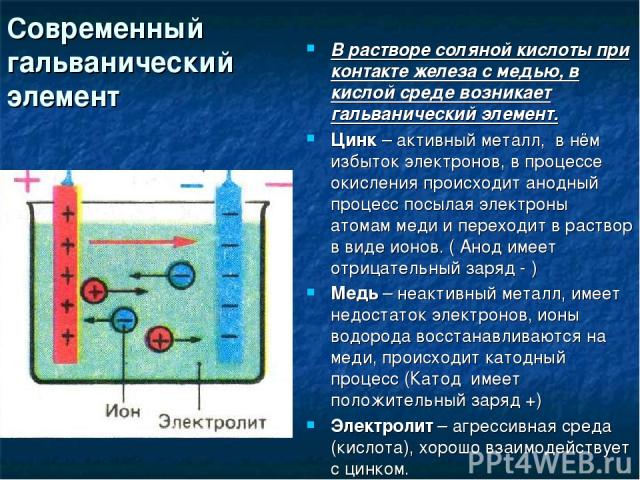
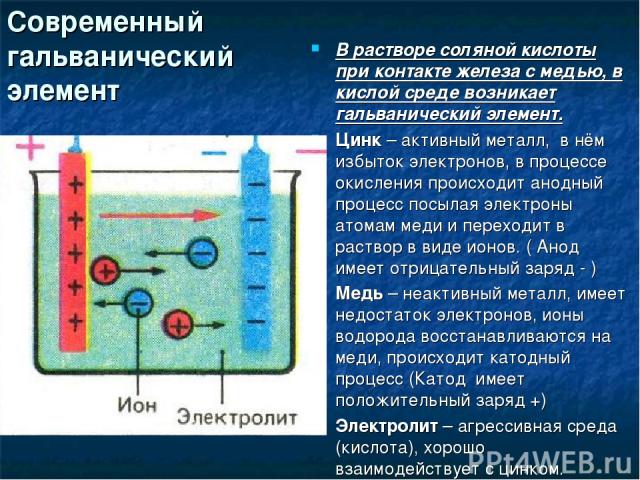
Современный гальванический элемент В растворе соляной кислоты при контакте железа с медью, в кислой среде возникает гальванический элемент. Цинк – активный металл, в нём избыток электронов, в процессе окисления происходит анодный процесс посылая электроны атомам меди и переходит в раствор в виде ионов. ( Анод имеет отрицательный заряд - ) Медь – неактивный металл, имеет недостаток электронов, ионы водорода восстанавливаются на меди, происходит катодный процесс (Катод имеет положительный заряд +) Электролит – агрессивная среда (кислота), хорошо взаимодействует с цинком.
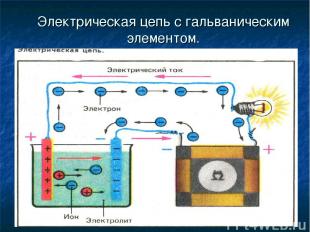
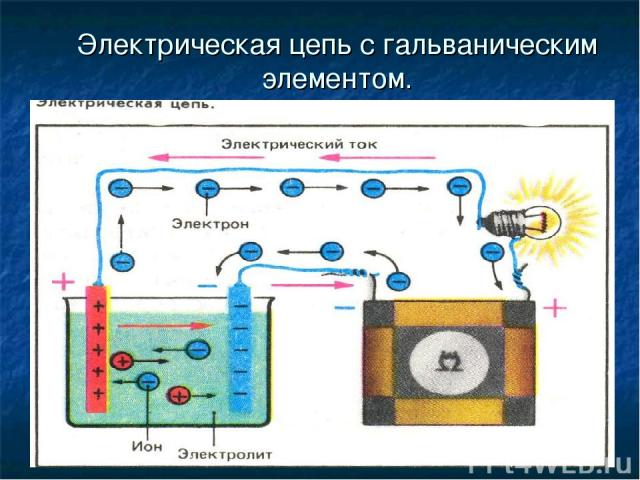
Электрическая цепь с гальваническим элементом.

Батарея сухих элементов. Схема подключения.

ЭКОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ. УТИЛИЗАЦИИ ГАЛЬВАНИЧЕСКИХ ЭЛЕМЕНТОВ 1. Нельзя выбрасывать и загрязнять: землю, воду, лес, бросать в огонь. 2. Нельзя вскрывать элемент в своей квартире. 3. Утилизировать гальванические элементы только в контейнеры для бытового мусора. 4. После утилизации, тщательно вымыть руки с мылом.

САМОСТОЯТЕЛЬНАЯ РАБОТА УЧАЩИХСЯ 1.Знакомство с устройством гальванического элемента Вольта. 2.Выполнение схемы устройства гальванического элемента Вольта и сухого элемента. 3.Записать устройство гальванического элемента.
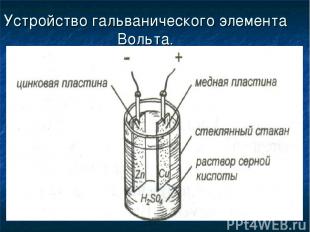
Устройство гальванического элемента Вольта.
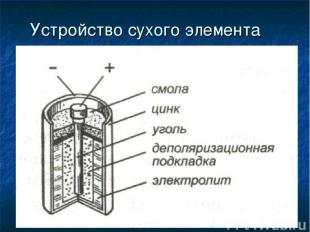
Устройство сухого элемента
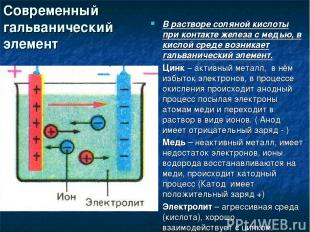
Современный гальванический элемент В растворе соляной кислоты при контакте железа с медью, в кислой среде возникает гальванический элемент. Цинк – активный металл, в нём избыток электронов, в процессе окисления происходит анодный процесс посылая электроны атомам меди и переходит в раствор в виде ионов. ( Анод имеет отрицательный заряд - ) Медь – неактивный металл, имеет недостаток электронов, ионы водорода восстанавливаются на меди, происходит катодный процесс (Катод имеет положительный заряд +) Электролит – агрессивная среда (кислота), хорошо взаимодействует с цинком.

Заключительная часть урока Закрепление пройденного урока: 1. Из каких основных элементов состоит гальванический элемент? 2. Какие виды гальванических элементов вы знаете? 3. Покажите на электрической схеме, условное изображение гальванического элемента? 4. Как правильно утилизировать гальванический элемент?
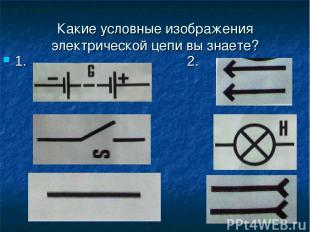
Какие условные изображения электрической цепи вы знаете? 1. 2.
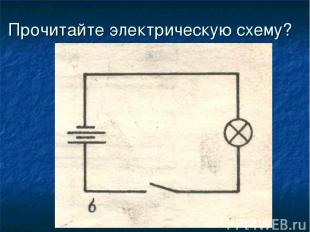
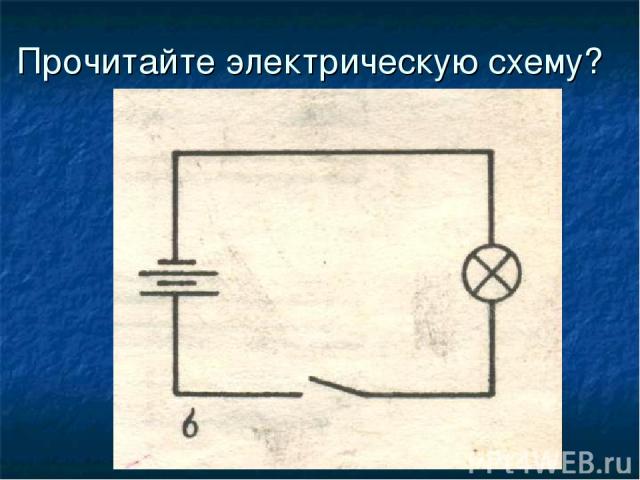
Прочитайте электрическую схему?

Домашнее задание: Найдите в интернете материал о новых видах переносных автономных источниках электрической энергии.