Презентация на тему: Металлоорганические соединения непереходных металлов

Металлоорганические соединения непереходных металлов *

Лекция 2 Характерные типы и энергетика связей металл-углерод Основные синтетические подходы к металлоорганическим соединениям *
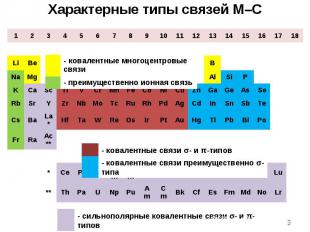
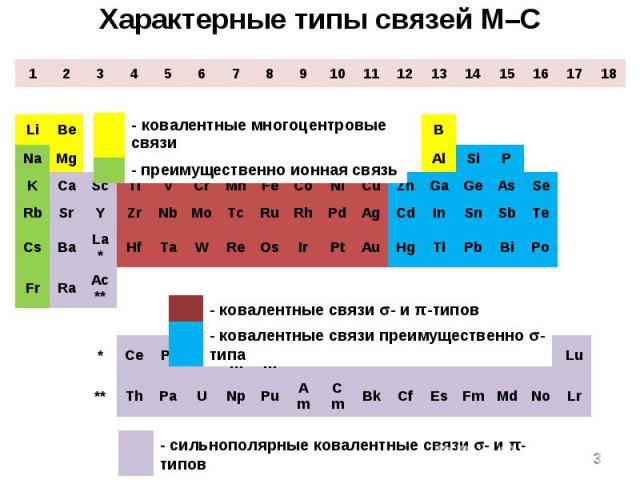
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Cs Ba La* Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Fr Ra Ac** * Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu ** Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Характерные типы связей M–C - ковалентные многоцентровые связи - преимущественно ионная связь - ковалентные связи - и π-типов - ковалентные связи преимущественно - типа - сильнополярные ковалентные связи - и π-типов *
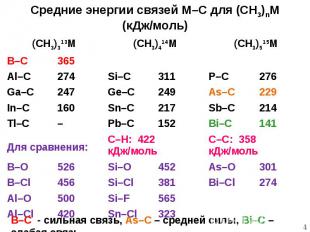
Средние энергии связей M–C для (CH3)nM (кДж/моль) (CH3)313M (CH3)414M (CH3)515M B–C 365 Al–C 274 Si–C 311 P–C 276 Ga–C 247 Ge–C 249 As–C 229 In–C 160 Sn–C 217 Sb–C 214 Tl–C – Pb–C 152 Bi–C 141 Для сравнения: C–H: 422 кДж/моль C–C: 358 кДж/моль B–O 526 Si–O 452 As–O 301 B–Cl 456 Si–Cl 381 Bi–Cl 274 Al–O 500 Si–F 565 Al–Cl 420 Sn–Cl 323 B–C - сильная связь, As–C – средней силы, Bi–C – слабая связь *

Условность величины средней энергии связи!!! (CH3)2Hg CH3Hg + CH3 D1(Hg – C) = 214 кДж/моль (CH3)Hg Hg + CH3 D2(Hg – C) = 29 кДж/моль Среднее значение – Dср(Hg – C) = 121.5 кДж/моль!!! *
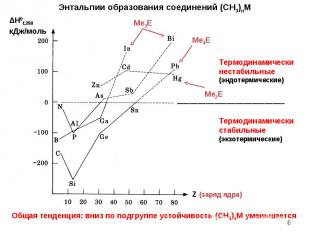
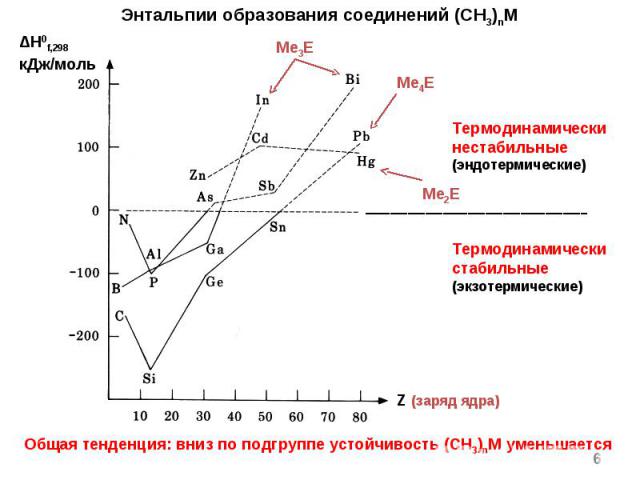
* Энтальпии образования соединений (CH3)nM Общая тенденция: вниз по подгруппе устойчивость (CH3)nM уменьшается ΔH0f,298 кДж/моль Me3E Z (заряд ядра) Me4E Me2E Термодинамически нестабильные (эндотермические) Термодинамически стабильные (экзотермические)

* Отношение металлоорганических соединений к воздуху и воде: термодинамическая устойчивость и кинетическая инертность Соединение Теплота сгорания Термодинамич. устойчивость Кинетич. инертность Устойчивость на воздухе Устойчивость к гидролизу ZnEt2 – 1920 Нестабилен Лабилен Пирофорен Легко гидролизуется SnMe4 – 3590 Нестабилен Инертен Устойчив Инертен

Обзор методов синтеза металлоорганических соединений (для металлов главных подгрупп) *

* Основа подхода – окисление металла галогенуглеводородами 2M + nRX RnM + MXn M0 – ne– Mn+ R1+ + 2e– R– Окислительное присоединение (подход [1])
![Подход [1], примеры * Метод [1a] - «прямой синтез» - металл + галогенуглеводород Подход [1], примеры * Метод [1a] - «прямой синтез» - металл + галогенуглеводород](https://fs1.ppt4web.ru/images/3018/55248/310/img9.jpg)
Подход [1], примеры * Метод [1a] - «прямой синтез» - металл + галогенуглеводород 2Li + C4H9Br C4H9Li + LiBr Mg + C6H5Br C6H5MgBr Реакции экзотермичны в случае наиболее электроположитель-ных металлов, образующих ионные и сильные ковалентные связи М–С. Метод неприемлем в случае металлов, образующих слабые связи М–С (Tl, Pb, Bi, Hg). Растворители: простые эфиры, циклические эфиры, алканы
![* Метод [1б] - «смешаннометаллический» - смесь металла-восстановителя + металл, * Метод [1б] - «смешаннометаллический» - смесь металла-восстановителя + металл,](https://fs1.ppt4web.ru/images/3018/55248/310/img10.jpg)
* Метод [1б] - «смешаннометаллический» - смесь металла-восстановителя + металл, соединение которого вы хотите получить: 2Na + Hg + 2CH3Br (CH3)2Hg + 2NaBr H0298 = – 530 кДж/моль H0f,298 (NaBr) = – 361 кДж/моль Удобен, если есть возможность использовать сплавы 4Na/Pb + 4C2H5Cl (C2H5)4Pb +3Pb + 4NaCl Подход [1], примеры
![* Метод [1в] – окисление металлов в промежуточной степени окисления: PbI2 + CH3I * Метод [1в] – окисление металлов в промежуточной степени окисления: PbI2 + CH3I](https://fs1.ppt4web.ru/images/3018/55248/310/img11.jpg)
* Метод [1в] – окисление металлов в промежуточной степени окисления: PbI2 + CH3I (CH3)PbI3 Подход [1], примеры Pb2+ – 2e– Pb4+ (CH3)+ + 2e– (CH3) –
![* Трансметаллирование (подход [2]) Основа подхода – восстановление металлооргани * Трансметаллирование (подход [2]) Основа подхода – восстановление металлооргани](https://fs1.ppt4web.ru/images/3018/55248/310/img12.jpg)
* Трансметаллирование (подход [2]) Основа подхода – восстановление металлоорганического соединения менее электроположительного металла более электроположительным M + RM’ RM + M’ Пример: Zn + (CH3)2Hg (CH3)2Zn + Hg H0298 = – 35 кДж/моль Метод [2] применим для 1M; 2M; 3M; 13M = Al, Ga; 14M = Sn, Pb; 15M = Bi; 16M = Se, Te; 15M = Bi; 12M = Zn, Cd.
![* Обмен металлов (подход [3]) Основа подхода – вывод одного из продуктов в другу * Обмен металлов (подход [3]) Основа подхода – вывод одного из продуктов в другу](https://fs1.ppt4web.ru/images/3018/55248/310/img13.jpg)
* Обмен металлов (подход [3]) Основа подхода – вывод одного из продуктов в другую фазу (чаще, в осадок) RM + R’M’ R’M + RM’ Пример: 4PhLi + (CH2=CH)4Sn 4(CH2=CH)Li + Ph4Sn (в не- или малополярных апротонных растворителях)
![* Метатезис (подход [4]) (нуклеофильное замещение галогена на R) Движущая сила – * Метатезис (подход [4]) (нуклеофильное замещение галогена на R) Движущая сила –](https://fs1.ppt4web.ru/images/3018/55248/310/img14.jpg)
* Метатезис (подход [4]) (нуклеофильное замещение галогена на R) Движущая сила – образование галогенида электроположительного металла nRM + M’Xn RnM’ + nMX Пример: 3(CH3)Li + SbCl3 (CH3)3Sb + 3LiCl Один из наиболее распространенных подходов! Имеется возможность «играть» на нерастворимости галогенида металла. Есть «подводные камни»: R - сильные восстановители

* Замещение галогена на металл в реакции арилгалогенидов с алкиллитием (подход [5]) RLi + ArX RX + ArLi Пример: n-BuLi + PhX n-BuX + PhLi (X = Br, I очень редко Cl, но не F!) Реакция замещения галогена на литий очень быстрая, поэтому метод может быть использован для замещенных арилов (NO2, CONR2, COOR, SiCl3), поскольку протекает при низкой температуре! Механизм до конца не ясен. Подозревается, что он радикальный.
![* Металлирование C–H кислот (подход [6]) Пример: Кислотно-основное равновесие. О * Металлирование C–H кислот (подход [6]) Пример: Кислотно-основное равновесие. О](https://fs1.ppt4web.ru/images/3018/55248/310/img16.jpg)
* Металлирование C–H кислот (подход [6]) Пример: Кислотно-основное равновесие. Образуется «соль» более сильной кислоты. 2
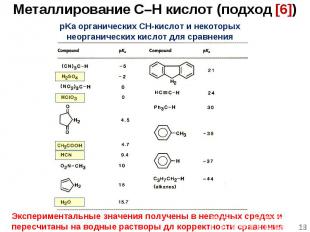
* pKa органических CH-кислот и некоторых неорганических кислот для сравнения Экспериментальные значения получены в неводных средах и пересчитаны на водные растворы дл корректности сравнения Металлирование C–H кислот (подход [6])

* Ацетилены и циклопентадиен являются довольно сильными кислотами. Для них возможно «прямое» металлирование: Циклопентадиен можно депротонировать твердым MOH (M = Na, K) в ТГФ: C5H6(р-р) + NaOH(тв., изб.) (C5H5)M(р-р) + (H2O/NaOH)(тв.) Введение в него алкильных заместителей понижает кислотность. Для полиметильных и полиарильных замещенных используют NaH, NaNH2, RLi. Металлирование C–H кислот (подход [6])
![* Металлирование C–H кислот (подход [6]) Возможные проблемы: в некоторых случаях * Металлирование C–H кислот (подход [6]) Возможные проблемы: в некоторых случаях](https://fs1.ppt4web.ru/images/3018/55248/310/img19.jpg)
* Металлирование C–H кислот (подход [6]) Возможные проблемы: в некоторых случаях депротонирование в органических средах чрезвычайно заторможено! Реакция выгодна термодинамически, но чрезвычайно медленная. Добавлением TMEDA или t-BuO- удается увеличить скорость до разумной:
![* Меркурирование C–H кислот (подход [7]) (особый случай металлирования!) Первая * Меркурирование C–H кислот (подход [7]) (особый случай металлирования!) Первая](https://fs1.ppt4web.ru/images/3018/55248/310/img20.jpg)
* Меркурирование C–H кислот (подход [7]) (особый случай металлирования!) Первая стадия – легко, вторая требует более жестких условий. Пример: Реакция протекает в протонных средах, не требует тщательной защиты от воздуха и влаги, а ртуть позже может быть «трансметаллирована»!
![* Гидрометаллирование (подход [8]) Пример: Способность к присоединению увеличива * Гидрометаллирование (подход [8]) Пример: Способность к присоединению увеличива](https://fs1.ppt4web.ru/images/3018/55248/310/img21.jpg)
* Гидрометаллирование (подход [8]) Пример: Способность к присоединению увеличивается в ряду:
![* Карбометаллирование (подход [9]) Аналогично гидрометаллированию, но с присоеди * Карбометаллирование (подход [9]) Аналогично гидрометаллированию, но с присоеди](https://fs1.ppt4web.ru/images/3018/55248/310/img22.jpg)
* Карбометаллирование (подход [9]) Аналогично гидрометаллированию, но с присоединением углеводородного радикала. Пример: Только для щелочных металлов и алюминия!
![* Внедрение карбенов (подход [10]) Примеры: Обычно карбены внедряются по связи M * Внедрение карбенов (подход [10]) Примеры: Обычно карбены внедряются по связи M](https://fs1.ppt4web.ru/images/3018/55248/310/img23.jpg)
* Внедрение карбенов (подход [10]) Примеры: Обычно карбены внедряются по связи M–H и M–X, внедрение по связи M–C не происходит!
![* Декарбоксилирование (подход [11]) Примеры: Важно!!! Радикалы R должны быть сил * Декарбоксилирование (подход [11]) Примеры: Важно!!! Радикалы R должны быть сил](https://fs1.ppt4web.ru/images/3018/55248/310/img24.jpg)
* Декарбоксилирование (подход [11]) Примеры: Важно!!! Радикалы R должны быть сильноакцепторными: C6F5, CF3, CCl3, и т.п. Металлоорганические гидриды могут быть получены разложением соответствующих формиатов:
![* Арилирование через соли диазония (подход [12]) Примеры: Применение метода очен * Арилирование через соли диазония (подход [12]) Примеры: Применение метода очен](https://fs1.ppt4web.ru/images/3018/55248/310/img25.jpg)
* Арилирование через соли диазония (подход [12]) Примеры: Применение метода очень ограничены. Особое значение имеет, пожалуй, только для мышьякорганики.







![* Основа подхода – окисление металла галогенуглеводородами 2M + nRX RnM + MXn M0 – ne– Mn+ R1+ + 2e– R– Окислительное присоединение (подход [1]) * Основа подхода – окисление металла галогенуглеводородами 2M + nRX RnM + MXn M0 – ne– Mn+ R1+ + 2e– R– Окислительное присоединение (подход [1])](https://fs1.ppt4web.ru/images/3018/55248/640/img8.jpg)
![Подход [1], примеры * Метод [1a] - «прямой синтез» - металл + галогенуглеводород 2Li + C4H9Br C4H9Li + LiBr Mg + C6H5Br C6H5MgBr Реакции экзотермичны в случае наиболее электроположитель-ных металлов, образующих ионные и сильные ковалентные связи М–С… Подход [1], примеры * Метод [1a] - «прямой синтез» - металл + галогенуглеводород 2Li + C4H9Br C4H9Li + LiBr Mg + C6H5Br C6H5MgBr Реакции экзотермичны в случае наиболее электроположитель-ных металлов, образующих ионные и сильные ковалентные связи М–С…](https://fs1.ppt4web.ru/images/3018/55248/640/img9.jpg)
![* Метод [1б] - «смешаннометаллический» - смесь металла-восстановителя + металл, соединение которого вы хотите получить: 2Na + Hg + 2CH3Br (CH3)2Hg + 2NaBr H0298 = – 530 кДж/моль H0f,298 (NaBr) = – 361 кДж/моль Удобен, если есть возможность использов… * Метод [1б] - «смешаннометаллический» - смесь металла-восстановителя + металл, соединение которого вы хотите получить: 2Na + Hg + 2CH3Br (CH3)2Hg + 2NaBr H0298 = – 530 кДж/моль H0f,298 (NaBr) = – 361 кДж/моль Удобен, если есть возможность использов…](https://fs1.ppt4web.ru/images/3018/55248/640/img10.jpg)
![* Метод [1в] – окисление металлов в промежуточной степени окисления: PbI2 + CH3I (CH3)PbI3 Подход [1], примеры Pb2+ – 2e– Pb4+ (CH3)+ + 2e– (CH3) – * Метод [1в] – окисление металлов в промежуточной степени окисления: PbI2 + CH3I (CH3)PbI3 Подход [1], примеры Pb2+ – 2e– Pb4+ (CH3)+ + 2e– (CH3) –](https://fs1.ppt4web.ru/images/3018/55248/640/img11.jpg)
![* Трансметаллирование (подход [2]) Основа подхода – восстановление металлоорганического соединения менее электроположительного металла более электроположительным M + RM’ RM + M’ Пример: Zn + (CH3)2Hg (CH3)2Zn + Hg H0298 = – 35 кДж/моль Метод [2] при… * Трансметаллирование (подход [2]) Основа подхода – восстановление металлоорганического соединения менее электроположительного металла более электроположительным M + RM’ RM + M’ Пример: Zn + (CH3)2Hg (CH3)2Zn + Hg H0298 = – 35 кДж/моль Метод [2] при…](https://fs1.ppt4web.ru/images/3018/55248/640/img12.jpg)
![* Обмен металлов (подход [3]) Основа подхода – вывод одного из продуктов в другую фазу (чаще, в осадок) RM + R’M’ R’M + RM’ Пример: 4PhLi + (CH2=CH)4Sn 4(CH2=CH)Li + Ph4Sn (в не- или малополярных апротонных растворителях) * Обмен металлов (подход [3]) Основа подхода – вывод одного из продуктов в другую фазу (чаще, в осадок) RM + R’M’ R’M + RM’ Пример: 4PhLi + (CH2=CH)4Sn 4(CH2=CH)Li + Ph4Sn (в не- или малополярных апротонных растворителях)](https://fs1.ppt4web.ru/images/3018/55248/640/img13.jpg)
![* Метатезис (подход [4]) (нуклеофильное замещение галогена на R) Движущая сила – образование галогенида электроположительного металла nRM + M’Xn RnM’ + nMX Пример: 3(CH3)Li + SbCl3 (CH3)3Sb + 3LiCl Один из наиболее распространенных подходов! Имеется… * Метатезис (подход [4]) (нуклеофильное замещение галогена на R) Движущая сила – образование галогенида электроположительного металла nRM + M’Xn RnM’ + nMX Пример: 3(CH3)Li + SbCl3 (CH3)3Sb + 3LiCl Один из наиболее распространенных подходов! Имеется…](https://fs1.ppt4web.ru/images/3018/55248/640/img14.jpg)
![* Замещение галогена на металл в реакции арилгалогенидов с алкиллитием (подход [5]) RLi + ArX RX + ArLi Пример: n-BuLi + PhX n-BuX + PhLi (X = Br, I очень редко Cl, но не F!) Реакция замещения галогена на литий очень быстрая, поэтому метод может быт… * Замещение галогена на металл в реакции арилгалогенидов с алкиллитием (подход [5]) RLi + ArX RX + ArLi Пример: n-BuLi + PhX n-BuX + PhLi (X = Br, I очень редко Cl, но не F!) Реакция замещения галогена на литий очень быстрая, поэтому метод может быт…](https://fs1.ppt4web.ru/images/3018/55248/640/img15.jpg)
![* Металлирование C–H кислот (подход [6]) Пример: Кислотно-основное равновесие. Образуется «соль» более сильной кислоты. 2 * Металлирование C–H кислот (подход [6]) Пример: Кислотно-основное равновесие. Образуется «соль» более сильной кислоты. 2](https://fs1.ppt4web.ru/images/3018/55248/640/img16.jpg)
![* pKa органических CH-кислот и некоторых неорганических кислот для сравнения Экспериментальные значения получены в неводных средах и пересчитаны на водные растворы дл корректности сравнения Металлирование C–H кислот (подход [6]) * pKa органических CH-кислот и некоторых неорганических кислот для сравнения Экспериментальные значения получены в неводных средах и пересчитаны на водные растворы дл корректности сравнения Металлирование C–H кислот (подход [6])](https://fs1.ppt4web.ru/images/3018/55248/640/img17.jpg)

![* Металлирование C–H кислот (подход [6]) Возможные проблемы: в некоторых случаях депротонирование в органических средах чрезвычайно заторможено! Реакция выгодна термодинамически, но чрезвычайно медленная. Добавлением TMEDA или t-BuO- удается увеличи… * Металлирование C–H кислот (подход [6]) Возможные проблемы: в некоторых случаях депротонирование в органических средах чрезвычайно заторможено! Реакция выгодна термодинамически, но чрезвычайно медленная. Добавлением TMEDA или t-BuO- удается увеличи…](https://fs1.ppt4web.ru/images/3018/55248/640/img19.jpg)
![* Меркурирование C–H кислот (подход [7]) (особый случай металлирования!) Первая стадия – легко, вторая требует более жестких условий. Пример: Реакция протекает в протонных средах, не требует тщательной защиты от воздуха и влаги, а ртуть позже может … * Меркурирование C–H кислот (подход [7]) (особый случай металлирования!) Первая стадия – легко, вторая требует более жестких условий. Пример: Реакция протекает в протонных средах, не требует тщательной защиты от воздуха и влаги, а ртуть позже может …](https://fs1.ppt4web.ru/images/3018/55248/640/img20.jpg)
![* Гидрометаллирование (подход [8]) Пример: Способность к присоединению увеличивается в ряду: * Гидрометаллирование (подход [8]) Пример: Способность к присоединению увеличивается в ряду:](https://fs1.ppt4web.ru/images/3018/55248/640/img21.jpg)
![* Карбометаллирование (подход [9]) Аналогично гидрометаллированию, но с присоединением углеводородного радикала. Пример: Только для щелочных металлов и алюминия! * Карбометаллирование (подход [9]) Аналогично гидрометаллированию, но с присоединением углеводородного радикала. Пример: Только для щелочных металлов и алюминия!](https://fs1.ppt4web.ru/images/3018/55248/640/img22.jpg)
![* Внедрение карбенов (подход [10]) Примеры: Обычно карбены внедряются по связи M–H и M–X, внедрение по связи M–C не происходит! * Внедрение карбенов (подход [10]) Примеры: Обычно карбены внедряются по связи M–H и M–X, внедрение по связи M–C не происходит!](https://fs1.ppt4web.ru/images/3018/55248/640/img23.jpg)
![* Декарбоксилирование (подход [11]) Примеры: Важно!!! Радикалы R должны быть сильноакцепторными: C6F5, CF3, CCl3, и т.п. Металлоорганические гидриды могут быть получены разложением соответствующих формиатов: * Декарбоксилирование (подход [11]) Примеры: Важно!!! Радикалы R должны быть сильноакцепторными: C6F5, CF3, CCl3, и т.п. Металлоорганические гидриды могут быть получены разложением соответствующих формиатов:](https://fs1.ppt4web.ru/images/3018/55248/640/img24.jpg)
![* Арилирование через соли диазония (подход [12]) Примеры: Применение метода очень ограничены. Особое значение имеет, пожалуй, только для мышьякорганики. * Арилирование через соли диазония (подход [12]) Примеры: Применение метода очень ограничены. Особое значение имеет, пожалуй, только для мышьякорганики.](https://fs1.ppt4web.ru/images/3018/55248/640/img25.jpg)











