Презентация на тему: Кристаллические решётки химия

Строение вещества Презентация к уроку химии по теме «Кристаллические решетки» Бербенцева София Николаевна, учитель химии МОУ СОШ № 3 п.Солнечный Хабаровского края 900igr.net

Вещество – то, из чего состоит физическое тело.
Состояние вещества Твердое Жидкое Газообразное

Состояние вещества Твердое Жидкое Газообразное Стекло Железо Соль

Твердое вещество Аморфное Кристаллическое нет определенной tпл определенная tпл смола хлорид натрия стекло графит пластилин металлы

Кристаллические решётки веществ-это упорядоченное расположение частиц (атомов, молекул, ионов) в строго определённых точках пространства. Точки размещения частиц называют узлами кристаллической решётки.

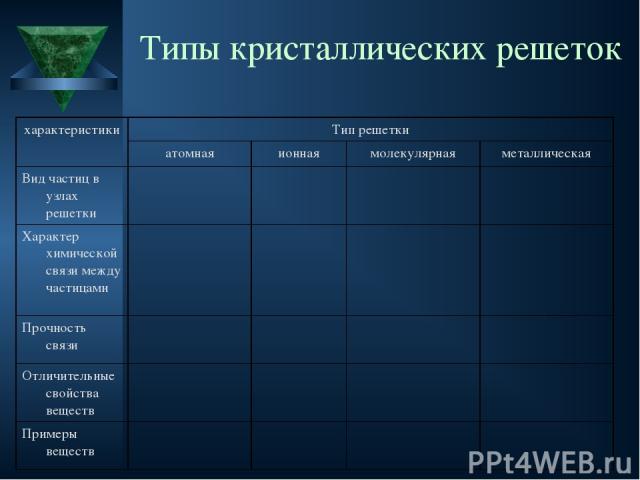
Типы кристаллических решеток характеристики Тип решетки атомная ионная молекулярная металлическая Вид частиц в узлах решетки Характер химической связи между частицами Прочность связи Отличительные свойства веществ Примеры веществ

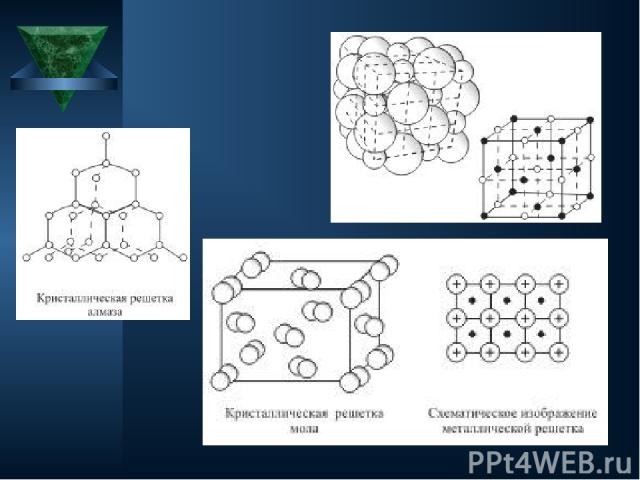
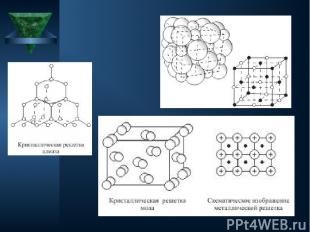
ИОННЫЕ Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Рассмотрим строение кристалла поваренной соли, в узлах которого находятся ионы хлора и натрия. Связи между ионами в кристалле очень прочные и устойчивые. Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.

Атомные Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, которые соединены очень прочными ковалентными связями. Выше показана кристаллическая решётка алмаза. В природе встречается немного веществ с атомной кристаллической решёткой. К ним относятся бор, кремний, германий, кварц, алмаз. Вещества с АКР имеют высокие температуры плавления, обладают повышенной твёрдостью. Алмаз - самый твёрдый природный материал.

Молекулярные Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные. Выше представлена кристаллическая решётка I2 Вещества с МКР имеют малую твёрдость, плавятся при низкой температуре, летучие, при обычных условиях находятся в газообразном или жидком состоянии

Металлические Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. Для металлов характерны физические свойства: пластичность, ковкость, металлический блеск, высокая электро- и теплопроводность

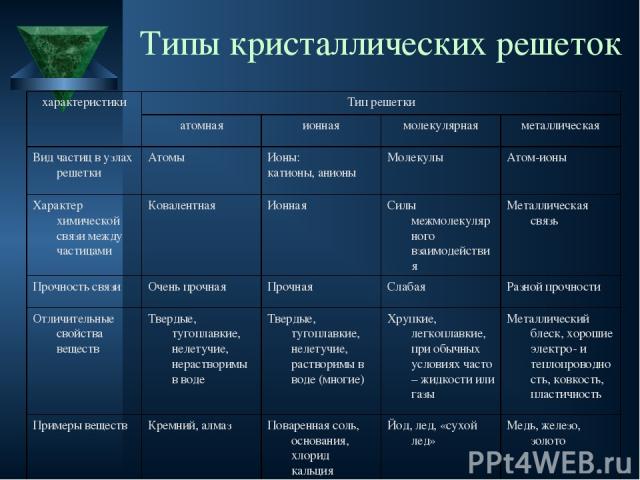
Типы кристаллических решеток характеристики Тип решетки атомная ионная молекулярная металлическая Вид частиц в узлах решетки Атомы Ионы: катионы, анионы Молекулы Атом-ионы Характер химической связи между частицами Ковалентная Ионная Силы межмолекулярного взаимодействия Металлическая связь Прочность связи Очень прочная Прочная Слабая Разной прочности Отличительные свойства веществ Твердые, тугоплавкие, нелетучие, нерастворимы в воде Твердые, тугоплавкие, нелетучие, растворимы в воде (многие) Хрупкие, легкоплавкие, при обычных условиях часто – жидкости или газы Металлический блеск, хорошие электро- и теплопроводность, ковкость, пластичность Примеры веществ Кремний, алмаз Поваренная соль, основания, хлорид кальция Йод, лед, «сухой лед» Медь, железо, золото

Закон постоянства состава Жозеф Луи Пруст. 1808 г. родился 26 сентября 1754 г. в небольшом городке Анжере в семье аптекаря 1775 г. он был назначен на должность управляющего аптекой больницы Сальпетриер 1777 г. Пруст получил приглашение на кафедру химии и металлургии недавно основанной Королевской семинарии в Вергаре (Испания) 1785 г. король Испании Карл III пригласил Пруста на должность профессора химии Артиллерийской школы в Сеговии В дальнейшем Пруст руководил кафедрами химии в университете Саламанки (1789), а затем Мадрида (1791–1808).

Закон постоянства состава Жозеф Луи Пруст. 1808 г. «Молекулярные химические соединения независимо от способа их получения имеют постоянный состав и свойства»

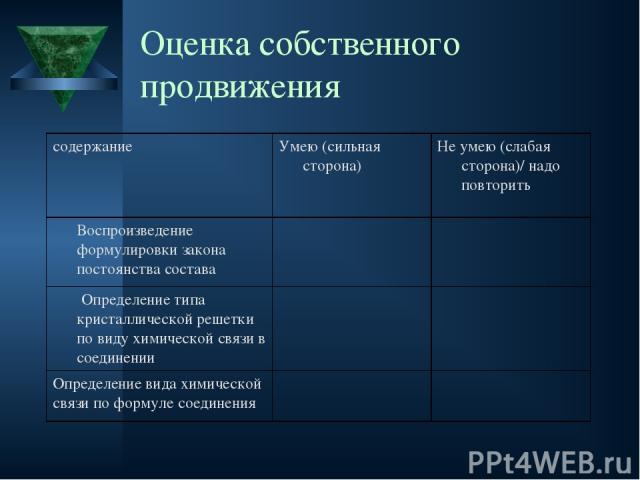
Оценка собственного продвижения содержание Умею (сильная сторона) Не умею (слабая сторона)/ надо повторить Воспроизведение формулировки закона постоянства состава Определение типа кристаллической решетки по виду химической связи в соединении Определение вида химической связи по формуле соединения

Домашнее задание § 22, выполни задания 1, 6 после параграфа; обрати особое внимание на слабые стороны, выделенные тобой при рефлексии