Презентация на тему: Ковалентная связь

Ковалентная связь

Атомы благородных газов имеют завершённый внешний энергетический уровень. Он наиболее устойчив и стабилен, что является причиной инертности атомов благородных газов. Атомы других элементов пытаются приобрести конфигурацию ближайшего благородного газа и перейти в наиболее устойчивое состояние. Такое состояние атомы приобретают, взаимодействуя между собой, в результате между ними возникает химическая связь.

Химическая связь – это силы взаимодействия, которые соединяют отдельные атомы в молекулы, ионы, кристаллы.

Валентность – это способность атома элемента образовывать различное число химических связей с другими атомами. Величина валентности элемента определяется числом химических связей, которые атом элемента образует с другими атомами.

В образовании химической связи участвуют только валентные электроны. У элементов главных подгрупп это электроны внешнего энергетического уровня. Они расположены дальше от ядра и менее прочно связаны с ним. В зависимости от способа образования завершённых электронных структур атомов различают несколько видов химической связи.
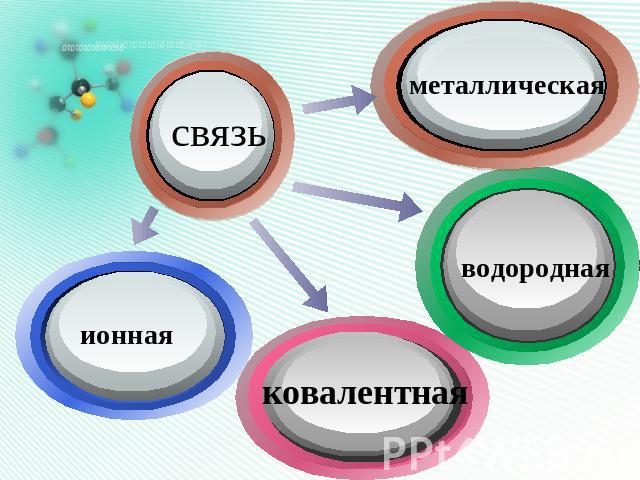
связь ионная ковалентная водородная металлическая

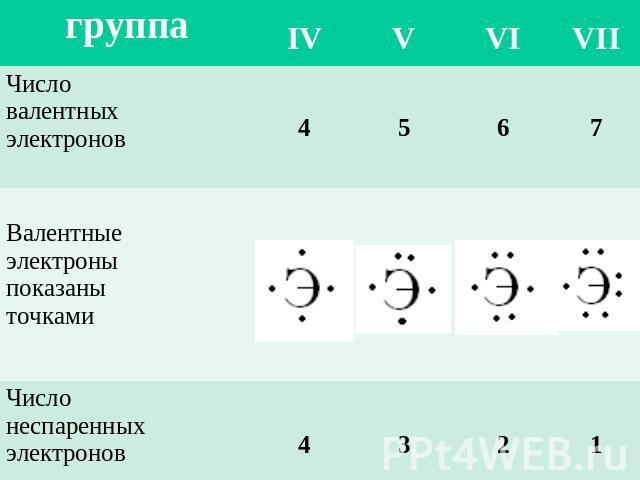
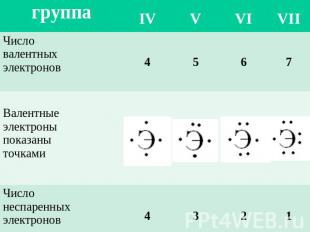
В образовании ковалентной связи принимают участие неспаренные валентные электроны атома, которые располагаются на внешнем уровне по одному. Число неспаренных электронов = 8 – номер группы элемента Например, у серы число неспаренных электронов равно 8 – 6 = 2.

Ковалентная связь – это химическая связь между атомами, осуществляемая при помощи общих электронных пар.

Механизм образования ковалентной связи Неспаренные Общая или поделённая пара электронов Между ядрами образуется сгущение отрицательного заряда, который притягивает к себе ядра атомов.

Образование ковалентной связи в молекуле хлора (Cl2). Для завершения внешнего слоя каждому атому не хватает по 1е-.За счёт образования ковалентной связи каждый атом в молекуле приобретает завершённый внешний слой.
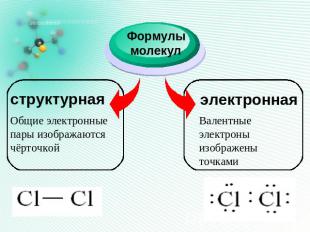
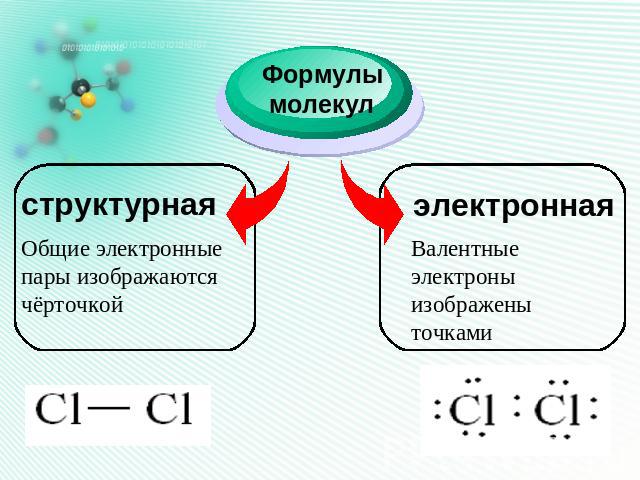
Формулы молекул структурная Общие электронные пары изображаются чёрточкой электронная Валентные электроны изображены точками
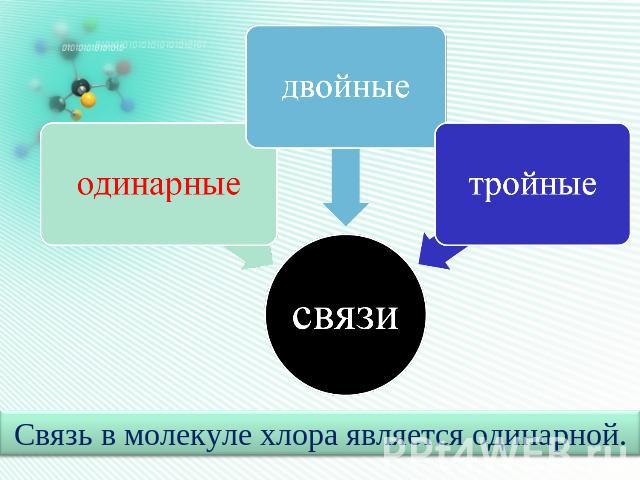
Связь в молекуле хлора является одинарной.

Образование молекулы азота (N2). В молекуле азота образуется тройная связь, значит атом азота трёхвалентен.

Образование молекулы хлороводорода (HCl). Водород и хлор в молекуле хлороводорода одновалентны, так как образуется одинарная связь.

фПрактическая часть. Составьте схему строения атома кислорода. Подчеркните валентные электроны и обозначьте их точками вокруг символа атома. Сколько электронов атома кислорода могут участвовать в образовании связей с атомами водорода?

Ответы. Число валентных электронов равно 6,из них неспаренных - 2 (8 – 6 = 2). В образовании связей с атомами водорода участвуют 2 неспаренных электрона .