Презентация на тему: Ковалентная полярная связь

Задание: 1. Выполнить на доске №5, страница 62. 2. Класс: записать образование молекул O2, H2, Br2, LiCl. Определить вид химической связи. 900igr.net

Мы условно разделили элементы на металлы и неметаллы. Рассмотрели, как образуются связи между атомами металлов и неметаллов (как называется такой вид связи?), между атомами одного и того же элемента неметалла (как называется такой вид связи?)

А какой тип связи мы можем ожидать при образовании соединений между атомами разных неметаллов?

Очевидно, опять ковалентную связь – засчет образования общих электронных пар. Но ведь элементы – то разные!!! Наверное, следует ожидать, что такая ковалентная связь будет отличаться от рассмотренной ранее ковалентной связи.

Атомы разных элементов по-разному относятся к общим электронным парам: те неметаллы, что сильнее, будут сильнее оттягивать к себе общие электронные пары, совсем как у Крылова: «У сильного всегда бессильный виноват…»

Ковалентная полярная химическая связь Урок на тему:

Цель урока: 1. Продолжить формирование понятия о ковалентной химической связи. 2. Познакомить учащихся с полярной ковалентной химической связью и электроотрицательностью (ЭО) как мерой неметалличности элементов. 3. Продолжить формирование умения записывать схемы образования молекул бинарных соединений элементов – неметаллов.

Электроотрицательность Способность атомов химических элементов оттягивать к себе общие электронные пары, называется электроотрицательнос-тью (ЭО)

Ряд электроотрицательности химических элементов H As I Si P Se C S Br Cl N O F Усиление электроотрицательности

Запишите в тетрадь (на странице 64, §11) как изменяется ЭО в периоде и подгруппе (смтр. запись курсивом со слов: в каждом периоде…)

Ряд электроотрицательности элементов поможет вам определить, в сторону атомов какого химического элемента будут смещены общие электронные пары, а, следовательно, на каком из атомов будет избыточный отрицательный заряд (он будет обозначаться буквой «δ» – греч. дельта), а, значит, где будет отрицательный полюс молекулы.

Разумеется, атомы менее электроотрицательного элемента будут иметь избыточный положительный заряд, т.е. будут представлять собой как бы положительный полюс молекулы с зарядом δ+. Вот вам и стало понятно название этой разновидности ковалентной связи – полярная.

Между атомами одного и того же элемента неметалла, т.е. с одинаковой электроотрицательностью, общие электронные пары не смещены ни к одному из атомов, поэтому они не имеют заряда – полюса и это неполярная ковалентная связь.

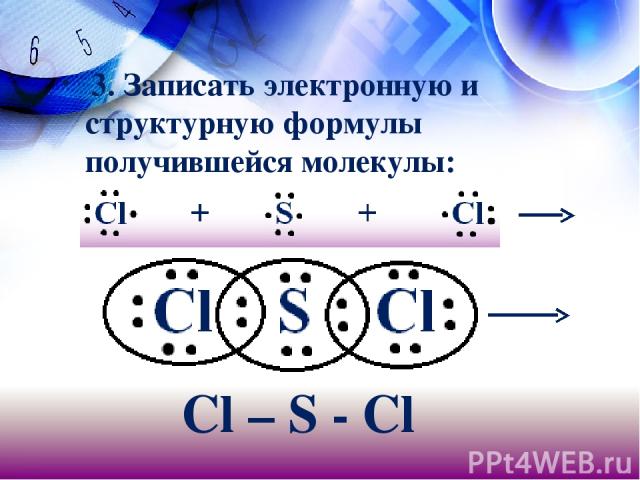
Теперь давайте с вами запишем алгоритм образования молекулы SCl2

1. Определить число внешних электронов у атомов неметаллов и по формуле 8 – N число неспаренных электронов. Записать электронные формулы атомов:

2. Записать символ элемента – неметалла, который представлен одним атомом (S), в центр и знаком «плюс» – два атома другого элемента (Сl):

3. Записать электронную и структурную формулы получившейся молекулы: Сl – S - Cl

4. Определить по ряду электроотрицательности, к атомам какого из элементов смещены общие электронные пары, и заменить черточки маленькими стрелками, обозначить полюса: Clδ- Sδ+ Clδ-

Закрепление Упражнение №2 на странице 66

Домашнее задание §11, закончить №2, стр. 66 Повторить все виды химической связи: определения, механизм образования