Презентация на тему: Химия Фосфор

ФОСФОР 900igr.net

«Чудовище лежало перед нами… Его огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза обведены огненными кругами. Я дотронулся до этой светящейся головы и, подняв руку, увидел, что мои пальцы тоже засветились в темноте. - Фосфор, – сказал я». ФОСФОР

Открытие фосфора. Происхождение названия элемента. Положение фосфора в периодической системе химических элементов. Нахождение фосфора в природе. Аллотропные модификации фосфора. Химические свойства элемента. Соединения фосфора и их свойства. Применение фосфора и его соединений Минеральные удобрения. ПЛАН УРОКА:
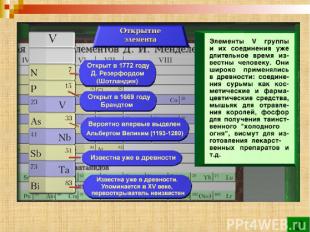

ПРОИСХОЖДЕНИЕ НАЗВАНИЯ Я светоносный элемент. Я спичку вам зажгу в момент. Сожгут меня – и под водой Оксид мой станет кислотой. V

ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ ?

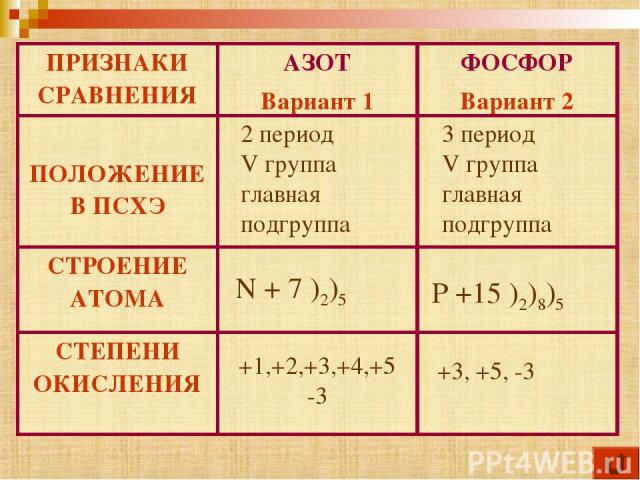
3 период V группа главная подгруппа 2 период V группа главная подгруппа Р +15 )2)8)5 N + 7 )2)5 +3, +5, -3 +1,+2,+3,+4,+5 -3 ПРИЗНАКИ СРАВНЕНИЯ АЗОТ Вариант 1 ФОСФОР Вариант 2 ПОЛОЖЕНИЕ В ПСХЭ СТРОЕНИЕ АТОМА СТЕПЕНИ ОКИСЛЕНИЯ

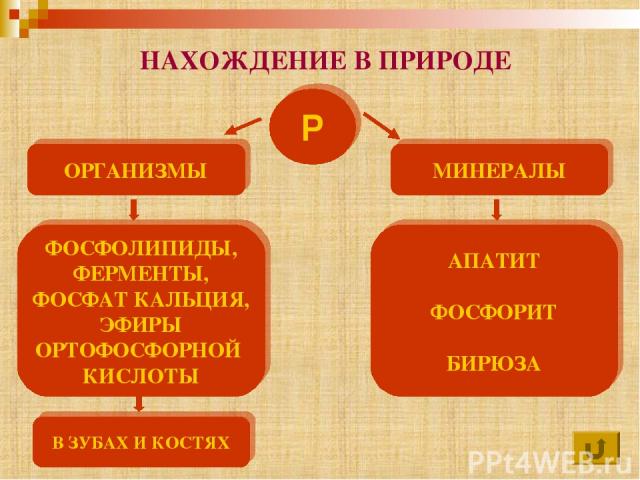
Р ОРГАНИЗМЫ МИНЕРАЛЫ ФОСФОЛИПИДЫ, ФЕРМЕНТЫ, ФОСФАТ КАЛЬЦИЯ, ЭФИРЫ ОРТОФОСФОРНОЙ КИСЛОТЫ В ЗУБАХ И КОСТЯХ АПАТИТ ФОСФОРИТ БИРЮЗА НАХОЖДЕНИЕ В ПРИРОДЕ
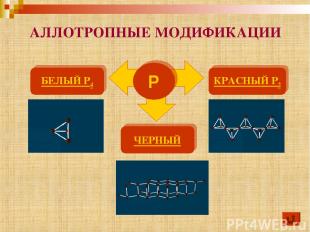
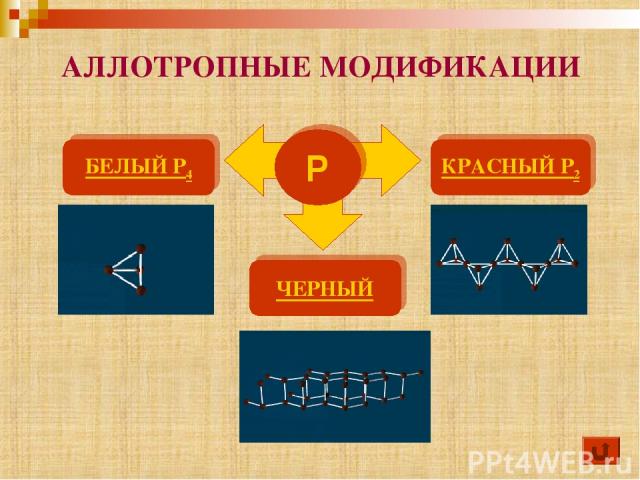
АЛЛОТРОПНЫЕ МОДИФИКАЦИИ Р БЕЛЫЙ P4 КРАСНЫЙ P2 ЧЕРНЫЙ

С металлами: Ca + P = C неметаллами: P + O2 = P + S = 4P0 + 5O02 = 2P+52O-25 3Ca0 + 2P0 = Ca+23P-32 ХИМИЧЕСКИЕ СВОЙСТВА 2P0 + 3O0 = 2P+32S-23
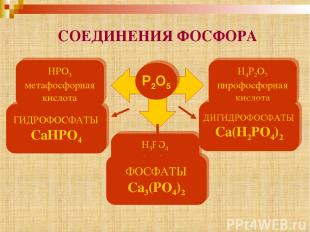
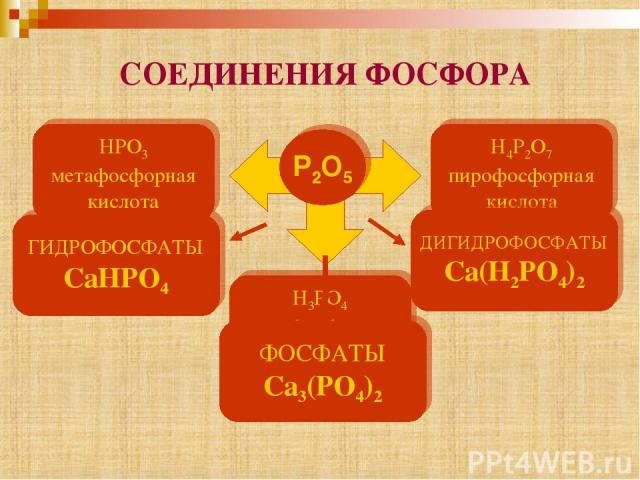
СОЕДИНЕНИЯ ФОСФОРА Р2O5 HPO3 метафосфорная кислота H4P2O7 пирофосфорная кислота H3PO4 ортофосфорная кислота ФОСФАТЫ Ca3(PO4)2 ГИДРОФОСФАТЫ CaНPO4 ДИГИДРОФОСФАТЫ Ca(Н2PO4)2
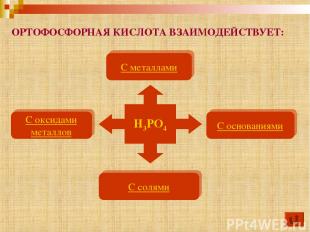
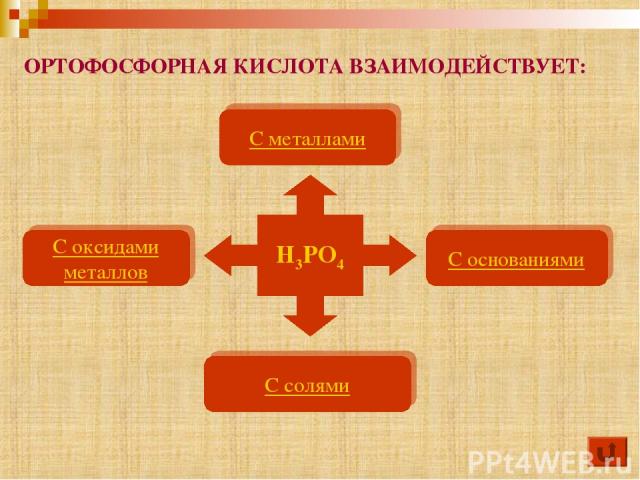
С металлами С основаниями С оксидами металлов С солями H3PO4 ОРТОФОСФОРНАЯ КИСЛОТА ВЗАИМОДЕЙСТВУЕТ:
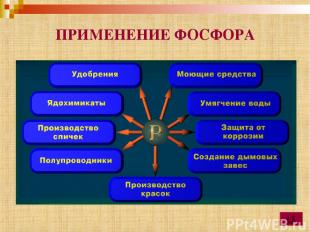
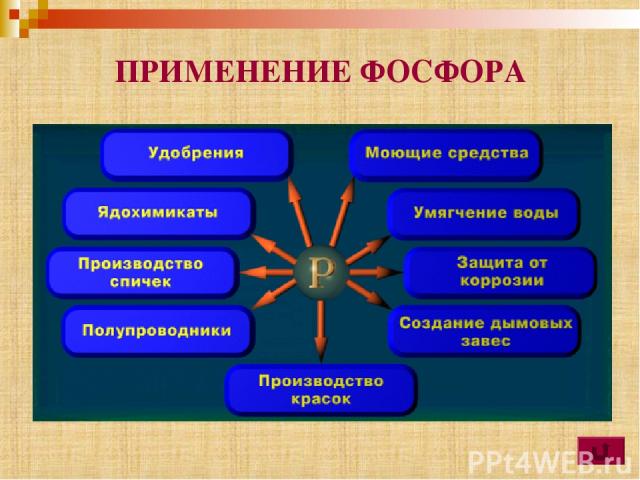
ПРИМЕНЕНИЕ ФОСФОРА
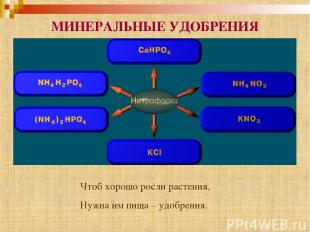
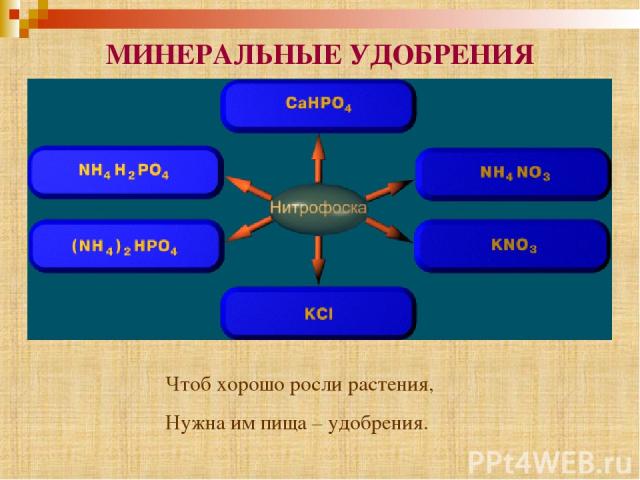
МИНЕРАЛЬНЫЕ УДОБРЕНИЯ Чтоб хорошо росли растения, Нужна им пища – удобрения.

ДОМАШНЕЕ ЗАДАНИЕ §27, упр. 2,3. Задача: Какова масса фосфора в вашем теле, если известно, что фосфор составляет ≈1% от массы тела?


Молекулы P4 имеют форму тетраэдра. Это легкоплавкое t(пл)=44,1оС, t(кип)=275оС, мягкое, бесцветное воскообразное вещество. Хорошо растворяется в сероуглероде и ряде других органических растворителей. Ядовит, воспламеняется на воздухе, светится в темноте. Хранят его под слоем воды. БЕЛЫЙ ФОСФОР

Существует несколько форм красного фосфора Их структуры окончательно не установлены. Известно, что они являются атомными веществами с полимерной кристаллической решеткой. Их температура плавления 585-600оС, цвет от темно-корчневого до красного и фиолетового. Не ядовит. КРАСНЫЙ ФОСФОР

Черный фосфор имеет слоистую атомную кристаллическую решетку. По внешнему виду похож на графит, но является полупроводником. Не ядовит. ЧЕРНЫЙ ФОСФОР

При комнатной температуре инертна. При повышенных температурах реагирует с большинством металлов. 2H3PO4+3Mg =Mg3(PO4)2+3H2 С металлами H3PO4

При комнатной температуре инертна. При повышенных температурах реагирует с большинством оксидов металлов. 2H3PO4+3CaO=Ca3(PO4)2+3H2O H3PO4 С оксидами металлов

Фосфорная кислота является относительно слабой кислотой. При её нейтрализации можно, например, получить дигидро- и гидрофосфаты натрия. Фосфат натрия таким путём получить не удаётся из-за сильного гидролиза по аниону. H3PO4+ NaOH=NaH2PO4+ H2O H3PO4 С основаниями H3PO4+2NaOH=Na2HPO4+2H2O

Фосфорная кислота может взаимодействовать с различными солями. Фосфорную кислоту и ее соли можно определить по выпадению желтого осадка при их взаимодействии с раствором нитрата серебра: 2H3PO4+3Na2СO3=2Na3PO4+3СО2+3H2O H3PO4 С солями H3PO4+3AgNO3=Ag3PO4↓+3HNO3

СПИСОК ЛИТЕРАТУРЫ: Габриелян О.С. Настольная книга учителя. Химия. 9 класс. – М.: Дрофа, 2002. Габриелян О.С. Химия. 9 кл.: рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 9 класс». – М.: Дрофа, 2005. Габриелян О.С. Химия. 9 класс: учеб. для общеобразоват. учеб. заведений. – М.: Дрофа, 2000. Образовательный комплекс 1 С: Школа. Химия, 8 класс. [Электронный носитель]. – М.: Фирма «1 С», 2004. Химия. 9 класс. Поурочные планы по учебнику «Химия. 9 класс» О.С. Габриеляна. – М.: Дрофа, 2002. Уроки химии Кирилла и Мефодия. 8-9 класс. [Электронный носитель]. – М.: «Кирилл и Мефодий», 2002.