Презентация на тему: Гидролиз солей


Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого изменяется рН среды. В процессе гидролиза соли в водном растворе появляется избыток катионов Н+ или анионов ОН- ГИДРОЛИЗ – это реакция обмена между некоторыми солями и водой приводящая к образованию слабого электролита.
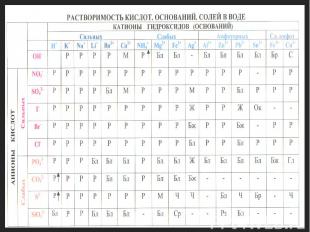



H2O H+ + OH- H2O H+ + OH- Na2CO3 2Na+ + CO32- 2Na+ +CO32- +HOH HCO3- +2Na+ +OH-

Сформулируем вывод: Сформулируем вывод: Раствор соли, образованной ________________, имеет__________реакцию, так как в растворе избыток ________________.
![Na2CO3 Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что с Na2CO3 Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что с](https://fs1.ppt4web.ru/images/95241/114557/310/img7.jpg)
Na2CO3 Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что сильней того и больше!) Щ е л о ч н а я среда


H2O H+ + OH- H2O H+ + OH- AlCl3 Al3+ + 3Cl- Al3+ +3Cl- +HOH Al OH2+ +H+ + 3Cl-

Сформулируем вывод: Сформулируем вывод: Раствор соли, образованной ________________, имеет _____________реакцию, так как в растворе избыток___________________.
![AlCl3 AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- < [H]+ (что си AlCl3 AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- < [H]+ (что си](https://fs1.ppt4web.ru/images/95241/114557/310/img11.jpg)
AlCl3 AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- < [H]+ (что сильней того и больше!) К и с л а я среда


H2O H+ + OH- H2O H+ + OH- NaСl Na+ + Cl- Na+ +Cl- +HOH Cl- + Na+ + HOH Данная соль гидролизу не подвергается.

Сформулируем вывод: Сформулируем вывод: Раствор соли, образованной__________________, имеет________________________реакцию, так как в растворе__________________________________.
![NaCl NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е й т р а л NaCl NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е й т р а л](https://fs1.ppt4web.ru/images/95241/114557/310/img15.jpg)
NaCl NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е й т р а л ь н а я среда







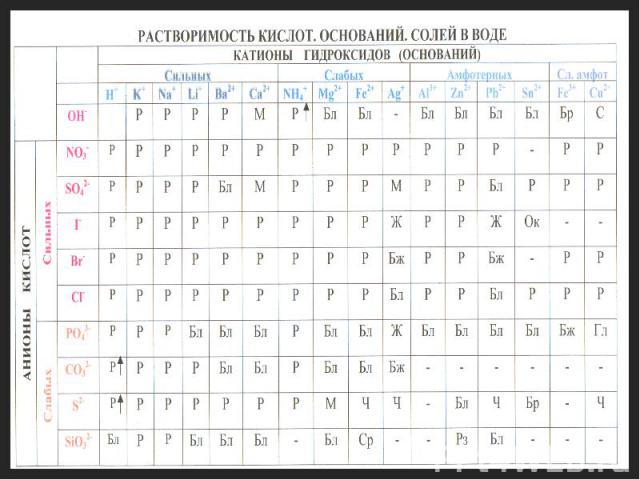




![Na2CO3 Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что сильней того и больше!) Щ е л о ч н а я среда Na2CO3 Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что сильней того и больше!) Щ е л о ч н а я среда](https://fs1.ppt4web.ru/images/95241/114557/640/img7.jpg)



![AlCl3 AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- < [H]+ (что сильней того и больше!) К и с л а я среда AlCl3 AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- < [H]+ (что сильней того и больше!) К и с л а я среда](https://fs1.ppt4web.ru/images/95241/114557/640/img11.jpg)



![NaCl NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е й т р а л ь н а я среда NaCl NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е й т р а л ь н а я среда](https://fs1.ppt4web.ru/images/95241/114557/640/img15.jpg)