Презентация на тему: Галогены

Галогены

Галогены 1. История открытия галогенов 2. Положение в Периодической системе 3. Химические свойства 4. Применение 5.Проверка знаний 6.Домашнее задание. Итоги урока.

История открытия галогенов Фтор Хлор Бром Йод Астат

История открытия фтора В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры –23°C (в жидкости должно содержаться немного фторида калия, который обеспечивает ее электропроводимость), смог на аноде получить первую порцию нового, газа. В первых опытах для получения фтора Муассан использовал очень дорогой электролизер, изготовленный из платины и иридия. При этом каждый грамм полученного фтора «съедал» до 6 г платины.

История открытия хлора В 1774 году шведский ученый К. Шееле открыл хлор, который принял за сложное вещество и назвал "дефлогистированной соляной кислотой". В 1807 году английский химик Гемфри Дэви получил тот же газ. Он пришел к выводу, что получил новый элемент и назвал его "хлорин" (от "хлорос" - желто-зеленый). В 1812 году Гей-Люсеок дал газу название хлор.

История открытия брома В 1825 году французский химик А.Ж.Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал - "мурид" (от латинского слова muria, означающего "рассол"). Комиссия Академии, проверив это сообщение, подтвердила открытие Балара и предложила назвать элемент бромом (от "бромос", с греческого "зловонный").

История открытия йода В 1811 году французский химик Бернар Куртуа открыл иод путём перегонки маточных растворов от своего азотнокислого кальция с серной кислотой Чтобы другие химики могли изучать новое вещество, Б. Куртуа подарил его (правда, очень небольшое количество) фармацевтической фирме в Дижоне. В 1813 году Ж.-Л.Гей-Люссак подробно изучил этот элемент и дал ему современное название. Название "иод" происходит от греческого слова "иодэс" - "фиолетовый" (по цвету паров).

История открытия астата В 1869 г Д.И.Мендеелеев предсказал его существование и возможность открытия в будущем (как «эка-иод»). Впервые астат был получен искусственно в 1940 г открыт Д.Корсоном, К.Маккензи и Э.Сегре (Калифорнийский университет в Беркли) . Для синтеза изотопа 211At они облучали висмут альфа-частицами. В 1943-1946 годах изотопы астата были обнаружены в составе природных радиоактивных рядов. Астат является наиболее редким элементом среди всех, обнаруженных в природе. В поверхностном слое земной коры толщиной 1,6 км содержится всего 70 мг астата.

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Химические свойства 45F2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с участием Au, Pt. С простыми веществами: С металлами С неметаллами Na + F2 → H2 + F2 → Mo + F2 → Xe + F2 → Со сложными веществами: H2O + F2 → KCl + F2 → KBr + F2 → KI + F2 →

Химические свойства 45F2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с участием Au, Pt. С простыми веществами: С металлами С неметаллами 2Na + F2 → 2NaF H2 + F2 → 2HF Mo + 3F2 → MoF6 Xe + 2F2 → XeF4 Со сложными веществами: 2H2O + F2 → 4HF + O2 2KCl + F2 → Cl2 + 2NaF 2KBr + F2 → Br2 + 2КF 2KI + F2 → I2 + 2КF

Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2 и некот. др.) С простыми веществами: С металлами С неметаллами Fe + Cl2 → H2 + Cl2 → Cu + Cl2 → P + Cl2 → Со сложными веществами: H2O + Cl2 → NaOH + Cl2 → KBr + Cl2 → KI + Cl2 →

Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2 и некот. др.) С простыми веществами: С металлами С неметаллами 2Fe + 3Cl2 → 2FeCl3 H2 + Cl2 → 2HCl (tº, hυ) Cu + Cl2 → Cu Cl2 2P + 5Cl2 → 2PCl5 ( tº, в изб. Сl2) Со сложными веществами: H2O + Cl2 → HCl+HClO хлорная вода 2NaOH + Cl2 → NaOCl + NaCl + H2O жавелевая вода 2KBr + Cl2 → Br2 + 2КCl 2KI + Cl2 → I2 + 2КCl

Химические свойства Br2 - реакционноспособен С простыми веществами: С металлами С неметаллами Al + Br2 → H2 + Br2 → Cu + Br2 → P + Br2 → Со сложными веществами: Br2 + H2O → KI + Br2 →

Химические свойства Br2 - реакционноспособен С простыми веществами: С металлами С неметаллами 2Al + 3Br2 → 2AlBr3 H2 + Br2 → 2HCl Cu + Br2 → Cu Br2 2P + 5Br2 → 2PBr5 Со сложными веществами: Br2 + H2O → HBr + HBrO бромная вода 2KI + Br2 → I2 + 2КCl

Химические свойства I2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg + I2 → H2 + I2 → Al + I2 → P + Br2 → Со сложными веществами: I2 + H2O → I2 + р-р крахмала →

Химические свойства I2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg + I2 → HgI2 H2 + I2 → 2HCl (tº) 2Al + 3I2 → 2AlI3 2P + 3Br2 → 2PI3 Со сложными веществами: I2 + H2O → HI + HIO I2 + р-р крахмала → темно-синее окрашивание
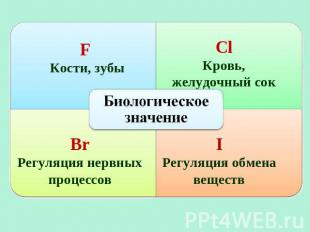
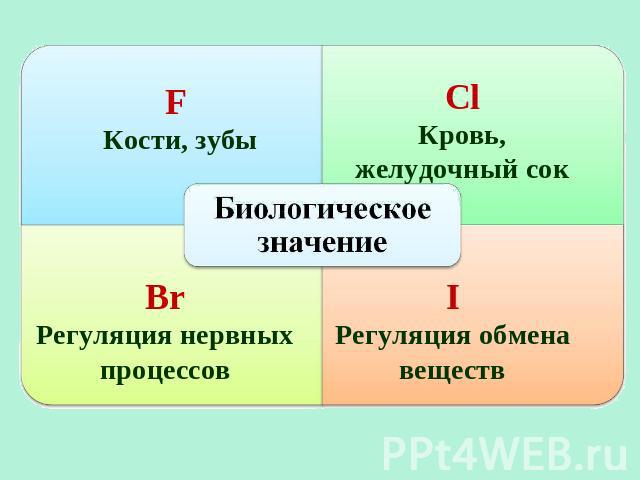
F Кости, зубы Сl Кровь, желудочный сок Br Регуляция нервных процессов I Регуляция обмена веществ
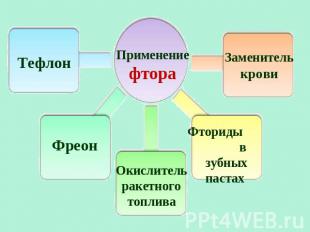
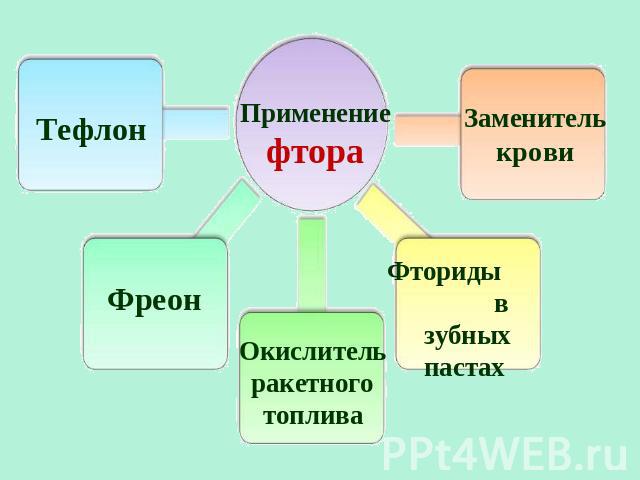
Тефлон Применение фтора Заменитель крови Фреон Окислитель ракетного топлива Фториды в зубных пастах Применение фтора
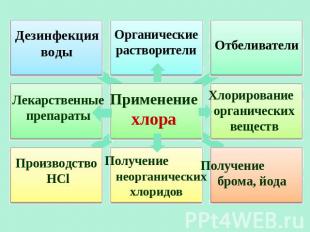
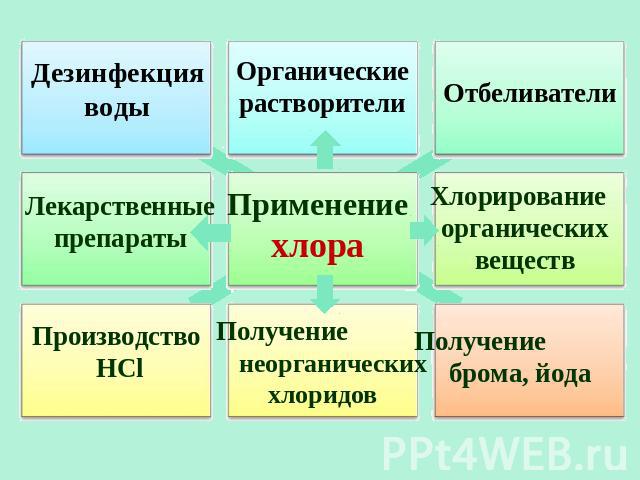
Дезинфекция воды Органические растворители Отбеливатели Отбеливатели Применение хлора Хлорирование органических веществ Производство HCl Получение неорганических хлоридов Получение брома, йода
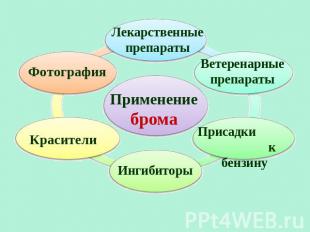
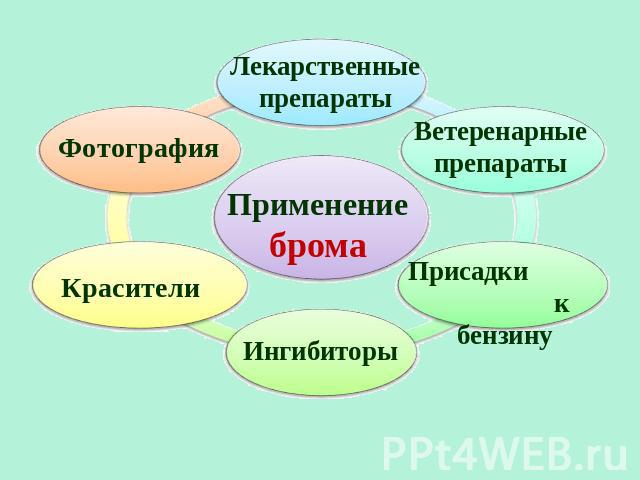
Лекарственные препараты Фотография Применение брома Ветеренарные препараты Красители Ингибиторы Присадки к бензину
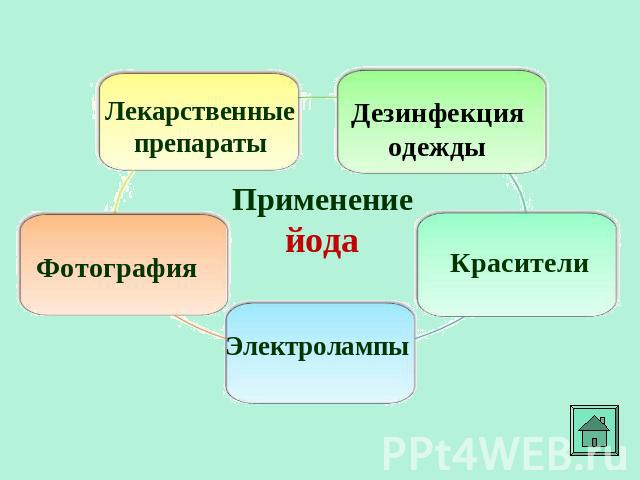
Лекарственные препараты Дезинфекция одежды Фотография Применение йода Красители Электролампы

Физические свойства галогеновЗаполни пропуски Фтор - , в воде , так как интенсивно с ней взаимодействует. Хлор - , раствор хлора в воде практически бесцветен - . Бром - . Йод - с с металлическим блеском. Кристаллический йод легко - переходит из твердого в газообразное состояние. Астат похож на , но имеет более ярко выраженный металлический характер. Все галогены обладают запахом, вдыхание их вызывает сильнейшее раздражение дыхательных путей и тяжелые .

Химические свойства галогеновПоставь коэффициенты Na + Cl2 = NaCl S + F2 = SF6 Fe + Br2= FeBr3 P + Cl2 = PCl5 NaI + Cl2 = NaCl + I2 F2 + H2O = HF + O2 NaBr + Cl2 = NaCl + Br2 KOH + Cl2 = KCl + KClO3 + H2O

Химические свойства галогеновНайди соответствие между исходными веществами и продуктами реакций

Спасибо за урок! Благодарю за сотрудничество.

Использованная литература, интернет-ресурсы «Химия-9», О.С.Габриелян, М, Дрофа,2005г, стр 78-90 «Химия в действии», М.Фримантл, М, «Мир»,1991г, стр 269-286. «Неорганическая химия в таблицах»,Н.В.Манцевич, Минск, Современная школа,2008г, стр 275-280 http://www.chem100.ru/ http://rrc.dgu.ru/res/n-t.ru/ri/ps/index.htm http://www.periodictable.ru/ http://sevchem.info/?go=galeri&act=show_photo&idr=17&id_f=35 http://sevchem.info/?go=galeri&act=show_photo&idr=17&id_f=23 http://sevchem.info/?go=galeri&act=show_photo&idr=17&id_f=72 http://ru.wikipedia.org/wiki/%D0%A4%D1%80%D1%8D%D0%B4_%D0%90%D0%BB%D0%BB%D0%B8%D1%81%D0%BE%D0%BD