Презентация на тему: Вода в природе

Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения:

Водород. Нахождение в природе. Физические и химические свойства. Применение. Через тернии к звёздам... Цель: Познакомиться с распространением водорода в природе Изучить физические и химические свойства водорода в сравнении с кислородом Рассмотреть основные области применения водорода

ВОДОРОД В П Р И Р О Д Е

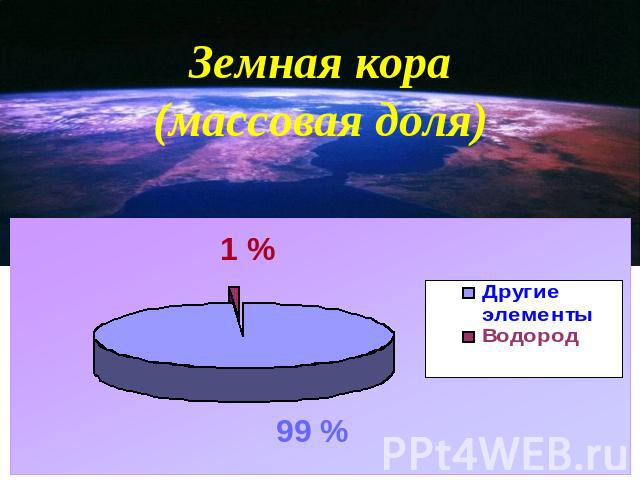
Земная кора (массовая доля)

В составе атмосферного воздуха присутствие водорода менее 0,0001 %




Горные породы и минералы Каменный уголь

На долю водорода приходится 50 % массы Солнца и других звезд


Какое соединение богаче водородом: H2O или CH 4 ? РЕШЕНИЕ:

Генри Кавендиш

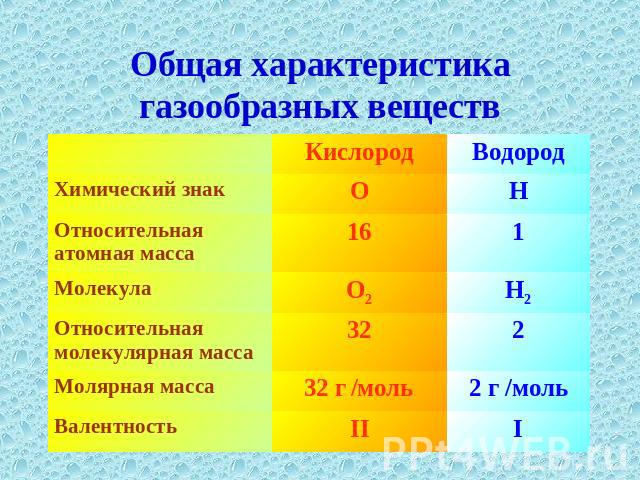
Общая характеристика газообразных веществ
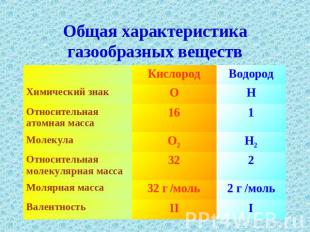
Общая характеристика газообразных веществ



Получение водорода. В лаборатории: Взаимодействие цинка с соляной кислотой: Zn+2H Cl=ZnCl2+ H2 хлорид цинка Взаимодействие калия с водой: 2К+2H2O=2KOH+H2 гидроксид калия В промышленности: Разложение воды электрическим током: 2H2O=2H2+O2





П р и м е н е н и е в о д о р о д а Для получения аммиака NH3 Для получения метилового спирта СH3OH Для получения соляной кислоты HCl Восстановитель металлов и оксидов Как топливо H2

Домашнее задание: п. 6.1 – 6.6; Конспект в тетради; Творческое задание «Почему Водород называют топливом будущего?»


Проверь себя: 1 – а 2 – а 3 – в 4 - а

1. Я узнал(а) много нового. 2. Мне это пригодится в жизни. 3. На уроке было над чем подумать. 4. На все возникшие у меня вопросы, я получил(а) ответы. 5. На уроке я поработал(а) добросовестно.

С п а с и б о з а в н и м а н и е ! У с п е х о в в р а б о т е !