Презентация на тему: Физические и химические свойства кислот

Физические и химические свойства кислот. Учитель химии МОУ СОШ №41: Бронникова Марина Александровна г.Челябинск 900igr.net

Ожидаемые результаты: Знать состав формул, определение кислот, индикаторов, физические и химические свойства кислот. Совершенствовать: учебные умения по составлению химических уравнений, практические навыки по проведению лабораторных опытов. Способствовать развитию умений сравнивать, обобщать, делать выводы; Развивать внимание, мышление и память. Повторить и закрепить правила ТБ при работе с веществами. Воспитывать бережливое отношение к реактивам и оборудованию, дисциплинированность, аккуратность и умение работать в группе.

Разгадайте шараду: Мы первым слогом подзовем кота, Вторым измерим с судна толщу вод, Союз на окончание пойдет, И целым станет слово... (Кис-лот-а.)

Кислоты — это сложные вещества, состоящие из атомов водорода и кислотного остатка. Нn+1 (KO)-n

Формулы, каких веществ «лишние» и почему? 1)HCI 2)CO2 3)NaOH 4) H2SO4 5) NaCI 6) H3PO4 7) HNO3 8) H2S 9) СаО 10) H2CO3 11)Н2О 12)Н2SiO4

Дать название кислотам: HCI H2SO4 H3PO4 HNO3 H2S НNO2 H 2SO3 H2CO3 Н2SiO4
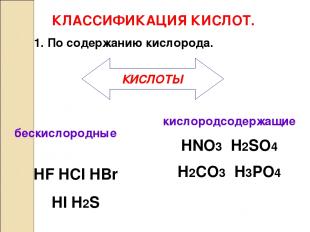
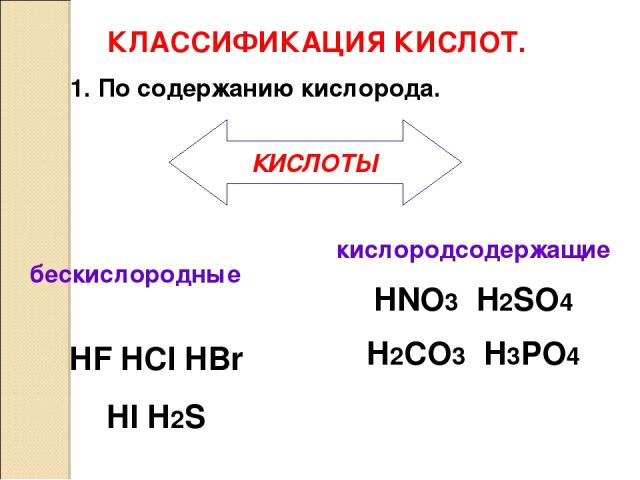
КЛАССИФИКАЦИЯ КИСЛОТ. бескислородные HF HCl HBr HI H2S 1. По содержанию кислорода. кислородсодержащие HNO3 H2SO4 H2CO3 H3PO4 КИСЛОТЫ
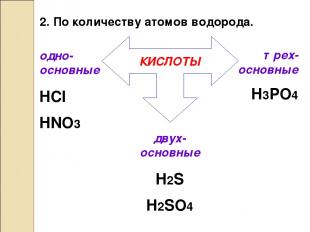
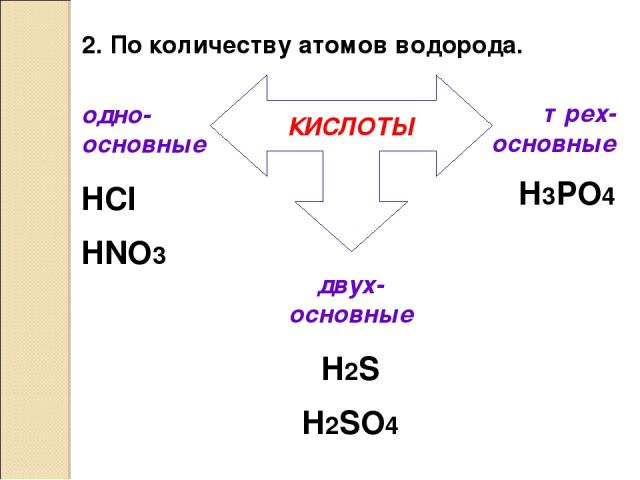
2. По количеству атомов водорода. КИСЛОТЫ одно-основные HCl HNO3 двух-основные H2S H2SO4 трех-основные H3PO4

Физические свойства кислот При обычных условиях кислоты могут быть твердыми и жидкими. Кислоты –едкие жидкости (кроме кремневой), с кислым вкусом, без запаха, разъедают многие вещества.

Польза кислот

Вред кислот

Техника безопасности от строгой химички. Ты в хим. кабинет пришел Так запомни кроха Безопасность хорошо, Быть безруким плохо. Ты над брюками держал С кислотой пробирку? Круто, парень, ты попал – На штанишки с дыркой! При работе с кислотой Не нужна тревога. С осторожностью простой Избежишь ожога.

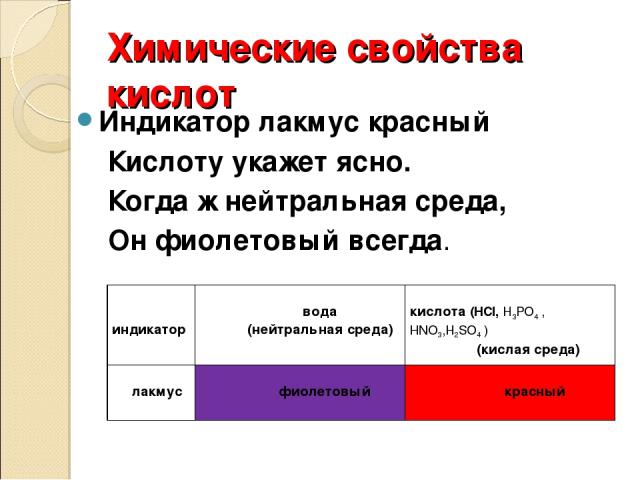
Химические свойства кислот Индикатор лакмус красный Кислоту укажет ясно. Когда ж нейтральная среда, Он фиолетовый всегда. индикатор вода (нейтральная среда) кислота (НСl, H3PO4 , НNO3,H2SO4 ) (кислая среда) лакмус фиолетовый красный
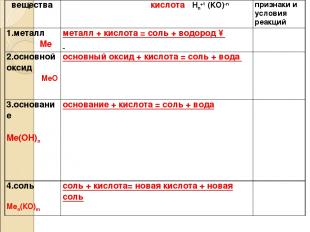
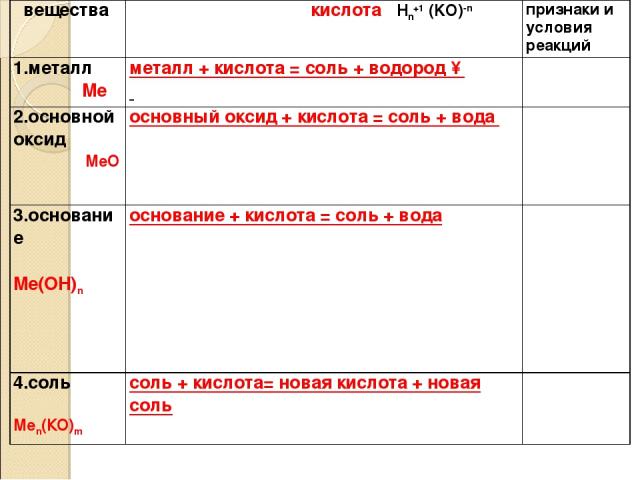
вещества кислота Нn+1 (KO)-n признаки и условия реакций 1.металл Ме металл + кислота = соль + водород ↑ 2.основной оксид МеО основный оксид + кислота = соль + вода 3.основание Ме(ОН)n основание + кислота = соль + вода 4.соль Меn(КО)m соль + кислота= новая кислота + новая соль
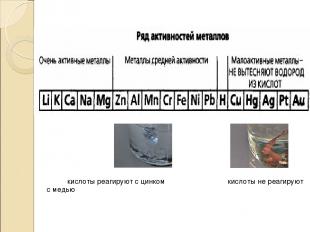
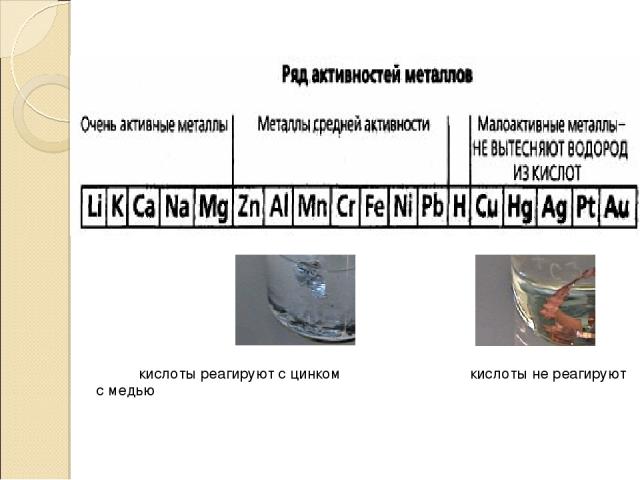
кислоты реагируют с цинком кислоты не реагируют с медью

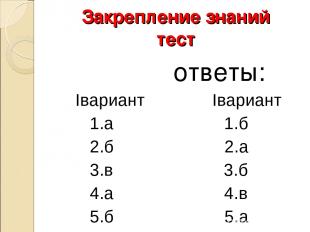
Закрепление знаний тест ответы: Iвариант Iвариант 1.а 1.б 2.б 2.а 3.в 3.б 4.а 4.в 5.б 5.а

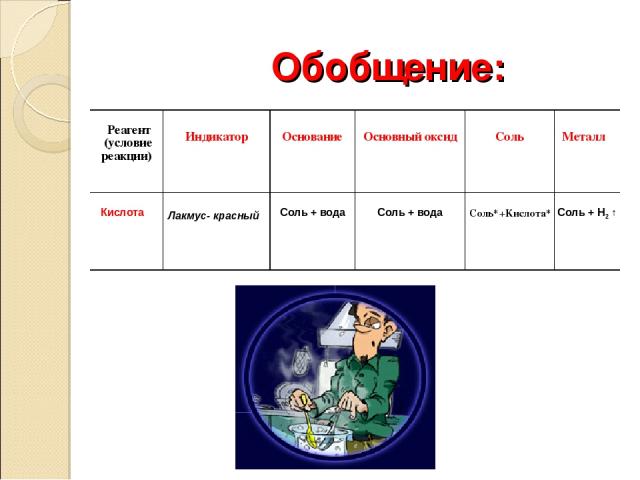
Обобщение: Реагент (условие реакции) Индикатор Основание Основный оксид Соль Металл Кислота Лакмус- красный Соль + вода Соль + вода Соль*+Кислота* Соль + Н2 ↑

Домашнее задание §20, 38 упр.4, дополнительно упр.6 стр.214 Составить кроссворд по теме «Кислоты».

БЛАГОДАРЮ ЗА УРОК ! УСПЕХА!