Презентация на тему: Биополимеры

Биополимеры

белки Нуклеиновые кислоты биополимеры углеводы липиды

белки строение структура аминокислоты функции классификация белков В начало

Строение белков Белки – это высокомолекулярные азотистые соединения, состоящие из аминокислот, связанных пептидными связями. Элементарный состав белков: С - 50%-55% Н – 6,3%-7,5% О – 21,5%-23,5% N – 15%-18% S - 0%-2,4% Р – 0%-2% Наиболее важным показателем является содержание N в белках. По содержанию N можно определить содержание белка в том или ином объекте:%белка = %N x 6,25 Как и любой биополимер белки также состоят из мономеров. Мономером белков является аминокислота. Выделяют примерно 170 аминокислот. Только 20 из них входят в состав белков. Они называются протеиногенными. NH2 – CH – COOH NH2 - аминогруппа СOOH – карбоксильная группа R Аминокислоты отличаются друг от друга только радикалами (R). Аминокислоты можно разделить на 2 группы: 1) заменимые (при отсутствии этих аминокислот они могут быть заменены другой аминокислотой близкой по строению); 2) незаменимые (при отсутствии этих аминокислот они не могут быть заменены другой аминокислотой (триптофан, метионин, лизин и др.). Они синтезируются только в автотрофных организмах.

Аминокислоты

Структура белков первичная вторичная четвертичная третичная

первичная стуртура белков Последовательное расположение аминокислотных остатков в полипептидной цепи. …- ала – лиз – вал – вал – иле - … Первичная структура белков может быть использована для систематической номенклатуры белков.

вторичная стуктура белков Происходит пространственное расположение полипептидной цепи. В зависимости от торсионных углов возможно образование 3 основныхтипов вторичной структуры:1) α – спираль. Торсионный угол колеблется от 45 до 60 градусов. Нативные (действующие) белки образуют правозакрученную α – спираль.Шаг спирали (один виток) – 0,54 нм, в шаге спирали 3,6 аминокислоты. Диаметр спирали – 0, 5 нм. Стабилизация α – спирали осуществляется за счет водородных связей, возникающих между соседними витками. 2) β – спираль. Торсионный угол от 120 до 130 градусов. Характерная особенность: они образуют складчатые слои. Диаметр спирали – 0,1 нм, шаг спирали – 0,33 нм, в шаге спирали 2,6 аминокислоты.Стабилизация осуществляется за счет межмолекулярных водородных связей между соседними молекулами.3) β – изгиб. В состав может входить до 4 аминокислотных остатков. Происходит определенная укладка полипептидной цепи.Существуют также другие виды вторичной структуры: π – спираль (отличается от α - спирали линейными группами. И др.

третичная стуктура белков Происходит общее пространственное расположение белковой молекулы. Третичная структура определяется формой «упаковки» доменов. (домен – это определенные структуры, состоящие из разных типов вторичной структуры белков). В зависимости от соотношения α и β участков различают глобулярные и фибриллярные третичные структуры белков. Происходит образование структуры называемой глобула. В стабилизации третичной структуры участвуют:1) дисульфитные ковалентные связи, образующиеся между остатками аминокислоты цистеина. Основная роль в стабилизации;2) водородные связи; 3) ионная связь;4) гидрофобное взаимодействие.

четвертичная структура белков Четвертичную структуру имеют только белки, состоящие из нескольких субъединиц. Это сформировавшаяся часть белковой молекулы, имеющий первичную, вторичную, третичную структуры. В состав белковых молекул обычно входят четное число субъединиц. Это обусловлено тем, что четное число субъединиц образует стабильную пространственную конфигурацию белков (тетраэдрическая, кубическая, диэдрическая и др.). Происходит пространственное расположение субъединиц. Примером четвертичной структуры может служить молекула гемоглобина, которая входит в состав эритроцитов (красные клетки крови). В состав гемоглобина входят 4 субъединицы (образуется тетраэдрическая конфигурация молекулы белка). Стабилизация структуры происходит за счет гидрофобных взаимодействий возникающих между субъединицами).

Функции белков 1) Пластическая (строительная) функция. Белки участвуют в образовании всех клеточных мембран и органоидов клетки, а также внеклеточных структур. 2) Каталитическая функция. Все биологические катализаторы – ферменты – вещества белковой природы, они ускоряют химические реакции, протекающие в клетке, в десятки и сотни тысяч раз. 3) Двигательная функция. Обеспечивается специальными сократительными белками. Эти белки участвуют во всех видах движения, к которым способны клетки и организмы: мерцание ресничек и биение жгутиков у простейших, сокращение мышц и многоклеточных животных, движение листьев у растений и др. 4) Транспортная функция. Происходит присоединение химических элементов (например, кислорода гемоглобином) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела. Очень много транспортных белков в мембранах клеток, они перенося различные вещества из окружающей среды в клетку. 5) Защитная функция. При поступлении чужеродных белков или микроорганизмов в лейкоцитах образуются особые белки - антитела. Они связываются с чужеродными веществами- антигенами. В результате образуется безвредный, нетоксичный комплекс – антигенантитело, который впоследствии фагоцитируется. 6) Энергетическая функция. Белки могут служить источником энергии. При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии. Однако, в таком качестве белки используются очень редко. 7) Регуляторная функция. Происходит за счет особых белков – гормонов. Они поддерживают постоянные концентрации веществ в крови и клетках, участвуют в росте, размножении и других жизненно важных процессах. Например, инсулин регулирует уровень глюкозы в крови. 8) Сигнальная функция. В мембрану встроены особые белки, способные изменять свою третичную структуру на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача информации в клетку.

классификация белков I. По химическому составу выделяют белки:1) Простые (протеины), состоящие только из аминокислот.2) сложные (протеиды), кроме аминокислот, в состав белков входят различные добавочные группы (нуклеопротеиды, гликопротеиды, и др.) II. По растворимости в различных растворителях:1) Альбумины – растворяются в насыщенных растворах минеральных солей;2) глобулины - растворяются в полунасыщенных растворах минеральных солей;3) проламины – растворяются в 60%-80% этаноле;4) глютаимины – растворяются в щелочных растворах и др. III. По характеру добавочных групп:1) Металлопротеиды2) Неметаллопротеиды.

Нуклеиновые кислоты ДНК РНК В начало

Д Н К Строение Функции Структура

Строение ДНК Нуклеиновые кислоты – высокомолекулярные соединения, характеризующиеся определенным элементарным составом и состоящие из нуклеотидов (АГЦО, углевод, остаток фосфорной кислоты. К ним относятся: ДНК, РНК.ДНК – дезоксирибонуклеиновая кислота РНК – рибонуклеиновая кислота Мономером нуклеиновых кислот является нуклеотид (структурная единица).Нуклеотид: 1) Азотистые гетороциклические основания: А – аденин Т – тимин (ДНК) У – урацил (РНК) Ц – цитозин Г – гуанин 2) углевод – пентоза: ДНК – дезоксирибоза РНК – рибоза 3) остаток фосфорной кислоты

Структура ДНК первичная третичная вторичная четвертичная

Первичная структура ДНК Происходит последовательное расположение нуклеотидов в полинуклеотидной цепи. В ходе изучения первичной структуры были открыты некоторые закономерности. 1) А + Г = Ц + Т Молекулярная масса пуриновых оснований равна молекулярной массе пиримидиновых оснований. 2) Отношение аденин-тиминовых пар и гуанин-цитозиновых пар представляет коэффициент специфичности ДНК. Этот показатель различается у различных видов животных. В ходе изучения первичной структуры было установлено, что 64% участков ДНК составляют уникальную последовательность. Такие участки называются – структурные гены. Структурные гены обеспечивают биосинтез специфических белков. Остальные гены контролируют синтез белка, которые требуются в больших количествах.

Вторичная структура Д Н К Происходит определенное пространственное расположение полинуклеотидной цепи. Характерной особенность вторичной структуры является спирализация полинуклеотидной цепи. У ДНК уровень спирализации достигает до 100%. Вторичная структура была установлена Уотсоном и Криком (получили Нобелевскую премию). В состав молекулы ДНК входят две полинуклеотидные цепи, образуя двойную спираль. Закрутка спирали правая. Основа расположена снаружи (углевод, остаток фосфорной кислоты), а – азотистые основание внутри. АГЦО, между которыми образуются водородные связи образуют комплементарные пары: А – Т Г – Ц Между А и Т образуются две водородные связи. Между Г и Ц – три. Выделяют несколько форм вторичной структуры ДНК:1) В – форма. Расположение АГЦО перпендикулярно к оси молекулы. В шаг спирали входят 16 пар нуклеотидов. Эта форма более стабильная. 2) А – форма. Расположение АГЦО происходит под углом 70 градусов к оси. В шаг спирали входят 11 пар нуклеотидов. Эта форма образуется в ходе репликации и транскрипции. 3) Z – форма. Характеризуется левой закруткой спирали. В шаг спирали входит 12 пар нуклеотидов.

Третичная структура Д Н К Происходит общее пространственное расположение молекулы ДНК. Благодаря третичной структуре происходит «плотная» упаковка молекулы ДНК в клетках прокариот и хромосомах ядра эукариот. Вещество хромосом называется хроматином и он содержит: ДНК, белки и некоторое количество РНК. Белки, входящие в состав белков: гистоны. Различают 5 видов гистонов, отличающиеся содержанием лизина и аргинина. В результате образуются нуклеосомы (размеры молекулы ДНК уменьшаются в20-50 раз). В состав нуклеосомы входит 145-150 нуклеотидов. Происходит скручивание нуклеосом, в результате образуется структура – соленоид (катушка) (размеры уменьшаются в 20-60 раз). Соленоиды образуют фибриллярные структуры (размеры уменьшаются в 200 раз). За счет которых образуются впоследствии хромосомы. В результате всей упаковки молекула ДНК уменьшается в 100 000 раз.

Четвертичная структура Д Н К Происходит общее пространственное расположение отдельных молекул ДНК в хромосоме и взаимное расположение отдельных молекул ДНК и РНК в ходе биосинтеза белка.

Функции Д Н К Значение ДНК (как РНК) в клетке очень велико. Особенности их химического строения обеспечивают возможность хранения, переноса и передачи по наследству дочерним клеткам информации о структуре белковых молекул, которые синтезируются в каждой ткани на определенном этапе индивидуального развития. Стабильность нуклеиновых кислот - важнейшее условие нормальной жизнедеятельности клеток влекут за собой изменения структуры клеток или активности физиологических процессов в них, влияя таким образом на жизнеспособность.

Р Н К виды строение

Строение РНК РНК, как и ДНК представляет собой биополимер, мономерами которого являются нуклеотиды, состоящие из трех основных компонентов: 1) азотистое основание; 2) углевод – рибозы; 3) остаток фосфорной кислоты. В состав РНК входят те же самые азотистые основания, что и в ДНК. Но вместо тимина (Т) в состав РНК входит урацил (У). По структуре различают одноцепочечные и двуцепочечные РНК. Двуцепочечные РНК являются хранителем наследственной информации у ряда вирусов. Существует несколько видов одноцепочечных РНК: т-РНК, и-РНК, р-РНК.

Виды Р Н К т – РНК (транспортная) р – РНК (рибосомная) и – РНК (информационная, матричная)

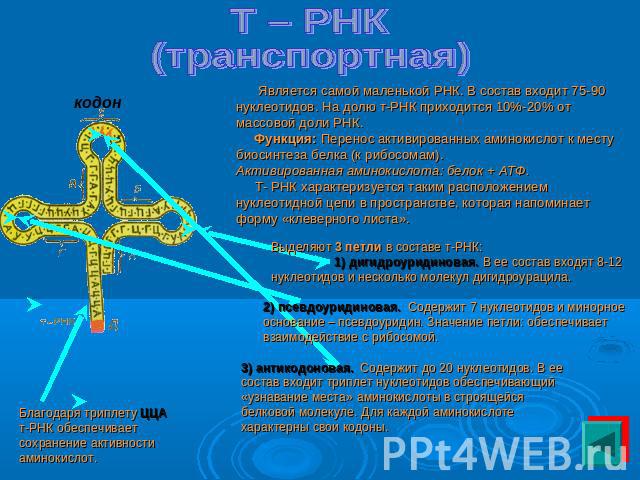
Т – РНК (транспортная) Является самой маленькой РНК. В состав входит 75-90 нуклеотидов. На долю т-РНК приходится 10%-20% от массовой доли РНК. Функция: Перенос активированных аминокислот к месту биосинтеза белка (к рибосомам). Активированная аминокислота: белок + АТФ. Т- РНК характеризуется таким расположением нуклеотидной цепи в пространстве, которая напоминает форму «клеверного листа». Выделяют 3 петли в составе т-РНК: 1) дигидроуридиновая. В ее состав входят 8-12 нуклеотидов и несколько молекул дигидроурацила. 2) псевдоуридиновая. Содержит 7 нуклеотидов и минорное основание – псевдоуридин. Значение петли: обеспечивает взаимодействие с рибосомой. 3) антикодоновая. Содержит до 20 нуклеотидов. В ее состав входит триплет нуклеотидов обеспечивающий «узнавание места» аминокислоты в строящейся белковой молекуле. Для каждой аминокислоте характерны свои кодоны. Благодаря триплету ЦЦА т-РНК обеспечивает сохранение активности аминокислот.

и – РНК (информационная, матричная) И - РНК образуется в ходе транскрипции на молекуле ДНК, поэтому первичная структура и-РНК является «отражением» соответствующего гена. Помимо этого в ходе биосинтеза и-РНК образуется достройка молекулы. На долю и-РНК приходится от 2 до 6% массовой доли всех РНК. В состав и-РНК входит 6 участков, каждый выполняет определенные функции.1) КЭП. Роль: стабилизация молекулы и-РНК. 2) Предцистронный участок. Роль: связывание с рибосомой за счет образования водородной связи. 3) Инициирующий участок. Роль: содержится «команда» о начале биосинтеза белка в рибосоме. 4) Цистронный участок. Роль: несет информацию о биосинтезе белка. 5) Обрывающийся триплет. Роль: Содержится «команда» о прекращении биосинтеза белка.6) Постцистронный участок. Роль: Регулирование количества синтезируемого белка.

р – РНК (рибосомная) Являются основным структурным компонентом рибосом. На долю р-РНК приходится до 75% от общей массы РНК. Взаимодействуя с белками (гистонами) р-РНК образует субъединицы рибосом. Рибосомы состоят из большой и малой субъединиц.

углеводы функции виды В начало
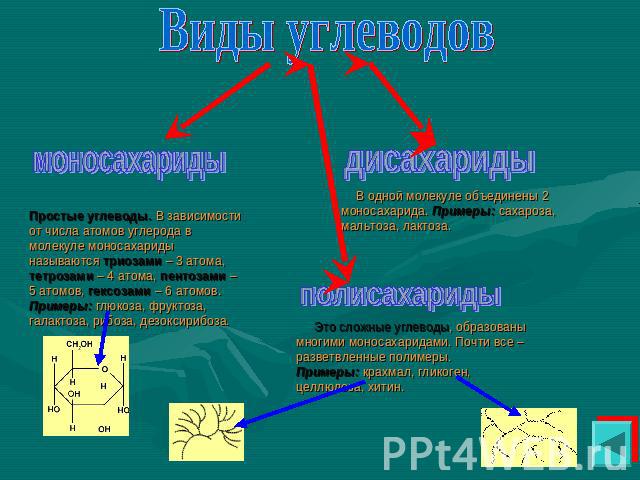
Виды углеводов моносахариды дисахариды Простые углеводы. В зависимости от числа атомов углерода в молекуле моносахариды называются триозами – 3 атома, тетрозами – 4 атома, пентозами – 5 атомов, гексозами – 6 атомов. Примеры: глюкоза, фруктоза, галактоза, рибоза, дезоксирибоза. полисахариды Это сложные углеводы, образованы многими моносахаридами. Почти все – разветвленные полимеры. Примеры: крахмал, гликоген, целлюлоза, хитин.

Функции углеводов 1) Основная функция – энергетическая. При расщеплении и окислении выделяется энергия, которая обеспечивает жизнедеятельность организма. В процессе окисления 1 г углевода освобождается 17,6 кДж энергии. 2) строительная функция. Целлюлоза входит в состав стенки растительных клеток; сложный полисахарид хитин - главный структурный компонент наружного скелета членистоногих. Строительную функцию хитин выполняет и у грибов. Крахмал – запасное питательное вещество у растений. Гликоген образуется из избытка глюкозы в крови. И т.д.

липиды Липиды присутствуют во всех без исключения клетках, выполняя специфические биологические функции. Жиры – наиболее простые и широко распространенные липиды. Липиды представляют собой соединение, состоящее из:1) высокомолекулярных жирных кислот 2) трехатомного спирта - глицеринаЖиры не растворяются в воде, они гидрофобны. В клетках есть и другие сложные гидрофобные жироподобные вещество – липоиды. Функции: 1) запасающая. У позвоночных животных примерно половина энергии, потребляемой клетками в состоянии покоя , образуется за счет окисления жиров. 2) энергетическая. В ходе расщепления 1 г жиров до СО2 и Н2О освобождается большое количество энергии – 38,9 кДж.3) теплоизоляция. У некоторых животных (тюлени, киты) он откладывается в подкожной жировой ткани, которая у китов образует слой толщиной до 1 м.4) регуляторная. Многие гормоны (например, коры надпочечников, половые) являются производными липидов.