Презентация на тему: Алкены

АлкеныСnH2n Цель урока: рассмотреть получение алкенов, химические свойства на основе их строения и применение алкенов.

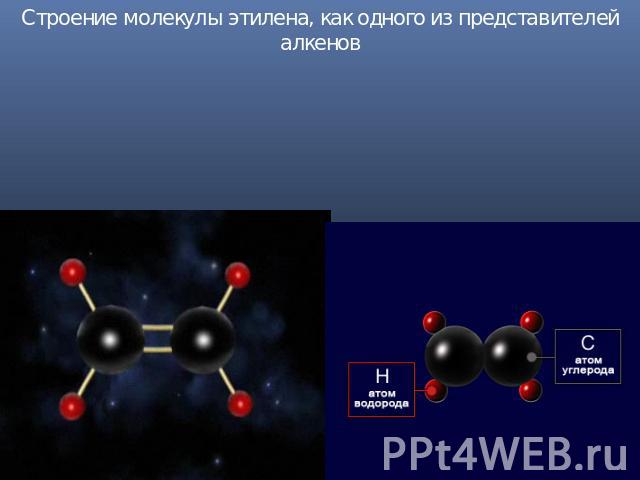
Строение молекулы этилена, как одного из представителей алкенов
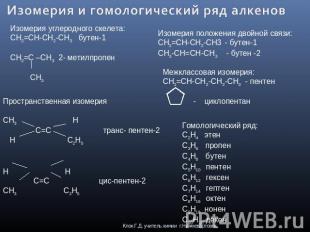
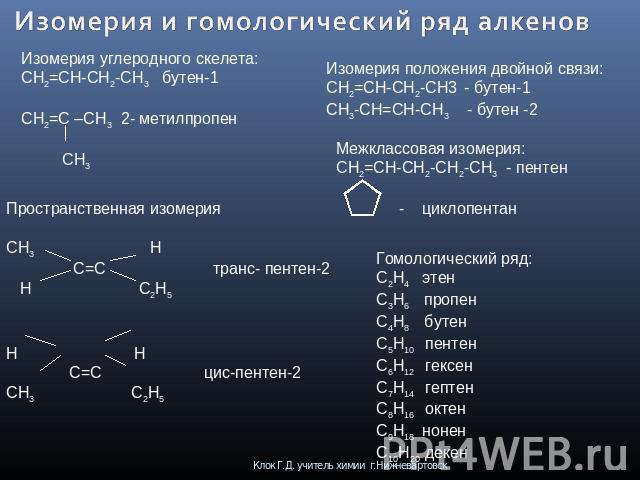
Изомерия и гомологический ряд алкенов Изомерия углеродного скелета:CH2=CH-CH2-CH3 бутен-1CH2=C –CH3 2- метилпропен CH3 Пространственная изомерияCH3 H C=C транс- пентен-2 H C2H5 H H C=C цис-пентен-2CH3 C2H5 Изомерия положения двойной связи:CH2=CH-CH2-CH3 - бутен-1CH3-CH=CH-CH3 - бутен -2 Межклассовая изомерия:CH2=CH-CH2-CH2-CH3 - пентен - циклопентан Гомологический ряд:C2H4 этенC3H6 пропенC4H8 бутенC5H10 пентенC6H12 гексенC7H14 гептенC8H16 октенC9H18 ноненC10H20 декен

Получение алкенов ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД Ni, t=500C Н3С - СН3 → Н2С = СН2 + Н2 этан этен (этилен) (-CH2-CH2-)n →t n CH2=CH2 полиэтилен (мономер) (полимер)

ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕ tН2С – СН2 + Zn → Н2С = СН2 + ZnBr2 Br Br 1,2-дибромэтан (этилен) ДЕГИДРАТАЦИЯ СПИРТОВСПИРТ → АЛКЕН + ВОДА Н Н Н2SO4(конц.) t≥140C, Н-С – С-Н → Н2С = СН2 + Н2О Н ОН этилен

ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ спиртовой H H раствор Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O Н Cl этен хлорэтан (этилен)

Качественные реакции на этилен

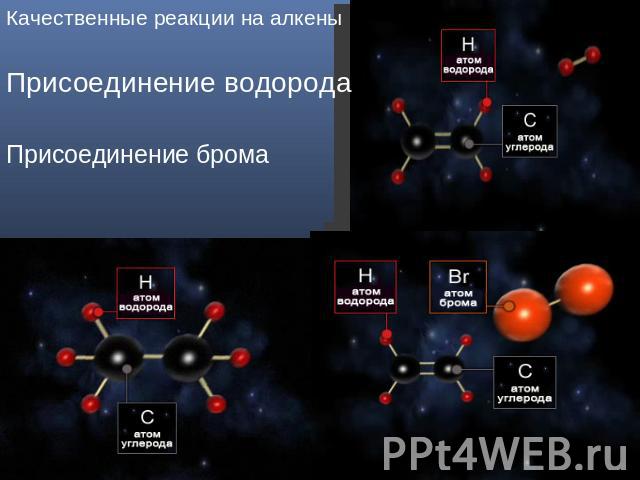
Качественные реакции на алкены Присоединение водорода Присоединение брома
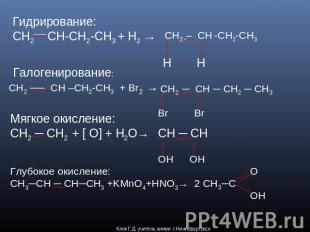
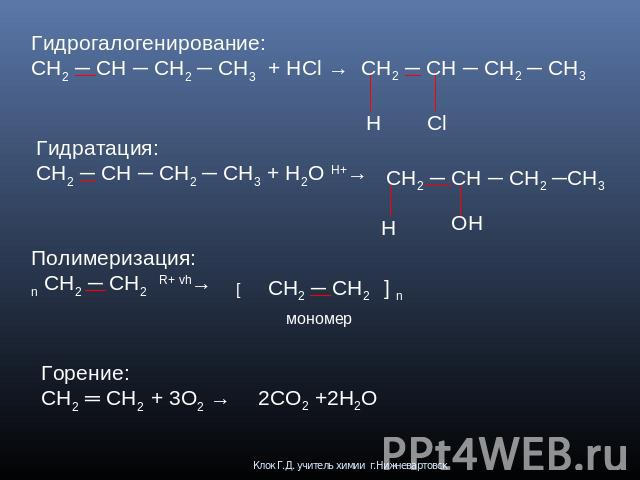
Гидрирование: CH2 CH-CH2-CH3 + H2 → Галогенирование: CH2 ── CH –CH2-CH3 + Br2 → Мягкое окисление:CH2 ─ CH2 + [ O] + H2O→ Глубокое окисление:CH3─CH ─ CH─CH3 +KMnO4+HNO3→ CH2 – CH -CH2-CH3
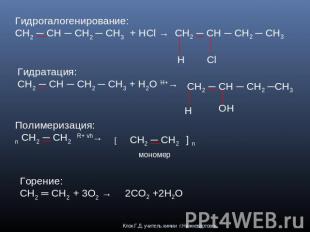
Гидрогалогенирование:CH2 ─ CH ─ CH2 ─ CH3 + HCl → CH2 ─ CH ─ CH2 ─ CH3 Гидратация:CH2 ─ CH ─ CH2 ─ CH3 + H2O H+→ CH2 ─ CH ─ CH2 ─CH3

применение

Проверочная работа 1.Какие вещества, формулы которых приведены ниже относятся к: а) алканам б) алкенамС6Н14 С5Н8 С4Н10 С5Н10 С3Н8 С2Н2 С2Н4 С6Н6 С7Н14 2.Сколько веществ изображено? 3.Назовите вещества по систематической номенклатуре. Определите среди них гомологи и изомеры. Н Н Н СН2=СН а) НССН=СНСН б) СН3СН – СНСН3 в) НСН - СН3 Н Н Н г) СН2СН2 д) СН= СН СН3 СН3 Н3С СН3

Закончите уравнения реакций CH2=CH–CH3 + HCl → CH3─ CHCl ─ CH3CH3–CH=CH–CH3 + H2 → CH3 ─ CH2 ─ CH2 ─ CH3 CH3–CH2–CH3 → H2 + CH3 ─ CH ═ CH2

Домашнее задание §12 упражнение 3-8

Список ресурсов: 1.Горковенко М.Ю. Поурочные разработки по химии 10 кл. М., «Вако» 20062. ЦОР «Подгруппа углерода . Органические соединения»3. www.uchportal.ru4. www. it-n.ru5. www.chemistry.ssu.samara.ru6. www.xumuk.ru/encyklopedia7.1september.ru






![Гидрирование: CH2 CH-CH2-CH3 + H2 → Галогенирование: CH2 ── CH –CH2-CH3 + Br2 → Мягкое окисление:CH2 ─ CH2 + [ O] + H2O→ Глубокое окисление:CH3─CH ─ CH─CH3 +KMnO4+HNO3→ CH2 – CH -CH2-CH3 Гидрирование: CH2 CH-CH2-CH3 + H2 → Галогенирование: CH2 ── CH –CH2-CH3 + Br2 → Мягкое окисление:CH2 ─ CH2 + [ O] + H2O→ Глубокое окисление:CH3─CH ─ CH─CH3 +KMnO4+HNO3→ CH2 – CH -CH2-CH3](/images/1413/43844/640/img8.jpg)