Презентация на тему: Алкены





Знать: Знать: Уметь:

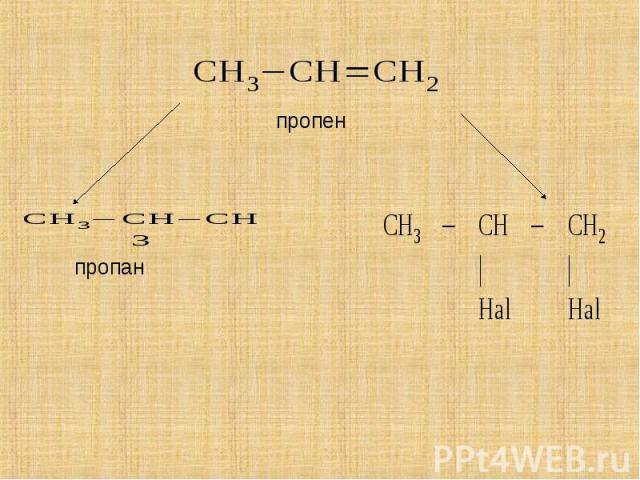
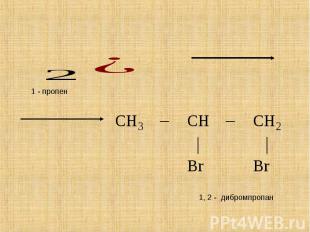
Присоединение водорода – гидрирование, образуются алканы. Присоединение водорода – гидрирование, образуются алканы. Присоединение галогенов (+F2, CL2, Br2, I2) – галогенирование, образуются дигалогеналкины.

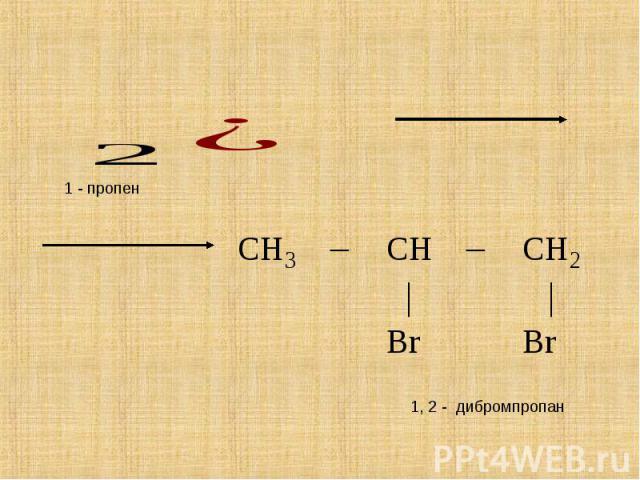
Качественно реакцией на все непредельные углеводороды, в том числе на алкены, является реакция с бромной водой. Бромная вода при взаимодействии с алкенами обесцвечивается. Качественно реакцией на все непредельные углеводороды, в том числе на алкены, является реакция с бромной водой. Бромная вода при взаимодействии с алкенами обесцвечивается.

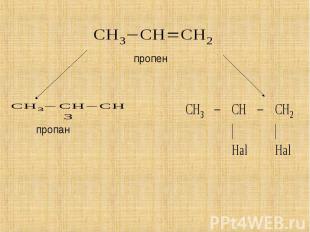
Присоединение галогеноводородов (+HHal) – гидрогалогенирование, образуются моногалогенфлканы (R-Hal). Присоединение галогеноводородов (+HHal) – гидрогалогенирование, образуются моногалогенфлканы (R-Hal). Присоединение воды (+H2O) – гидратация, образуются предельные одноатомные спирты (алканолы CnH2n+1OH).


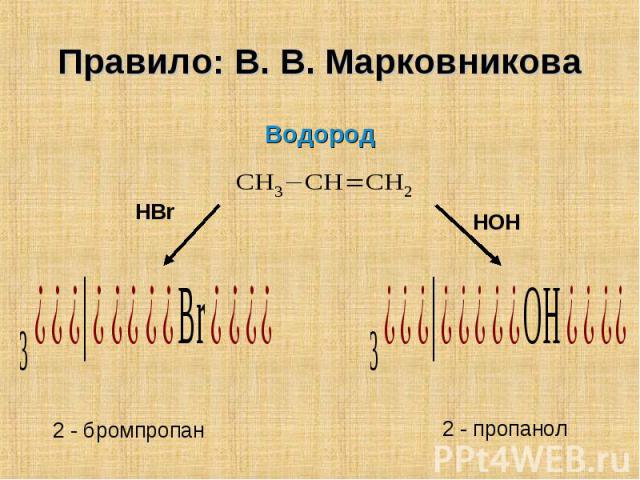
Атом водорода присоединяется к атому углерода у кратной связи, связанному с большим числом атомов водорода Атом водорода присоединяется к атому углерода у кратной связи, связанному с большим числом атомов водорода
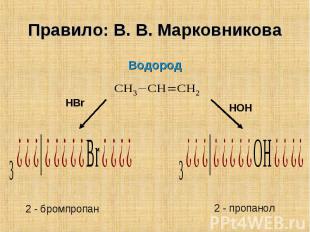
Водород Водород


В зависимости от условий непредельные углеводороды окисляются в различной степени. В зависимости от условий непредельные углеводороды окисляются в различной степени.

Полное (избыток О2) Полное (избыток О2) Неполное (недостаток О2)

Одной из наиболее характерных реакций окисления является взаимодействие непредельных углеводородов (УВ) с раствором перманганата калия (KMnO4)



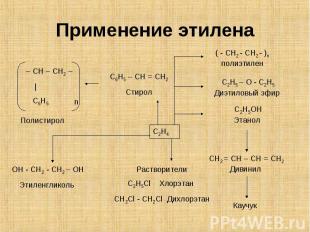
Процесс полимеризации алкенов открыт А М. Бутлеровым. Процесс полимеризации алкенов открыт А М. Бутлеровым. Полимеризацией называется процесс соединения одинаковых молекул (мономеров), протекающий за счет разрыва кратных связей, с образованием высокомолекулярного соединения (полимера).

Дегидрирование алканов (- Н2) Дегидрирование алканов (- Н2) Гидрирование алкинов (+ Н2) Дегидрирование спиртов (- H2O) Катализаторы: H2SO4, H3PO4, Al2O3, ZnCl2.

При дегидрировании спиртов атом водорода отщепляется от соседнего атома углерода, связанного с наименьшим числом атомов водорода (правила А. М. Зайцева): При дегидрировании спиртов атом водорода отщепляется от соседнего атома углерода, связанного с наименьшим числом атомов водорода (правила А. М. Зайцева):
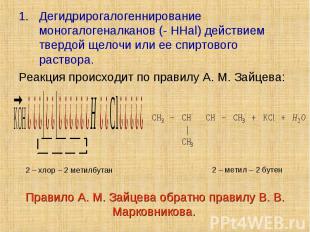
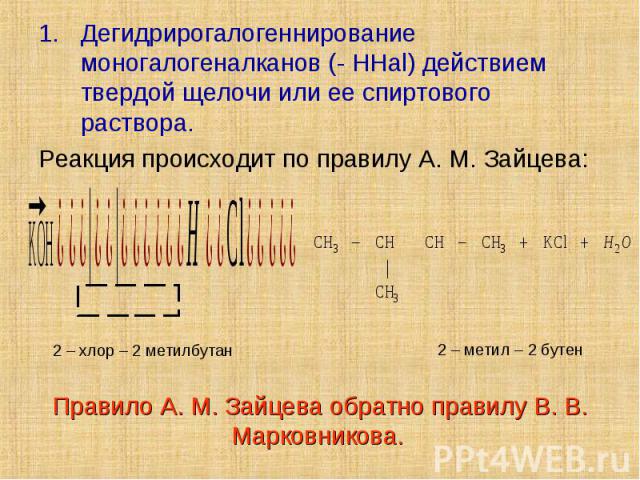
Дегидрирогалогеннирование моногалогеналканов (- HHal) действием твердой щелочи или ее спиртового раствора. Дегидрирогалогеннирование моногалогеналканов (- HHal) действием твердой щелочи или ее спиртового раствора. Реакция происходит по правилу А. М. Зайцева:

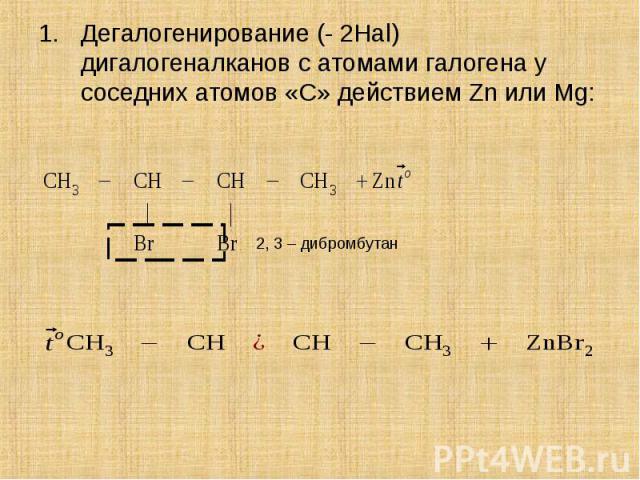
Дегалогенирование (- 2Hal) дигалогеналканов с атомами галогена у соседних атомов «С» действием Zn или Mg: Дегалогенирование (- 2Hal) дигалогеналканов с атомами галогена у соседних атомов «С» действием Zn или Mg: