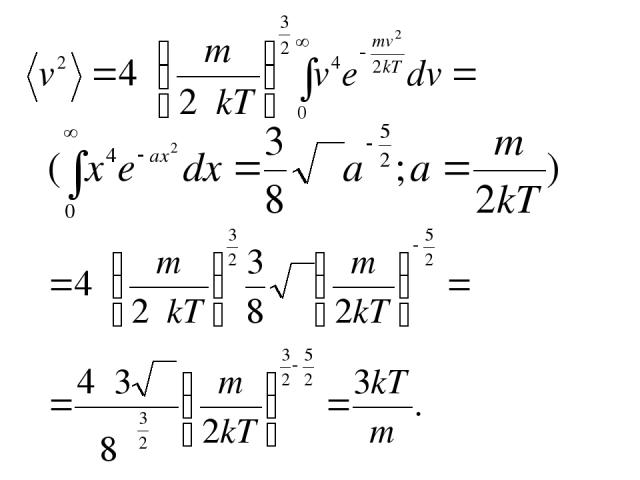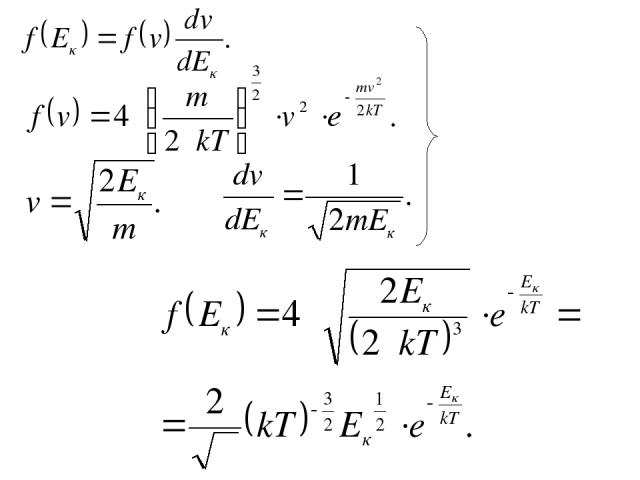Презентация на тему: Статистические распределения

Статистические распределения 900igr.net

Эргодическая гипотеза: среднее по ансамблю равно среднему по времени. Рассмотрим систему, состоящую из n тел, движущихся со скоростями v1, v2 … vn. Скорость средняя по ансамблю: где v1, v2 … vn измерены в один момент времени. Скорость средняя по времени: где v1, v2 … vn измерены для одной молекулы в разные моменты времени.

Распределение молекул по скоростям. (Распределение Максвелла) функция распределения – доля молекул, приходящаяся на единичный интервал скоростей вблизи некоторого значения v, т.е. в интервале Функция распределения – вероятность того, что скорость молекул лежит в единичном интервале вблизи некоторого значения v.
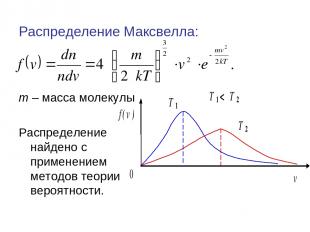
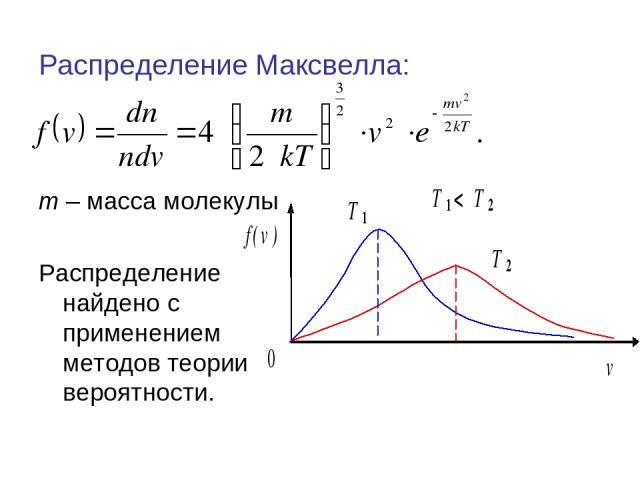
Распределение Максвелла: m – масса молекулы Распределение найдено с применением методов теории вероятности.
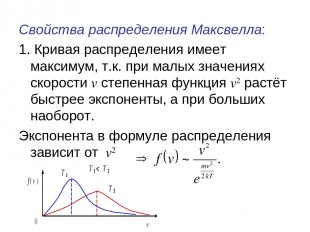
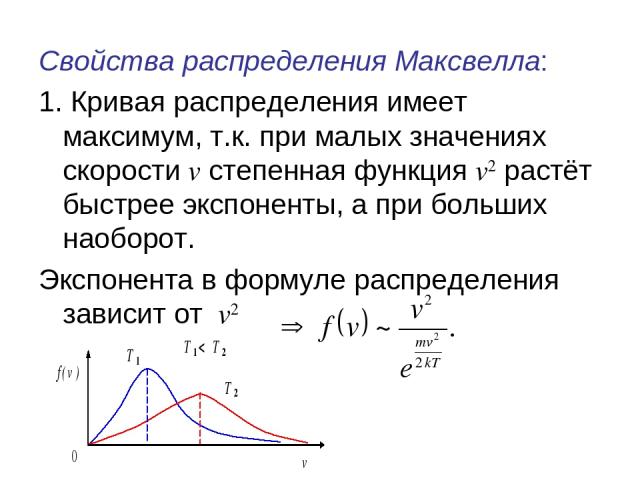
Свойства распределения Максвелла: 1. Кривая распределения имеет максимум, т.к. при малых значениях скорости v степенная функция v2 растёт быстрее экспоненты, а при больших наоборот. Экспонента в формуле распределения зависит от v2
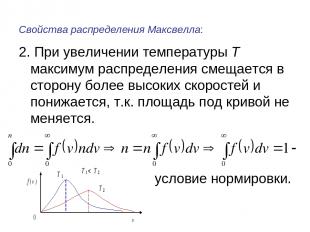
Свойства распределения Максвелла: 2. При увеличении температуры Т максимум распределения смещается в сторону более высоких скоростей и понижается, т.к. площадь под кривой не меняется. условие нормировки.

Свойства распределения Максвелла: 3. Доля молекул, приходящихся на единичный интервал скоростей вблизи v = 0 и v = ∞, равна нулю. Связано это с тем, что в соответствии с теорией вероятности молекулы при столкновении не могут либо только отдавать, либо только получать энергию.
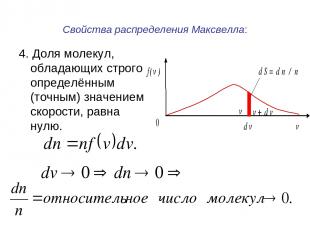
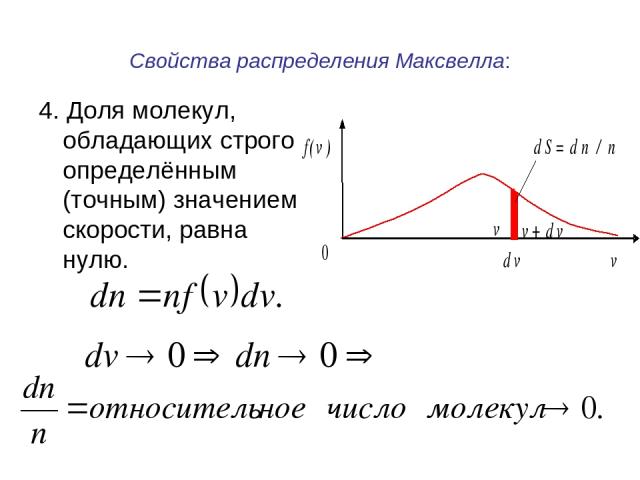
Свойства распределения Максвелла: 4. Доля молекул, обладающих строго определённым (точным) значением скорости, равна нулю.

Свойства распределения Максвелла: 5. Распределение Максвелла по скоростям справедливо для молекул не только идеального газа, но и для реального газа, жидкости, твёрдого тела. 6. Если систему молекул поместить в силовое поле, то это силовое поле не влияет на распределение молекул по скоростям.
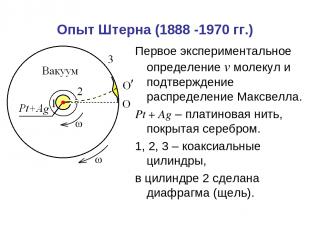
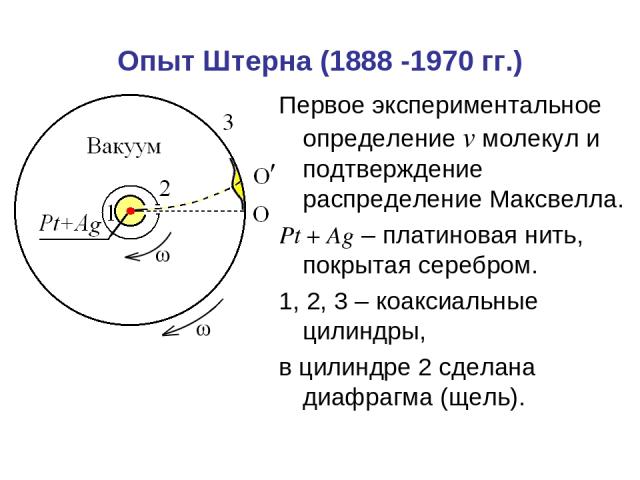
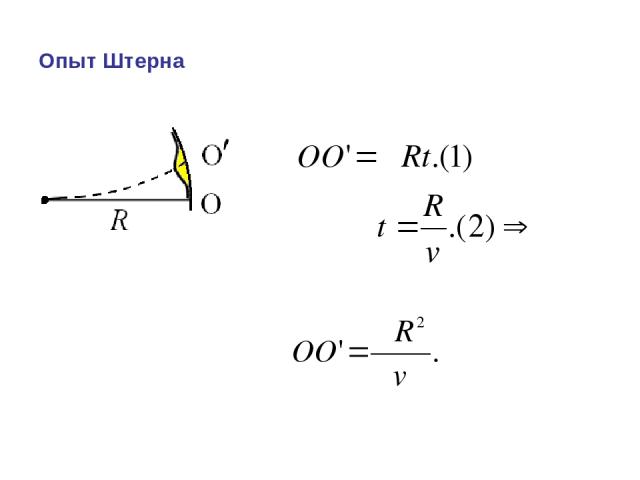
Опыт Штерна (1888 -1970 гг.) Первое экспериментальное определение v молекул и подтверждение распределение Максвелла. Pt + Ag – платиновая нить, покрытая серебром. 1, 2, 3 – коаксиальные цилиндры, в цилиндре 2 сделана диафрагма (щель).

Опыт Штерна Платиновая нить нагревается током до t ~ 12350 C, при этом атомы серебра испаряются и через щель в цилиндре 1 и диафрагму в цилиндре 2 попадают на внутреннюю поверхность цилиндра 3, давая изображение щели – полосу О. При вращении цилиндров 2 и 3 с одинаковой угловой скоростью ω атомы серебра оседают на некотором расстоянии от О, давая расплывчатое изображение щели. Толщина осаждённого слоя соответствует распределению Максвелла.
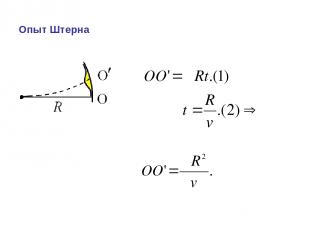
Опыт Штерна

Скорости газовых молекул Средняя скорость (средняя арифметическая скорость). в интервале от v до v + dv. Сумма всех скоростей:

Скорости газовых молекул Средняя скорость:

Скорости газовых молекул 2. Средняя квадратичная скорость.
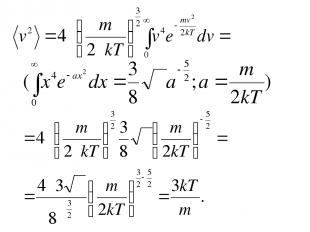

Средняя квадратичная скорость.
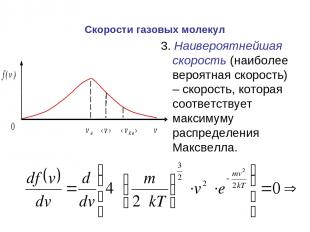
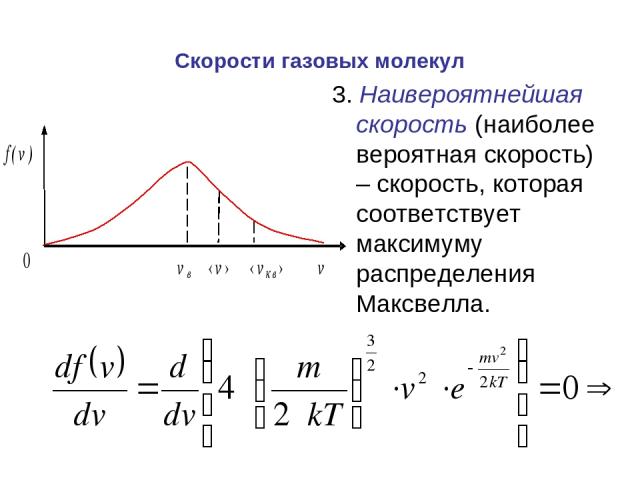
Скорости газовых молекул 3. Наивероятнейшая скорость (наиболее вероятная скорость) – скорость, которая соответствует максимуму распределения Максвелла.

3. Наивероятнейшая скорость
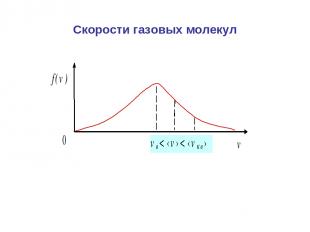
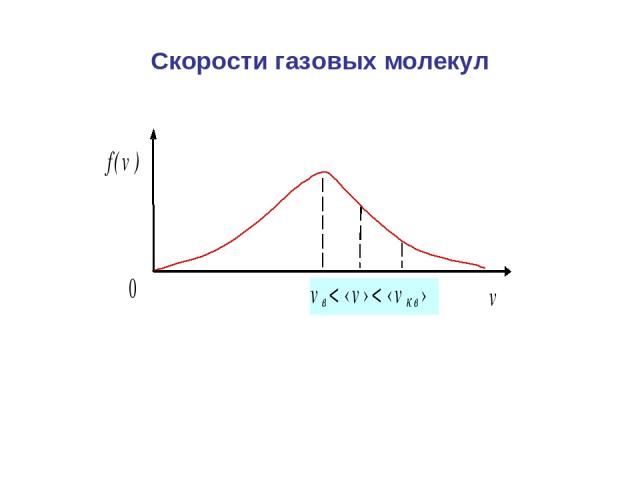
Скорости газовых молекул

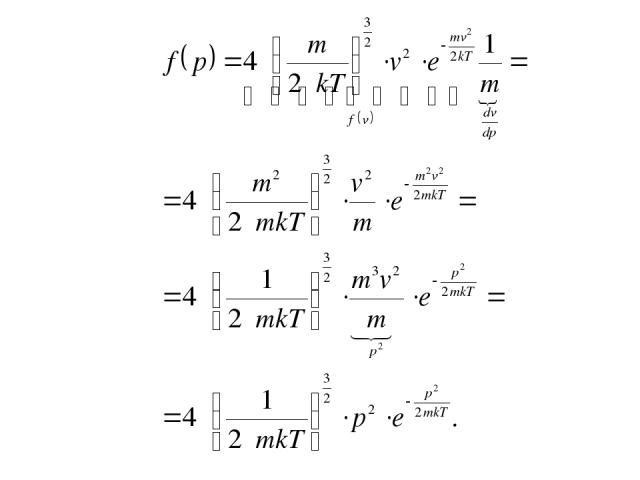
Распределение молекул по импульсам и кинетическим энергиям

Распределение молекул по импульсам и кинетическим энергиям Делаем замену переменных:


Распределение молекул по импульсам и кинетическим энергиям
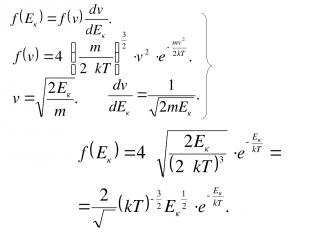

Распределение молекул по потенциальным энергиям (Распределение Больцмана)
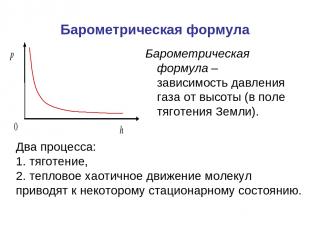
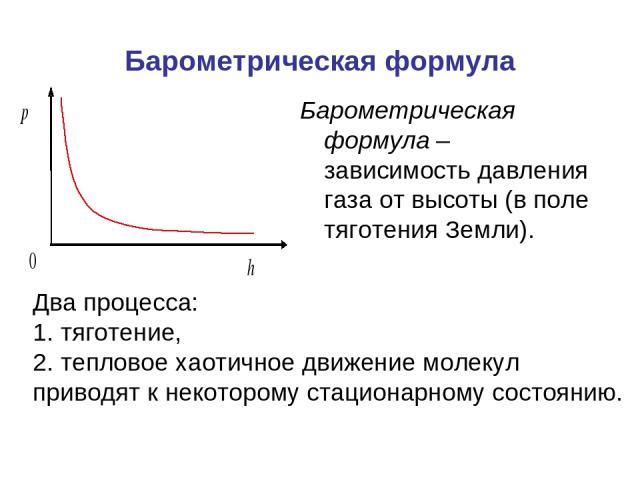
Барометрическая формула Барометрическая формула – зависимость давления газа от высоты (в поле тяготения Земли). Два процесса: 1. тяготение, 2. тепловое хаотичное движение молекул приводят к некоторому стационарному состоянию.

Барометрическая формула Предположим: 1) идеальный газ, m = const, 2) поле тяготения однородно, g = const, 3) T = const. сила давления столба воздуха высотой dh сечением S. m – масса молекулы. n – концентрация молекул.

Барометрическая формула Знак «–» отражает то, что с увеличением h давление p падает.

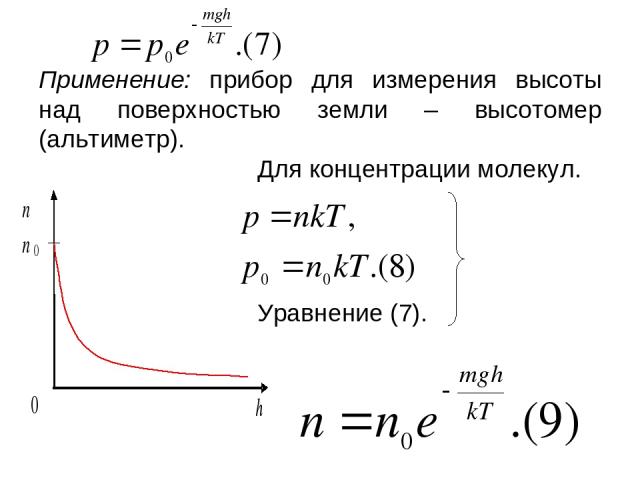
Применение: прибор для измерения высоты над поверхностью земли – высотомер (альтиметр). Для концентрации молекул. Уравнение (7).

Распределение молекул по потенциальным энергиям (Распределение Больцмана) потенциальная энергия в поле тяготения. распределение Больцмана. Больцман показал, что распределение такого вида справедливо для любого внешнего поля. n0 – концентрация молекул с нулевой потенциальной энергией U = 0.
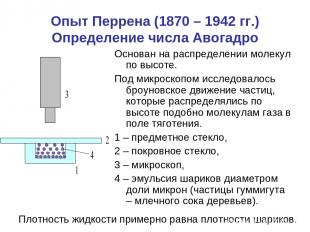
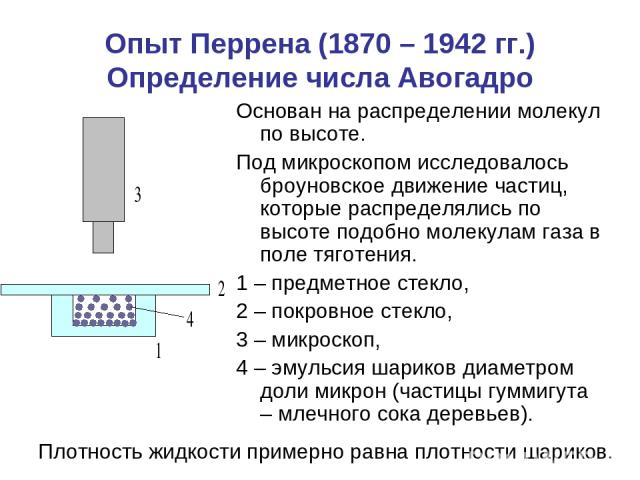
Опыт Перрена (1870 – 1942 гг.) Определение числа Авогадро Основан на распределении молекул по высоте. Под микроскопом исследовалось броуновское движение частиц, которые распределялись по высоте подобно молекулам газа в поле тяготения. 1 – предметное стекло, 2 – покровное стекло, 3 – микроскоп, 4 – эмульсия шариков диаметром доли микрон (частицы гуммигута – млечного сока деревьев). Плотность жидкости примерно равна плотности шариков.

Опыт Перрена m – масса шарика, mж – масса объёма жидкости, вытесненной шариком.

Опыт Перрена. Определение числа Авогадро Получил Точное значение:
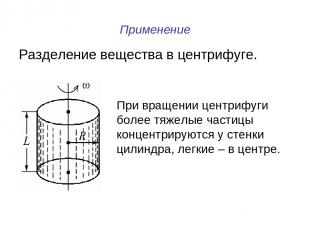
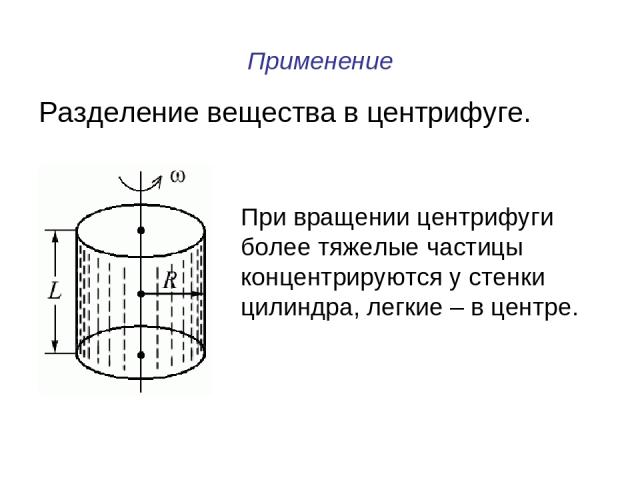
Применение Разделение вещества в центрифуге. При вращении центрифуги более тяжелые частицы концентрируются у стенки цилиндра, легкие – в центре.

Закон равномерного распределения энергии по степеням свободы Степени свободы – число независимых координат, определяющих положение и конфигурацию системы в пространстве.

1. Одноатомный газ имеет три степени свободы, т.к. может двигаться в 3-х направлениях. Следовательно, обладает 3 поступательными степенями свободы. Молекула –материальная точка. Энергии вращательного движения нет
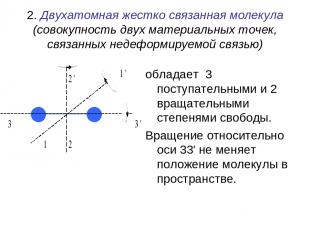
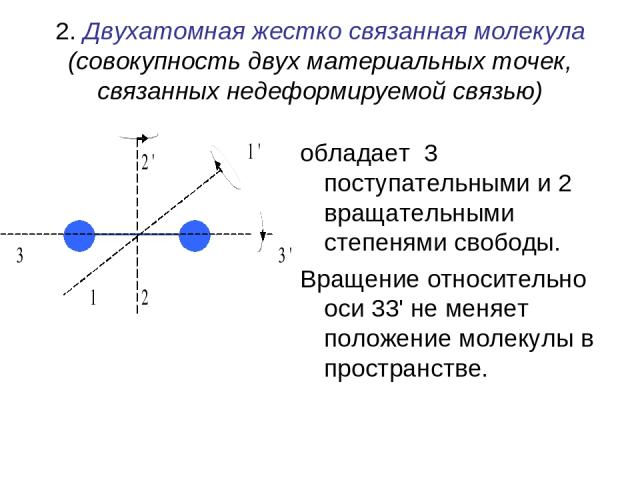
2. Двухатомная жестко связанная молекула (совокупность двух материальных точек, связанных недеформируемой связью) обладает 3 поступательными и 2 вращательными степенями свободы. Вращение относительно оси 33' не меняет положение молекулы в пространстве.
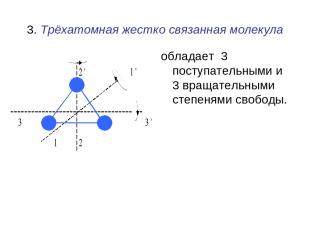
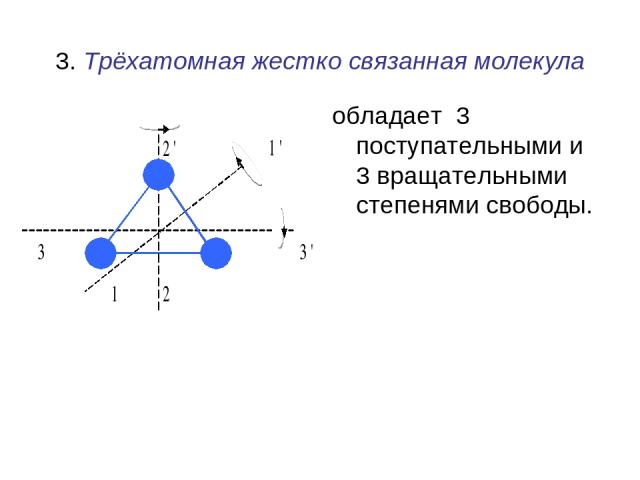
3. Трёхатомная жестко связанная молекула обладает 3 поступательными и 3 вращательными степенями свободы.

Закон равномерного распределения энергии по степеням свободы (закон Больцмана): если система частиц находится в состоянии термодинамического равновесия, то средняя кинетическая энергия хаотического движения молекул, приходящаяся на 1 степень свободы поступательного и вращательного движения, равна Для реальных молекул, не обладающих жёсткими связями между молекулами, необходимо учитывать также степени свободы колебательного движения.

На колебательную степень свободы приходится не только кинетическая энергия, но и потенциальная, причём среднее значение кинетической энергии равно среднему значению потенциальной энергии и равно Следовательно, средняя суммарная энергия молекулы: i = iпоступат. + iвращат. + 2iколеб.

В идеальном газе взаимная потенциальная энергия молекул , т.к. молекулы между собой не взаимодействуют, то рассматривается только кинетическая энергия, и • для 1 моля газа внутренняя энергия равна сумме кинетических энергии NA молекул: • Для произвольной массы m газа: υ – количество вещества.