Презентация на тему: Углекислый газ


Строение молекулы Молекула СО2 линейная, длина двойной связи С=О равна 0,116 нм. В рамках теории гибридизации атомных орбиталей две σ-связи образованы sp-гибридными орбиталями атома углерода и 2р-орбиталями атома кислорода. Не участвующие в гибридизации р-орбитали углерода образуют с аналогичными орбиталями кислорода p-связи. Молекула неполярная.

Оксид углерода (IV) – углекислый газ, газ без цвета и запаха, тяжелее воздуха, растворим в воде, при сильном охлаждении кристаллизуется в виде белой снегообразной массы – «сухого льда». При атмосферном давлении он не плавится, а испаряется, температура сублимации -78 °С. Углекислый газ образуется при гниении и горении органических веществ. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Мало растворим в воде (1 объем углекислого газа в одном объеме воды при 15 °С).

Химические свойства Химически оксид углерода инертен. 1. Окислительные свойства С сильными восстановителями при высоких температурах проявляет окислительные свойства. Углем восстанавливается до угарного газа: С + СО2 = 2СО. Магний, зажженный на воздухе, продолжает гореть и в атмосфере углекислого газа: 2Mg + CO2 = 2MgO + C.

Химические свойства 2. Свойства кислотного оксида Типичный кислотный оксид. Реагирует с основными оксидами и основаниями, образуя соли угольной кислоты: Na2O + CO2 = Na2CO3, 2NaOH + CO2 = Na2CO3 + H2O, NaOH + CO2 = NaHCO3.

Химические свойства 3. Качественна реакция Качественной реакцией для обнаружения углекислого газа является помутнение известковой воды: Ca(OH)2 + CO2 = CaCO3↓ + H2O. В начале реакции образуется белый осадок, который исчезает при длительном пропускании CO2 через известковую воду, т.к. нерастворимый карбонат кальция переходит в растворимый гидрокарбонат: CaCO3 + H2O + CO2 = Сa(HCO3)2.

В промышленности – побочный продукт при производстве извести. В лаборатории при взаимодействии кислот с мелом или мрамором. При сгорании углеродсодержащих веществ. При медленном окислении в биохимических процессах (дыхание, гниение, брожение). Получение
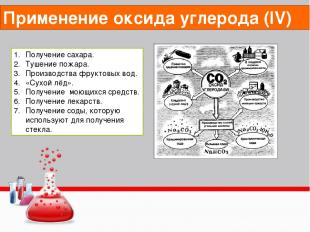
Получение сахара. Тушение пожара. Производства фруктовых вод. «Сухой лёд». Получение моющихся средств. Получение лекарств. Получение соды, которую используют для получения стекла. Применение оксида углерода (IV)

Горение связано с появлением дыма. Дым бывает белым, черным, а иногда – невидимый. Над горячей свечой или спиртовкой поднимается такой «невидимый» дым, называемый углекислым газом. Чистую пробирку подержи над свечей и улови немного «невидимого» дыма. Чтобы он не улетел, быстро закрой пробирку пробкой без отверстия. Углекислый газ будет невидим и в пробирке. Сохрани эту пробирку с углекислым газом для дальнейших опытов. Мы ловим дым

Налей немного известковой воды (чтобы покрыть дно) в ту пробирку, в которую ты уловил углекислый газ от пламени свечи. Закрой пробирку пальцем и встряхни ее. Прозрачная известковая вода стала совсем мутной. В этом виноват только углекислый газ. Если возьмёшь известковой воды в пробирку, в которой не было углекислого газа, и встряхнешь пробирку, то вода останется прозрачной. Значит, помутнение известковой воды является доказательством того, что в пробирке был углекислый газ.

Возьми немного порошка соды и подогрей его в горизонтальной укреплённой пробирке. Эту пробирку соедини коленчатой трубкой с другой пробиркой, в которой находится вода. Из трубки начнут появляться пузырьки. Следовательно, из соды в воду поступает какой то газ. Не следует допускать, чтобы стеклянная трубка была опущена в воду после окончания нагрева, иначе вода поднимется по трубке и попадет в горячую пробирку с содой. От этого пробирка может лопнуть. После того, кок ты увидишь, что из соды при нагревании выделяется газ, попробуй заменить простую воду в пробирке известковой водой. Она станет мутной. Из соды выделяется углекислый газ.

Если ты откроешь бутылку с лимонадом или же начнешь её взбалтывать, то в ней появится множество газовых пузырьков. Закрой бутылку с лимонадом пробкой, в которую вставлена стеклянная трубка, и опусти длинный конец трубки в пробирку с известковой водой. Вскоре вода станет мутной. Значит, лимонный газ – это углекислый газ. Он образуется из содержащей в лимонаде угольной кислоты.

Углекислый газ содержит в ряде веществ, но определить его на глаза невозможно. Если ты польёшь уксусом кусочек соды, то уксус сильно зашипит и при этом из соды выделится какой то газ. Если ты положишь кусочек соды в пробирку, нальёшь в нее немного уксуса, закроешь пробкой с коленчатой трубкой и опустишь длинный конец трубки в известковую воду, то убедишься, что из соды так же выделяется углекислый газ.

Даже слабая кислота выгоняет из соды углекислый газ. Покрой дно пробирки лимонной кислотой и насыпь поверху нее столько же соды. Смешай эти два вещества. Оба они уживаются, но ненадолго. Высыпь эту смесь в обыкновенный стакан и быстро наполни его свежей водой. Как сильно она шипит и пенится! Как настоящий лимонад. Ты спокойно можешь отпить его. Это абсолютно безвредно, даже вкусно. Надо только в самом начале добавить сахар, просто чтобы было вкуснее.

Углекислый газ в напитках увеличивает их освежающее действие. Ты можешь в любое время приготовить пенящийся лимон. Для этого надо в пробирке смешать 2 кубических сантиметра порошка лимонной кислоты, 2 кубических сантиметра соды и 6 кубических сантиметра истолченного в порошок сахара. Эти три вещества надо тщательно перемешать, встряхивая, и высыпая на большой лист бумаги. Это количество надо разделить на равные порции. Каждая порция должна быть такой величины, чтобы её можно было покрыть круглое дно пробирки. Каждую порцию заверни в отдельную бумажку, как заворачивают порошки в аптеке. Из одного такого пакетика можно получить стакан освежающего лимонада.

Если при смачивании какого – либо вещества кислотой появляется пена, почти всегда это происходит от выделяющего углекислого газа. Именно он и образует эту пену. Смоченный известняк шипит и пенится, из него выделяется углекислый газ. Если ты не уверен в этом, сделай опыт: положи кусочек известняка в пробирку и подлей кислоты, затем закрой пробирку пробкой со стеклянной трубкой и опусти длинный конец этой трубки в известковую воду. Вода помутнеет. Существует несколько видов извести. Известняк – это углекислый кальций.

Согретый углекислый газ, или дым, легок и свободно поднимается в воздух, холодный углекислый газ тяжёл, оседает на дно сосуда и наполняет его постепенно до краёв. В углекислом газе горение невозможно, так как он сам является продуктом горения. Если ты поставишь свечу на дно какого – нибудь сосуда и некоторое время понаблюдаешь за ней, то увидишь, что пламя вскоре погаснет. Углекислый газ, преобразовавшийся при горении свечи, постепенно наполнить сосуд до краёв, и пламя «утонет» в углекислом газе.





























