Презентация на тему: Количество вещества, моль

8 класс Количественные измерения в химии. Количество вещества. Моль Покровская Наталия Васильевна, учитель химии ГОУ СОШ №939 г.Москва

Ведь он принесёт тебе ЗНАНИЯ!

Тема урока: Количественные измерения в химии. Количество вещества. Моль.

Цель урока: Научиться рассчитывать по формулам массу вещества, количество вещества

Задачи урока: Образовательная: сформировать понятие о количестве вещества, единицах его измерения, о взаимосвязи физико-химических величин (массы, количества вещества и числа молекул). Развивающая: развить умение решения задач с использованием формул. Воспитательная: прививать нормы социальной жизни, воспитывать умение работать в группе.

Какие физические величины можно использовать для определения меры веществ? В каких единицах измеряются эти физические величины?

кг Л Л М

=158,988 л 1 карат = 0,2 г 1 баррель нефти

Порции

? Можно ли найти число частиц в порции вещества?

Моль от французского слова «moles»- множество 1 Моль – это количество вещества, в котором содержится 6,02 ∙1023 частиц Test - null

Число всех песчинок в пустыне Сахара = 3 моль!!!


Число частиц в одном моль вещества называется числом Авогадро (NА) NА = 6,02 ∙1023 1/моль

Н2О Число Авогадро больше числа всех капель воды на Земле

Обозначение: ν (ню), или n Единица измерения: моль Количество вещества
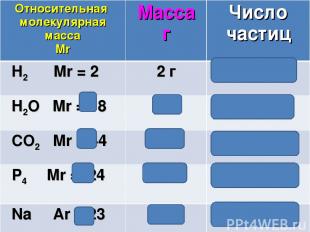
Относительная молекулярная масса Mr Масса г Число частиц H2 Mr = 2 2 г 6,02 ∙1023 H2O Mr = 18 18 г 6,02 ∙1023 CO2 Mr = 44 44 г 6,02 ∙1023 P4 Mr =124 124 г 6,02 ∙1023 Na Аr = 23 23 г 6,02 ∙1023

1 моль вещества – 6,02∙1023частиц Сколько частиц содержат 3 моль вещества? Сколько частиц содержат 0,5 моль вещества? 3 ∙ 6,02∙1023 = 18,06∙1023 0,5 ∙ 6,02∙1023 = 3,01∙1023

В общем виде: N = ν ∙ NA N – число частиц ν – количество вещества NA – число Авогадро
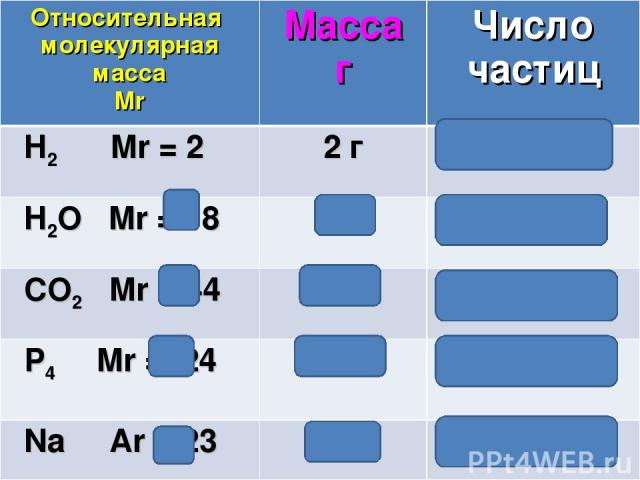
![[ Mr = M ] Mr(H2O)= 18 M(H2O)= 18 г/моль Молярная масса (М) – это суммарная масс [ Mr = M ] Mr(H2O)= 18 M(H2O)= 18 г/моль Молярная масса (М) – это суммарная масс](https://fs3.ppt4web.ru/images/132013/170801/310/img19.jpg)
[ Mr = M ] Mr(H2O)= 18 M(H2O)= 18 г/моль Молярная масса (М) – это суммарная масса всех частиц, входящих в 1 моль вещества.

Можно ли найти массу, зная количество вещества?

ν = m/M m = ν ∙ M

Что тяжелее: 1 моль атомов кислорода или 1 моль атомов фосфора? Почему? M(O) = 16 г/моль M(P) = 31 г/моль

Задача. Найти массу 3 моль атомов серы Дано ν (S) = 3моль M(S) = 32 г/моль Найти m(S) Решение m = ν ∙ M m = 3 ∙ 32 = 96 (г) Ответ: m(S) = 96 г

Равные массы, но разные объемы, потому что .... m = V∙ ρ

1 моль любого газа (н.у.) занимает объем 22,4 л VM = 22,4л/моль

ν = V/Vm V = ν ∙ Vm
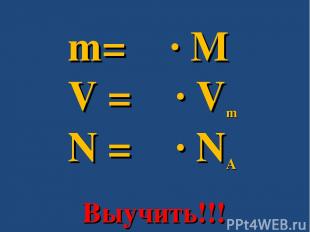
m= ν ∙ M V = ν ∙ Vm N = ν ∙ NA Выучить!!!

Сколько ложек сахарного песка вы кладете в чашку чая? Рассчитайте: какое количество сахарозы вы выпиваете с чаем; 2) сколько молекул сахарозы (C12H22O11) содержится в этом количестве, если в 1 чайной ложке примерно 5 г сахарозы.

Цель достигнута? Спасибо за урок!

Домашнее задание: по учебнику § 15 № 3, § 16



















![[ Mr = M ] Mr(H2O)= 18 M(H2O)= 18 г/моль Молярная масса (М) – это суммарная масса всех частиц, входящих в 1 моль вещества. [ Mr = M ] Mr(H2O)= 18 M(H2O)= 18 г/моль Молярная масса (М) – это суммарная масса всех частиц, входящих в 1 моль вещества.](https://fs3.ppt4web.ru/images/132013/170801/640/img19.jpg)