Презентация на тему: Состояние электронов в атоме

Состояние электронов в атоме Тверских О.И.,учитель химии

1924 год Франция Луи де Бройль (Луи Виктор Пьер Реймон, 7-й герцог Брольи) (1892-1987) Лауреат нобелевской премии (1929)Электрон обладает двойственными корпускулярно-волновыми свойствами (как свет), то есть проявляет одновременно свойства частицы и волны.

1927 год США Клинтон Дж. Дэвиссон (1881-1958) Лауреат нобелевской премии по физике(1937) Лестер Г. Джермер (1896-1971) Англия Джозеф Паджет Томсон (1892-1975) Экспериментально доказали утверждение Луи де Бройля

1924 год Германия Вернер Карл Гейзенберг (1901-1976) Лауреат нобелевской премии по физике (1932).Принцип неопределенности::Невозможно в один и тот же момент времени точно определить местонахождение электрона в пространстве и его скорость.

1926 годАвстрия Эрвин Шредингер (1887-1961) Лауреат нобелевской премии по физике (1933) Уравнение Шредингера
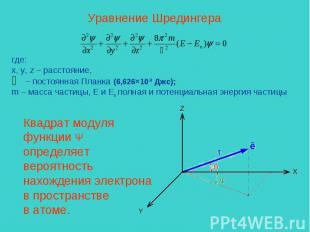
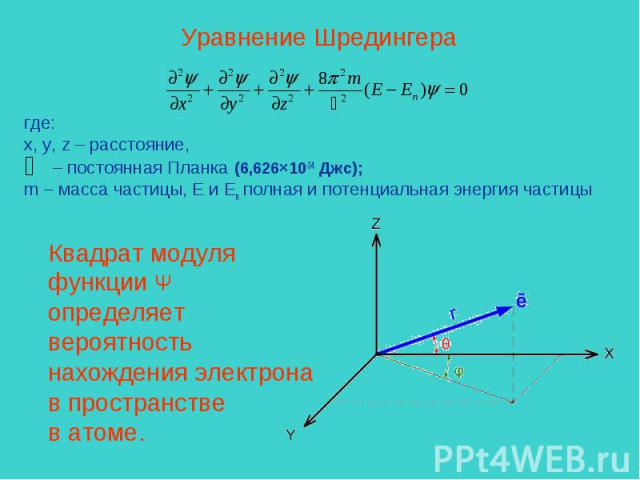
Уравнение Шредингера где: x, y, z – расстояние, – постоянная Планка (6,626×10-34 Дж.с); m – масса частицы, E и Eп полная и потенциальная энергия частицыКвадрат модуляфункции Ψопределяет вероятность нахождения электрона в пространстве в атоме.

Функция Ψ зависит от пространственныхкоординат электрона(радиуса и двух углов)и определяется набором квантовых чисел: n, l, m, s

Квантовые числа

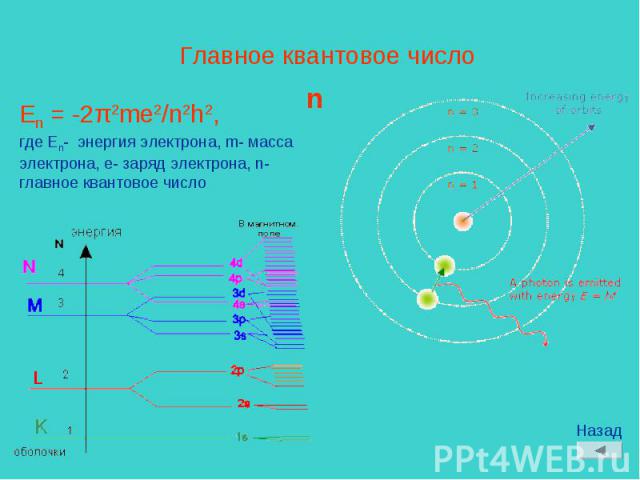
Главное квантовое числоn En = -2π2me2/n2h2,где En- энергия электрона, m- масса электрона, e- заряд электрона, n- главное квантовое число
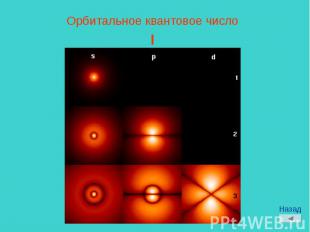
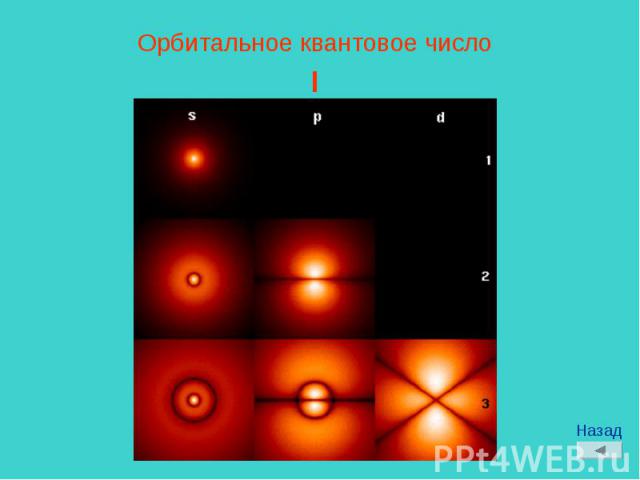
Орбитальное квантовое числоl
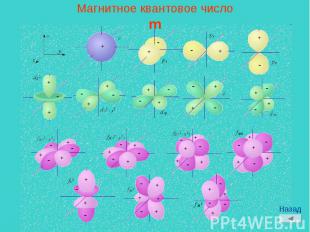
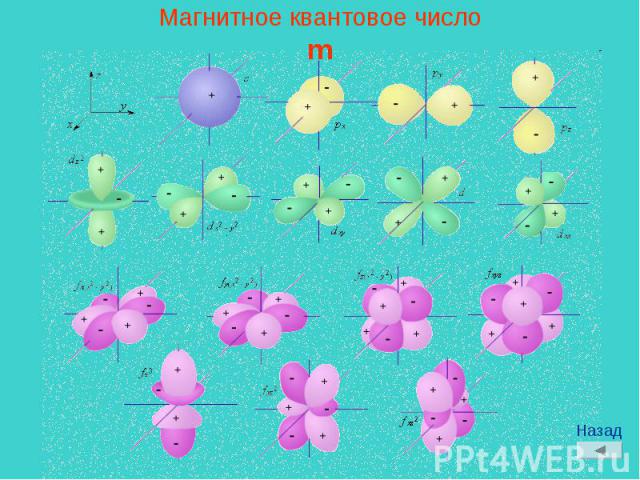
Магнитное квантовое числоm
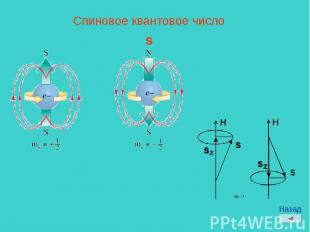
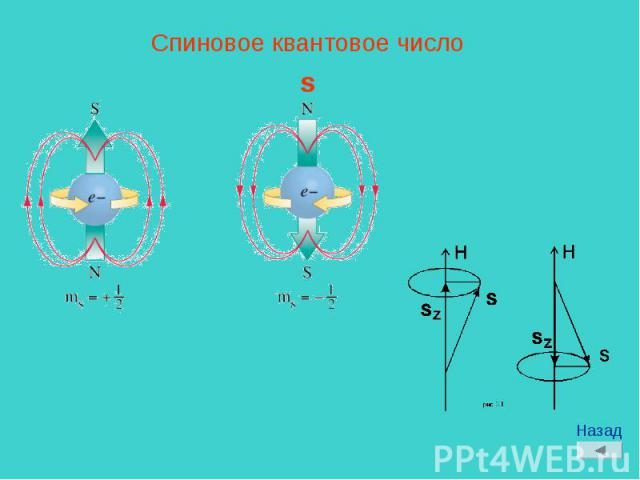
Спиновое квантовое числоs
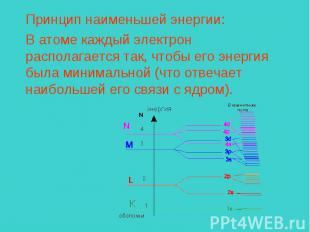
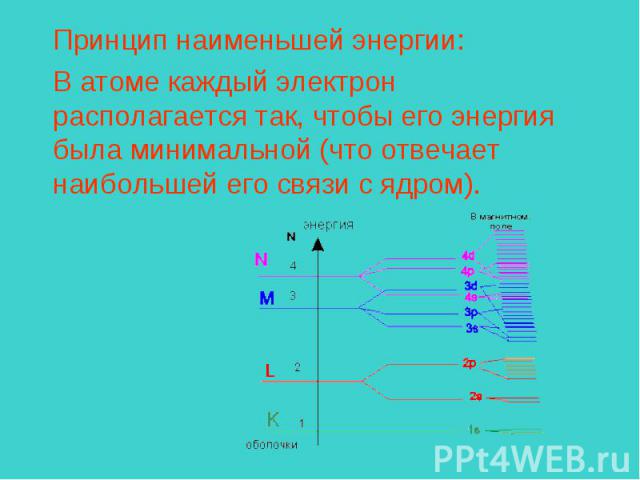
Принцип наименьшей энергии:В атоме каждый электрон располагается так, чтобы его энергия была минимальной (что отвечает наибольшей его связи с ядром).

1961 Клечковский Всеволод Маврикиевич (1900 -1972) РоссияПравило Клечковского:Электрон занимает в основном состоянии уровень не с минимально возможным значением n, а с наименьшим значением суммы n + l.

1940Вольфганг Эрнст Паули (1900 – 1958)Австрия Лауреат нобелевской премии (1945) Принцип Паули: В атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы.

Фридрих Хунд(1896 – 1997)ГерманияПравило Хунда:При данном значении l (т. е. в пределах определенного подуровня) электроны располагаются таким образам, чтобы суммарный спин был максимальным.

Состояние электронов в атоме