Презентация на тему: Алканы

Алканы Кузнецов Илья 10 (4)

ПланХимические свойстваПолучениеПрименение

Особенности химических свойств предельных углеводородовТак как алканы - насыщеные углеводороды, то для них не характерны реакции присоединения, а только реакции замещения.Так как все связи в алканах ковалентные ( очень прочные ), тяжело разрываются, то реакции замещения идут очень тяжело ( t; свет ).

1. Свойства, общие с другими органическими веществами 1) ГорениеCH4 + 2O2 CO2 + 2H2Oметан2) Изомеризация t kH3C–CH2-CH2-CH3 H3C-CH-CH3 CH3 бутан метилпропан, изобутан

Запишите уравнения реакций горения этана и пропанаРешите задачу : какой объём воздуха необходим для сгорания 3 м3 бутана?

2. Собственные свойства алканов 1) ГалогенированиеCH4 + Cl2 CH3Cl + HCl ( 1 стадия )CH3Cl + Cl2 CH2Cl2 + HCl ( 2 стадия )СH2Cl2 + Cl2 CHCl3 + HCl ( 3 стадия )СHCl3 + Cl2 CCl4 + HCl ( 4 стадия )

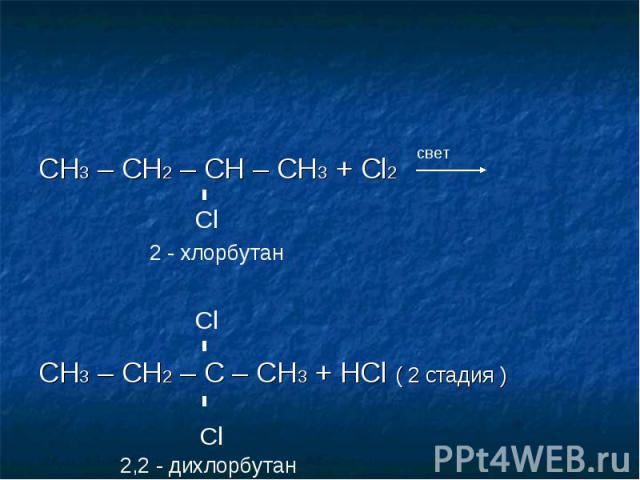
Особенности галогенирование алкановCH3 – CH2 – CH2 – CH3 + Cl2CH3 – CH2 – CH – CH3 + HCl ( 1 стадия )

CH3 – CH2 – CH – CH3 + Cl2 CH3 – CH2 – C – CH3 + HCl ( 2 стадия )

Домашнее задание Запишите уравнения реакции галогенирования бутана на 3, 4 и 5 стадиях. Назовите продукты этих реакций.Решите задачу: какой объём хлора потребуется для полного галогенирования 6 г этана?

2) Нитрование – реакция Коновалова СH4 + HO – NO2 CH3 – NO2 + H2O (HNO3)

Домашнее задание Запишите уравнения реакций последовательного нитрования этана до тринитроэтана.Решите задачу: найти массу нитропропана, образующегося из 22кг пропана, если массовая доля выхода продукта реакции составила 90%.

3) Дегидрирование – отрыв молекул водорода3) Дегидрирование – отрыв молекул водородаC2H6 C2H4 + H2

Запишите реакции получения пропена и пентена из соответствующих алканов.Решите задачу: найти массу и объём бутана, из которого был получен бутен объёмом 300 литров при объёмной доле выхода 85%?

Термическое разложение СH4 C + 2H2

Домашнее задание Запишите уравнения реакций термического разложения этана, пропана.Решите задачу: найти объёмную долю выхода газообразного водорода, образующегося при термическом разложении 127,6 г бутана, содержащего 10% углекислого газа, если известно, что в результате было получено 200л водорода.

4) Крекинг – разложение тяжелых углеводородов на более легкие.С16H34 C8H18 + C8H16C8H18 C4H10 + C4H8

Качественная реакция на предельные углеводороды Так как все связи в предельных углеводородах насыщенные, то эти вещества не обесцвечивают при обычных условиях бромную воду ( розового цвета ) и раствор перманганата калия.

3. Специфические свойстваОсобенности разложения метана 500°2CH4 C2H4 + 2H2 этен 1500°2CH4 C2H2 + 3H2 этин

Получение алканов 1. Природный способГазообразные алканы входят в состав природного и попутного нефтяного газов Жидкие – в состав нефти Твёрдые – в состав парафинов.

2. Промышленный способ1) Реакция соединения простых веществ t; C + 2H2 CH4 + Q ( 75 кДж ) 500°2) Синтез метана на основе водяного газаCO + 3H2 CH4 + H2O - Q

3. Лабораторный способ1) Синтез метана из ацетата натрия OCH3 C + NaOH CH4 + Na2CO3 О – Na твёрдый гидроксид карбонат натрия ( твёрдый ) натрия

2) Реакция удлинения цепи в 2 раза – реакция ВюрцаCH3 – Cl + Cl – CH3 + 2Na C2H6 + 2NaCl хлорметан этан хлорид натрия

Запишите уравнение реакций получения этана из соответствующей соли карбоновой кислоты.Решите задачу: найти объём пропана, образующегося при взаимодействии 184 г C3H7COONa c 20 г гидроксида натрия, если известно что реакция прошла на 70%.Запишите реакцию Вюрца для получения бутана из метана.Предложите схему получения этана из метана двумя разными способами. Запишите соответствующие уравнения реакций.

Метан – топливо, ценное химическое сырьё, из которого изготавливают: сажу ( идет на изготовление типографской краски и картриджей для принтера )водород ( идёт на производства аммиака , используется как восстановитель )непредельные углеводороды ( этен, ацетилен )хлорметан – хладоагент в холодильных установках.дихлорметан – растворитель.трихлорметан – растворитель.тетрохлорметан – растворитель, для тушения огня.нитрометан и другие нитроалканы – взрывчатые вещества.

Дегидрированием этана получают этилен – ценный химический продукт.Пропанобутановая смесь – топливо в быту.Жидкие алканы, входящие в состав нефти, идут на получение нефтепродуктов ( бензин, керосин, лигроин, газойль, мазут ).Твёрдые алканы входят в состав парафинов и используются в медицине и т.д.