Презентация на тему: Алканы

Тема урока Алканы.

План. Определение. Общая формула класса углеводородов. Гомологический ряд. Виды изомерии. Номенклатура алканов Строение алканов. Физические свойства. Способы получения. Химические свойства. Применение.

Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.) Алканы - углеводороды в молекулах которых все атомы углерода связаны одинарными связями (σ-) и имеют общую формулу:

Алканы - углеводороды в молекулах которых все атомы углерода связаны одинарными связями (σ-) и имеют общую формулу: Гомологи – это вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СH2. СН4 метан С2H6 этан C3H8 пропан C4H10 бутан C5H12 пентан C6H14 гексан C7H16 гептан C8H18 октан C9H20 нонан C10H22 декан

номенклатура алканов Алгоритм. Выбор главной цепи: CH3 – CH - CH2 - CH3 │ CH3

номенклатура алканов Алгоритм. Выбор главной цепи: CH3 – CH - CH2 - CH3 │ CH3

Номенклатура алканов 2. Нумерация атомов главной цепи: 1 2 3 4 CH3 – CH - CH2 - CH3 │ CH3
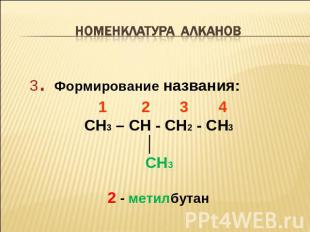
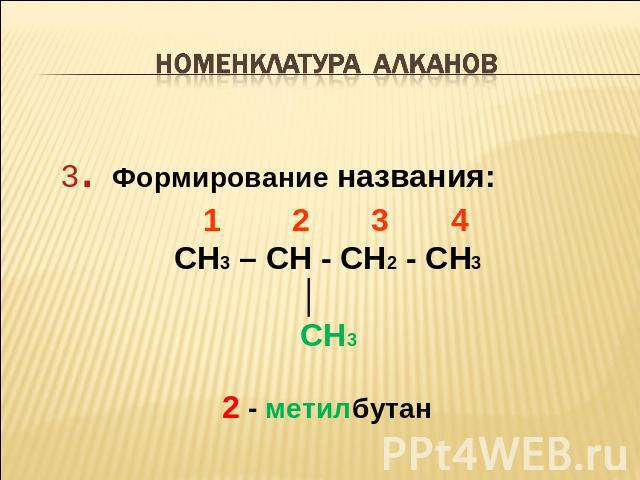
Номенклатура алканов 3. Формирование названия: 1 2 3 4 CH3 – CH - CH2 - CH3 │ CH3 2 - метилбутан

Радикал – это частица, имеющая неспаренные электроны.
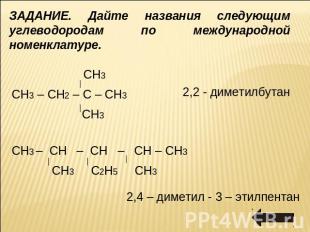
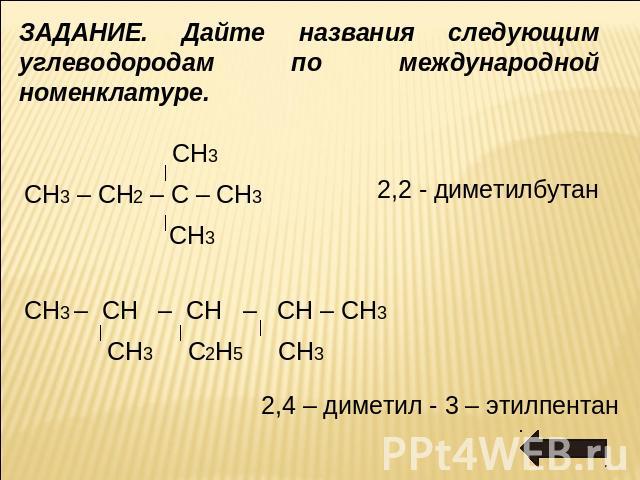
ЗАДАНИЕ. Дайте названия следующим углеводородам по международной номенклатуре. СН3 СН3 – СН2 – С – СН3 СН3 2,2 - диметилбутан СН3 – СН – СН – СН – СН3 СН3 С2Н5 СН3 2,4 – диметил - 3 – этилпентан
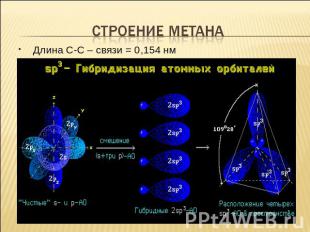
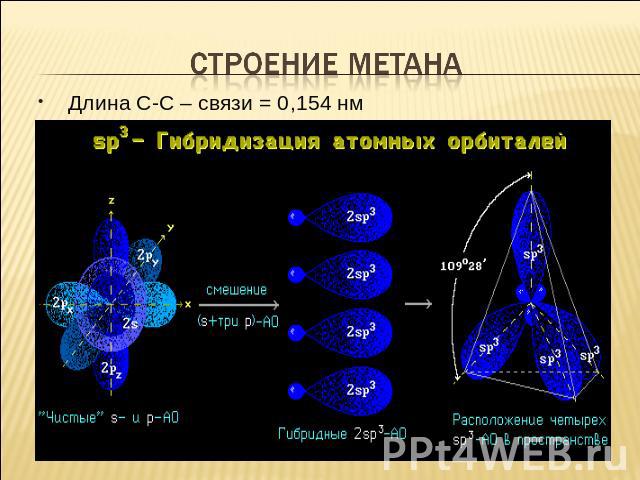
Строение метана

Строение метана
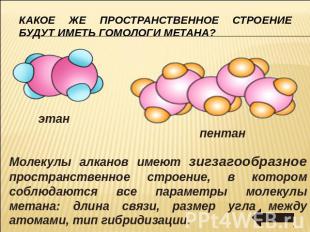
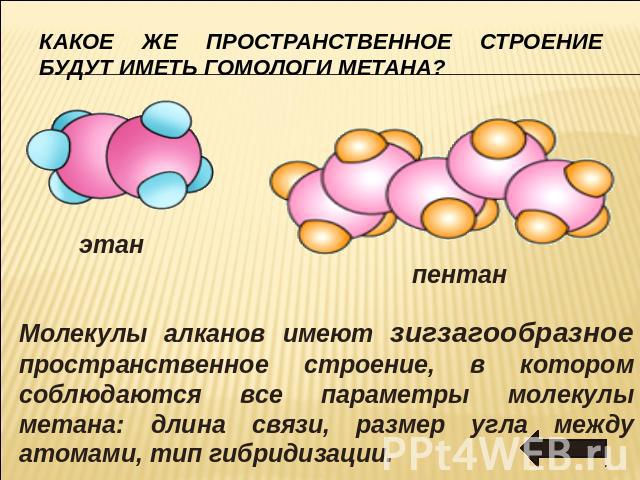
Какое же пространственное строение будут иметь гомологи метана? Молекулы алканов имеют зигзагообразное пространственное строение, в котором соблюдаются все параметры молекулы метана: длина связи, размер угла между атомами, тип гибридизации.

Физические свойства СН4…C4Н10 – газы T кипения: -161,6…-0,5 °C T плавления: -182,5…-138,3 °C С5Н12…C15Н32 – жидкости T кипения: 36,1…270,5 °C T плавления: -129,8…10 °C С16Н34…и далее– твёрдые вещества T кипения: 287,5 °C T плавления: 20 °C С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются их температуры кипения и плавления.

Получение алканов 1 –выделение углеводородов из природного сырья 2- гидрирование циклоалканов и непредельных углеводородов 3- декарбоксилирование натриевых солей карбоновых кислот 4- синтез Вюрца 5- гидролиз карбидов
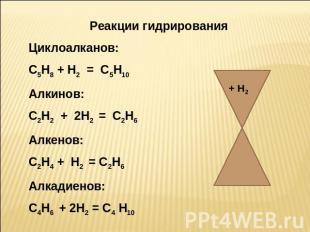
Реакции гидрирования Циклоалканов: С5Н8 + Н2 = С5Н10 Алкинов: С2Н2 + 2Н2 = С2Н6 Алкенов: С2Н4 + Н2 = С2Н6 Алкадиенов: С4Н6 + 2Н2 = С4 Н10

Получение алканов Получение метана при сплавлении ацетата натрия со щелочью: t C CH3COONa + NaOH CH4 + Na2CO3 ацетат натрия метан Свойства метана: 1) метан не вступает в реакцию окисления при действии водного раствора KMnO4; 2) метан не вступает в реакцию с раствором брома; 3) горение метана: CH4 + 2О2 СО2 + 2Н2О + Q

Синтез Вюрца проводят с целью получения алканов с более длинной углеродной цепью. Например: получение этана из метана 1 этап. Галогенирование исходного алкана СН4 + Сl2 = CH3Cl + HCl 2 этап. Взаимодействие с натрием 2CH3Cl + 2Na = C2H6 + 2NaCl

Метан в лаборатории можно получить гидролизом карбида алюминия Al4C3 + 12H2O = 4Al(OH)3 + 3CH4
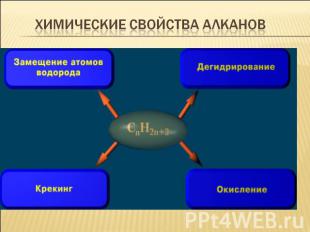
Химические свойства алканов

Химические свойства:1. Реакция замещения. Реакции протекают по радикальному механизму. 1) Реакция галогенирования: 1) Реакция галогенирования:

2. Реакции изомеризации: СН3 СН2 СН2 СН2 СН3 СН3 СН СН2 СН3 3.Реакции с водяным паром: СН4 + Н2О СО + 3Н2 синтез-газ 4. Реакции дегидрирования: 2СН4 Н С ≡ С Н + 3Н2 + Q СН3 СН3 Н2С=СН2 + Н2 + Q 5.Реакции окисления: Предельные углеводороды горят (пламя не коптящее) 3СО2 + 4Н2О + Q В присутствии катализаторов окисляются: 2СН3(СН2)34СН3 + 5О2 4СН3 (СН2)16СООН +2Н2О + Q

6. Реакция горения: CH4 + 2O2 → CO2 + 2H2O + Q

Применение Получение растворителей Получение ацетилена А также сырьё для синтезов спиртов, альдегидов, кислот. Горючее для дизельных и турбореактивных двигателей В металлургии

Применение алканов 1-3 – производство сажи (1 – картрижи; 2 – резина; 3 – типографическая краска) 4-7 – получение органических веществ (4 – растворителей; 5 – хладогентов, используемых в холодильных установках; 6 – метанол; 7 - ацетилен)

Проверка знаний Какие углеводороды относят к алканам? Запишите формулы возможных изомеров гексана и назовите их по систематической номенклатуре. Напишите формулы возможных продуктов крекинга октана 4. В каком объёмном соотношении смесь метана с воздухом становится взрывоопасной? 5. Каковы природные источники получения алканов? 6. Назовите области применения алканов

Домашнее задание Учебник О.С. Габриелян (10 класс базовый уровень) § 3, упр. 4, 7, 8 (стр. 32)