Презентация на тему: "Сера"

Химия элементов - неметаллов Сера Автор: Цуркан Лилия Фёдоровна учитель химии МОУ « ТСШ № 17» г. Тирасполь

Решаем загадки «Неметалы» Красив в кристаллах и парах, на детей наводит страх. Белый, воздуха боится, покраснел чтоб сохраниться. Хоть многие вещества превращает в яд, в химии она достойна всяческих наград.

Решаем загадки «Неметалы» Гость из космоса пришёл, в воздухе приют себе нашёл. Какой газ утверждает, что он - это не он? Какой неметалл является лесом?

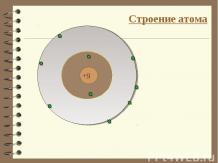
Сера - химический элемент Каков химический знак? В какой группе периодической системы находится? В каком периоде находится? Какой атомный номер? Какая относительная атомная масса? Сколько электронов в атоме? Как располагаются электроны на АО? Какая электронная формула серы? Какие низшая (в соединениях с водородом и металлами) и высшая (в соединении с кислородом) валентности серы?

Сера в природе

Сера также встречается в виде сульфатов солей серной кислоты - мирабилит

Пирит - огненный камень (соединение серы в природе)

Сера - жизненно важный химический элемент Сера входит в состав белков. Особенно много серы в белках волос, рогов, шерсти. Кроме этого сера является составной частью биологически активных веществ: витаминов и гормонов. При недостатке серы в организме наблюдается хрупкость и ломкость костей, выпадение волос.

Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца.

Физические свойства Твёрдое кристаллическое вещество желтого цвета, без запаха. Как и все неметаллы плохо проводит теплоту и не проводит электрический ток. Порошок серы всплывает в воде. Сера в природе практически не растворяется. Температура плавления 1200С.

Применение серы

Производство серной кислоты l стадия производства – обжиг: S + O2 =SO2 +297 кДж 4FeS2 + 11O2 = 8SO2 + 2Fe2O3 + 3400кДж ll стадия производства- окисление сернистого газа: 2SO2 + O2= 2SO3 + 197 кДж lll стадия производства – растворение оксида серы (Vl) в воде: SO3 + H2O = H2SO4 +Q

Любые процессы переработки природного сырья сопровождаются потерями вещества. Кроме того, не все реакции протекают до конца. Поэтому сырье используется не полностью. Эффективность его использования определяется выходом продукта- отношением массы полученного вещества к теоретически достижимой массе.

Рассмотрим пример - задачу. Сырье – пирит содержит 80% полезного вещества FeS2. При обжиге 1 т пирита было получено 800 кг сернистого газа. Определить выход продукта.

Стихотворение «Сера» Сера, сера, сера, эс. Тридцать два - атомный вес. Сера в воздухе сгорит, Мы получим ангидрид. Ангидрид её с водой Станет серной кислотой. Запишите уравнения химических реакций, о которых идет речь в стихотворении.
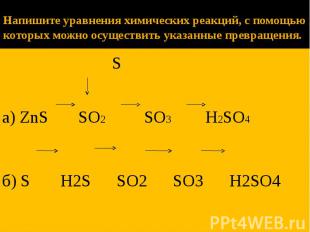
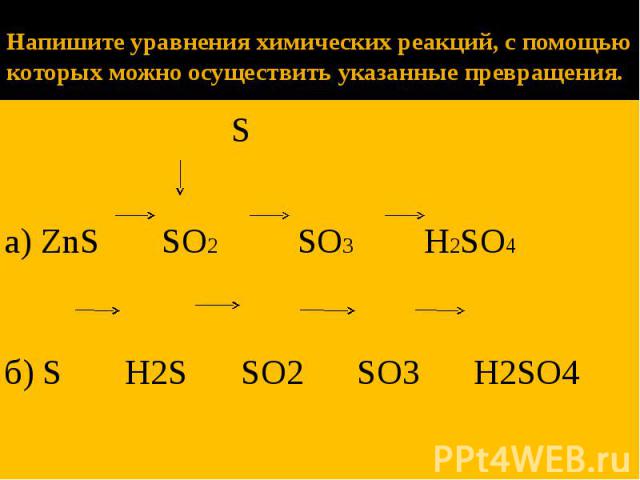
Напишите уравнения химических реакций, с помощью которых можно осуществить указанные превращения. S а) ZnS SO2 SO3 H2SO4 б) S H2S SO2 SO3 H2SO4

Задача: Каков объём (н.у.) а) сернистого газа получится при обжиге на воздухе 120г пирита FeS2; б) сероводорода получится при обработке 0,88 г сульфида железа (ll) соляной кислотой.

Домашнее задание & 19.1 ; задача № 15

за внимание! Спасибо